Clear Sky Science · fr
La mutation LRRK2R1627P amplifie l’inflammation chronique induite par des facteurs environnementaux et l’agrégation de α-synucléine dans l’intestin de rats
Pourquoi l’intestin compte dans une maladie cérébrale
La maladie de Parkinson est surtout connue pour les tremblements et les troubles moteurs, mais des preuves croissantes suggèrent que ses racines pourraient commencer loin du cerveau, au fond de l’intestin. Cette étude explore comment une modification génétique spécifique liée à Parkinson chez les populations asiatiques peut, combinée au vieillissement et à l’exposition à des toxiques, endommager progressivement l’intestin chez le rat. En observant ce qui se passe dans l’appareil digestif au cours de la vie des animaux, les chercheurs retracent comment des défenses immunitaires quotidiennes peuvent basculer vers une inflammation chronique, créant les conditions favorables à l’accumulation de protéines liées à la maladie qui pourraient, à terme, menacer le cerveau.
Un gène à risque dans le tube digestif
Les scientifiques se sont concentrés sur une variante d’un gène appelé LRRK2, depuis longtemps associé à la maladie de Parkinson et à certaines affections inflammatoires intestinales. Ils ont créé des rats portant la mutation homologue, nommée LRRK2R1627P, et les ont comparés à des rats normaux tout au long de leur vie. Bien que la quantité d’ARNm du gène LRRK2 dans l’intestin soit restée inchangée, la quantité totale de protéine LRRK2 et l’un de ses marqueurs d’activité clés ont diminué, indiquant que la mutation affaiblit la fonction normale de cette protéine dans l’intestin. Ce changement moléculaire subtil n’a pas causé de dommages précoces spectaculaires, mais il a discrètement modifié la manière dont les cellules intestinales se renouvellent et s’organisent à mesure que les animaux vieillissent.
Un intestin vieillissant sous tension lente et persistante
Au fil des mois, les rats porteurs de la mutation ont développé des signes évidents d’altération de la structure intestinale. Leur intestin grêle est devenu plus court, et les fines villosités et les cryptes qui absorbent les nutriments se sont réduites. Certaines cellules spécialisées de l’épithélium qui produisent le mucus protecteur et des substances antimicrobiennes — les cellules caliciformes et de Paneth — ont été diminuées, tandis que les protéines aidant les cellules voisines à former des jonctions étanches et résistantes aux fuites ont également chuté. Au microscope, ces jonctions sont devenues plus courtes ou plus larges, suggérant une barrière affaiblie. Il est important de noter que l’architecture globale ne s’est pas effondrée ; au contraire, l’intestin présentait un schéma plus insidieux de renouvellement et de protection réduits, ce qui le rend plus vulnérable aux irritations et aux infections. 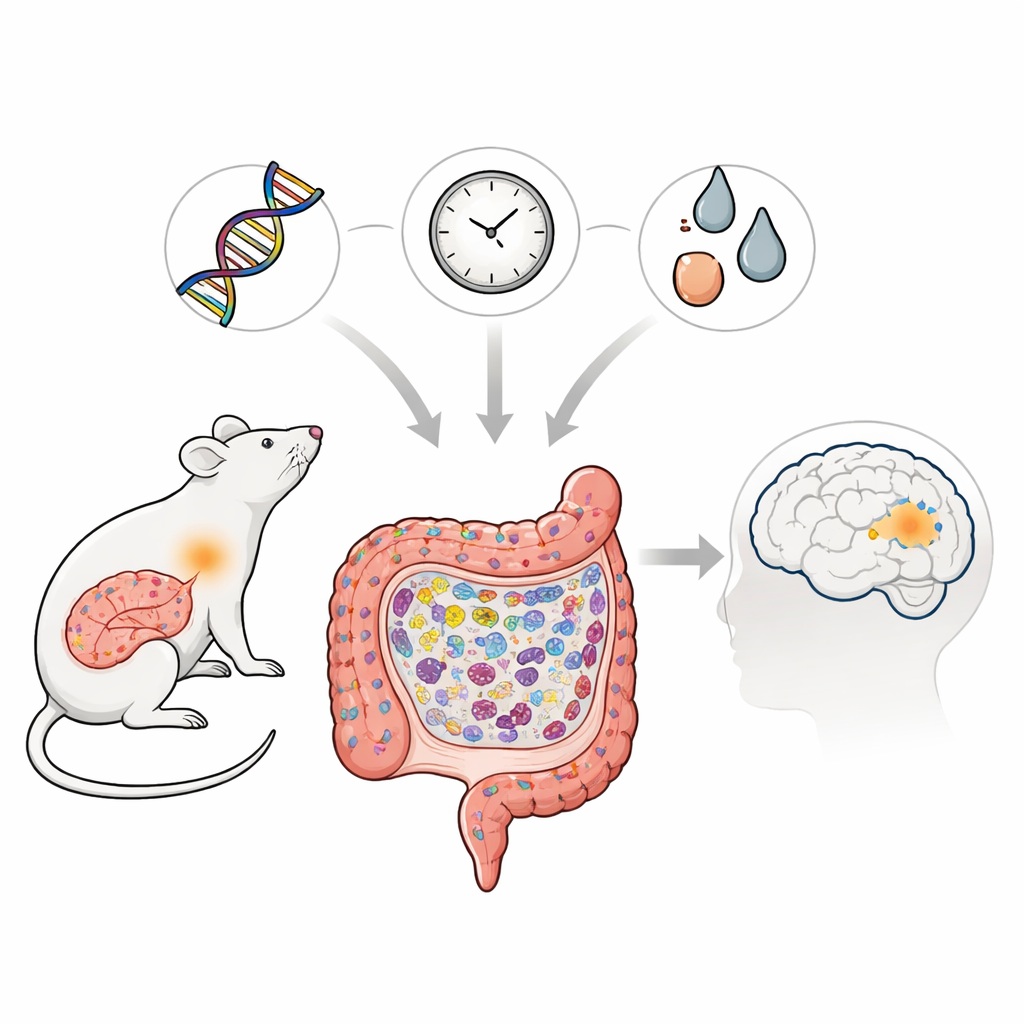
Système immunitaire sur le fil du rasoir
Pour comprendre pourquoi l’intestin basculait hors d’équilibre, l’équipe a examiné l’activité génique et les cellules immunitaires de la paroi intestinale. Ils ont constaté que des voies liées à un détecteur appelé TLR4 et à son partenaire NF-κB étaient hyperactives chez les rats mutants âgés. Ces détecteurs aident normalement l’organisme à repérer les microbes nuisibles, mais ici ils ont favorisé une accumulation de macrophages de type « combattant d’abord » appelés M1. Ces cellules ont sécrété des molécules inflammatoires, transformant l’intestin en un milieu chroniquement irrité. Fait frappant, la protéine liée à Parkinson, l’α-synucléine, sous sa forme phosphorylée associée à la maladie, a commencé à s’accumuler non pas dans les neurones intestinaux mais à l’intérieur de ces macrophages activés de l’intestin grêle, en particulier chez les animaux âgés.
Une sensibilité accrue aux agressions environnementales
La mutation génétique seule n’expliquait pas tout. Lorsque de jeunes rats ont été brièvement exposés à des toxines bactériennes (LPS), qui stimulent TLR4, les animaux porteurs de la mutation LRRK2 ont développé une inflammation intestinale bien plus sévère que leurs homologues normaux. Leur muqueuse a perdu davantage de cellules, les protéines de la barrière ont encore diminué, et les macrophages pro-inflammatoires ont augmenté, accumulant à nouveau une α-synucléine anormale. Cela suggère que les personnes porteuses de mutations analogues pourraient être particulièrement sensibles à des agressions environnementales perturbant l’intestin, comme certaines infections ou toxines, ce qui amplifie leur risque à long terme.
Atténuer le signal d’alarme
Parce que TLR4 se trouvait au centre de cette tempête inflammatoire, l’équipe a testé un médicament, TAK-242, qui atténue spécifiquement la signalisation de TLR4. Administré sur plusieurs mois à des rats d’âge moyen, l’inhibiteur a en grande partie restauré la longueur de l’intestin grêle, la taille des villosités et des cryptes, les cellules productrices de mucus et les protéines de la barrière. Il a réduit l’excès de macrophages, diminué les molécules inflammatoires et fortement réduit l’accumulation d’α-synucléine anormale dans l’intestin. Parallèlement, il a corrigé une communauté microbienne perturbée : la diversité a augmenté, une prolifération de Lactobacillus a diminué, et plusieurs groupes bactériens bénéfiques ont rebondi, tandis que les fonctions microbiennes prédites se sont éloignées de schémas associés à la maladie. 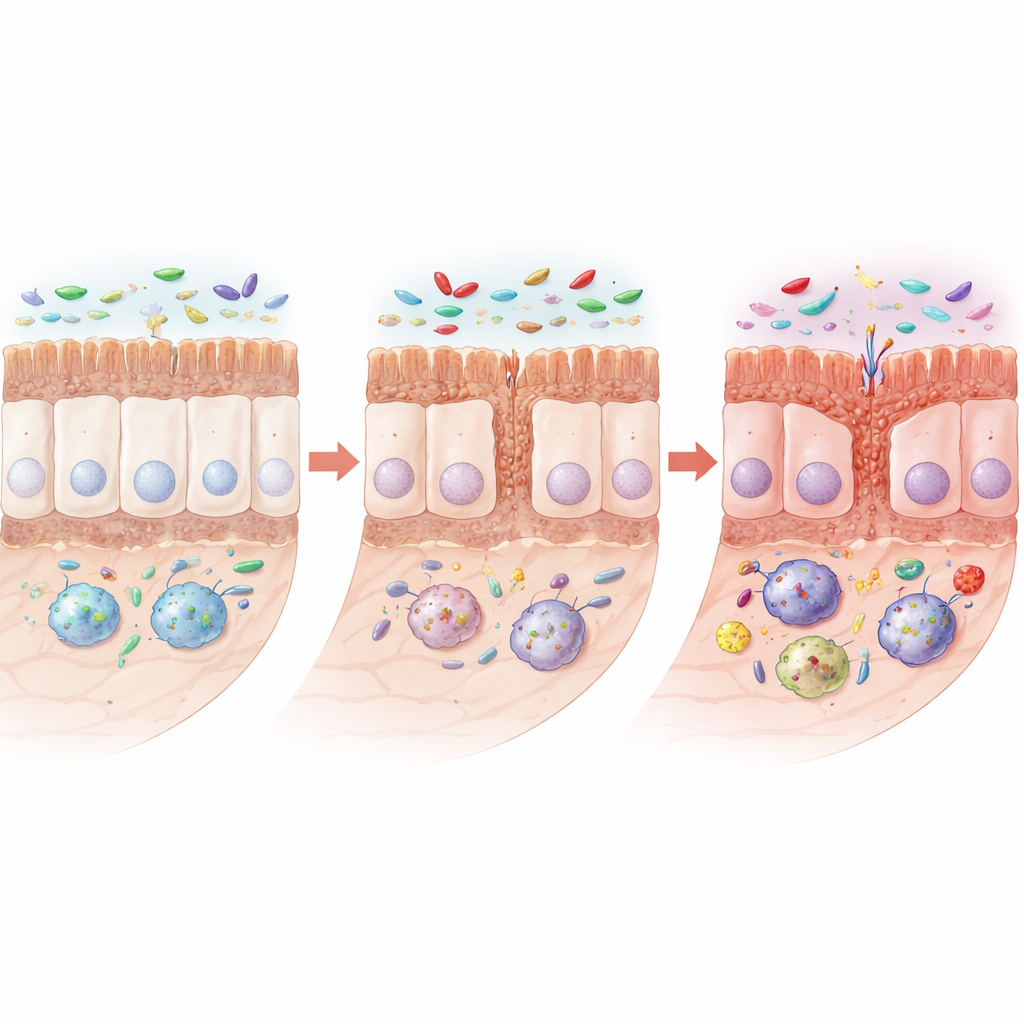
Ce que cela signifie pour le risque de Parkinson
Pour un non-spécialiste, le message est qu’un « gène de Parkinson » peut remodeler discrètement, au fil du temps, les défenses immunitaires de l’intestin, surtout en présence du vieillissement et du stress environnemental. Chez ces rats, le résultat est une inflammation chronique de bas grade qui affaiblit la barrière intestinale, perturbe les microbes résidents et provoque l’accumulation de la protéine liée à Parkinson dans des cellules immunitaires — pas encore une maladie de Parkinson manifeste, mais un contexte biologique qui pourrait favoriser une atteinte cérébrale ultérieure. En montrant que le blocage d’une unique voie immunitaire intestinale peut inverser bon nombre de ces changements, l’étude met en avant l’intestin comme une cible précoce et concrète : protéger la santé intestinale et maîtriser l’inflammation locale pourrait aider à retarder ou prévenir la maladie de Parkinson chez les personnes porteuses de risques génétiques.
Citation: Pang, S., Lu, J., Wang, Y. et al. LRRK2R1627P mutation amplifies environmental risk factors induced chronic inflammation and α-synuclein aggregation in the gut of rats. npj Parkinsons Dis. 12, 68 (2026). https://doi.org/10.1038/s41531-026-01281-3
Mots-clés: Maladie de Parkinson, inflammation intestinale, mutation LRRK2, microbiome, immunité innée