Clear Sky Science · fr
Évaluation systématique des régulateurs de la morphologie mitochondriale pour l’atténuation de l’α-synucléinopathie neuronale
Pourquoi ces minuscules centrales électriques comptent dans les maladies cérébrales
Les mitochondries, « centrales électriques » de la cellule, sont essentielles pour maintenir en vie les neurones et assurer le fonctionnement de leurs connexions. Dans des troubles cérébraux comme la maladie de Parkinson, ces structures minuscules apparaissent souvent endommagées ou fragmentées, mais il a été difficile de distinguer les altérations nocives des changements que l’on pourrait corriger en toute sécurité. Cette étude teste de manière systématique des « régulateurs de forme » mitochondriaux clés dans un modèle en laboratoire d’accumulation protéique liée à la maladie de Parkinson, en utilisant un outil d’intelligence artificielle pour mesurer la morphologie mitochondriale dans différentes parties des neurones. Le travail met en lumière un régulateur particulier, nommé Fis1, comme une cible prometteuse pour maintenir les mitochondries — et les synapses — en bonne santé sans provoquer d’effets secondaires indésirables.
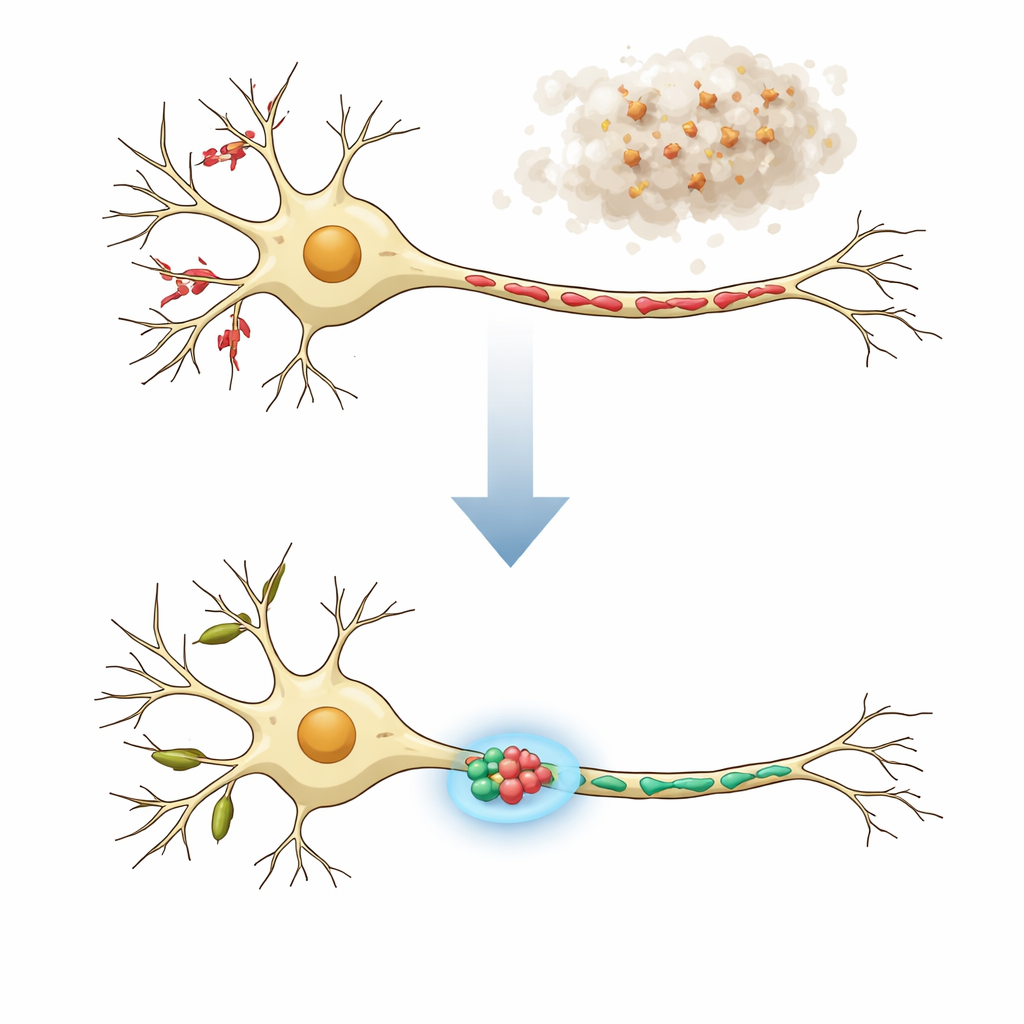
Les deux « quartiers » d’une cellule nerveuse
Les neurones ne sont pas homogènes : leurs branches en forme d’arbre (dendrites) et leurs longs câbles (axones) ont des fonctions différentes et hébergent des mitochondries aux morphologies distinctes. Dans les neurones sains, les dendrites contiennent plutôt des mitochondries longues et tubulaires qui soutiennent la production locale de protéines et la communication flexible au niveau des épines dendritiques. Les axones, qui transmettent les signaux, renferment de nombreux mitochondries courtes qui fournissent de l’énergie et aident à réguler le calcium aux terminaisons présynaptiques. Dans les maladies neurodégénératives, la fonction et la structure de ces mitochondries peuvent être perturbées, se manifestant par des fragments, des formes gonflées ou des chaînes perlées. Les auteurs estiment que des traitements réellement efficaces doivent restaurer les mitochondries dans les dendrites et les axones à leurs formes normales spécifiques à chaque compartiment.
Construire un test de contrainte de type Parkinson
Pour reproduire une caractéristique clé de la maladie de Parkinson et des troubles apparentés, les chercheurs ont exposé des neurones corticaux de souris en culture à des fibrilles préformées d’alpha-synucléine, une protéine susceptible de s’agréger en amas nocifs. En quelques jours, ces fibrilles ont amorcé une accumulation anormale d’alpha-synucléine dans les cellules et entraîné une fragmentation mitochondriale marquée dans les dendrites et les axones. Grâce à MitoVis, un système d’analyse d’images par apprentissage profond, l’équipe a pu séparer automatiquement dendrites et axones dans les images au microscope et mesurer la longueur, la surface et la forme de centaines de mitochondries par image environ dix fois plus vite que par traçage manuel. Cette approche à haut débit a confirmé que l’état de type pathologique raccourcissait les mitochondries et les rendait plus arrondies, en concordance avec des observations chez l’animal et sur des tissus de patients.
Tester les interrupteurs de forme mitochondriale
L’équipe a ensuite cherché à savoir si modifier l’activité de protéines spécifiques de fusion et de fission pouvait prévenir ces dommages. Augmenter deux protéines de fusion (Mfn1 et Mfn2) ou réduire l’expression d’une protéine de fission (Mff) a protégé les mitochondries dendritiques du raccourcissement induit par l’alpha-synucléine et a également préservé les épines dendritiques. Cependant, ces mêmes manipulations rendaient les mitochondries axonales excessivement longues, ce que des travaux antérieurs avaient associé à des problèmes de libération du signal et de ramification axonale. En revanche, réduire l’activité d’une autre protéine de fission, Fis1, a restauré la longueur mitochondriale dans les dendrites et les axones à des valeurs proches de la normale sans provoquer de sur-élongation. Fait important, dans ce dispositif, la diminution de Fis1 n’entraînait pas la mort neuronale et, comme les autres interventions, elle préservait la densité des épines dendritiques qui serait autrement diminuée sous le stress lié à l’alpha-synucléine.
Maintenir l’équilibre du calcium
Parce que les mitochondries axonales contribuent à tamponner le calcium lors de l’activité électrique, les chercheurs ont testé si la modification de leur morphologie altérait cet équilibre délicat. Ils ont utilisé un capteur fluorescent du calcium ciblé aux mitochondries dans les boutons présynaptiques et ont stimulé les axones par de brèves rafales de potentiels d’action. Dans la condition avec alpha-synucléine, la gestion du calcium par des mitochondries axonales légèrement raccourcies ressemblait à celle d’un état normal. Mais lorsque les mitochondries axonales étaient devenues excessivement longues du fait de la surexpression de Mfn1 ou de l’inhibition de Mff, elles absorbaient après stimulation plus de calcium que d’habitude. Cette augmentation de l’absorption pourrait perturber la fonction présynaptique. En revanche, l’inhibition de Fis1, qui normalisait sans dépasser la longueur mitochondriale, a préservé les réponses calciques mitochondriales proches de celles des contrôles sains, suggérant moins de compromis cachés.
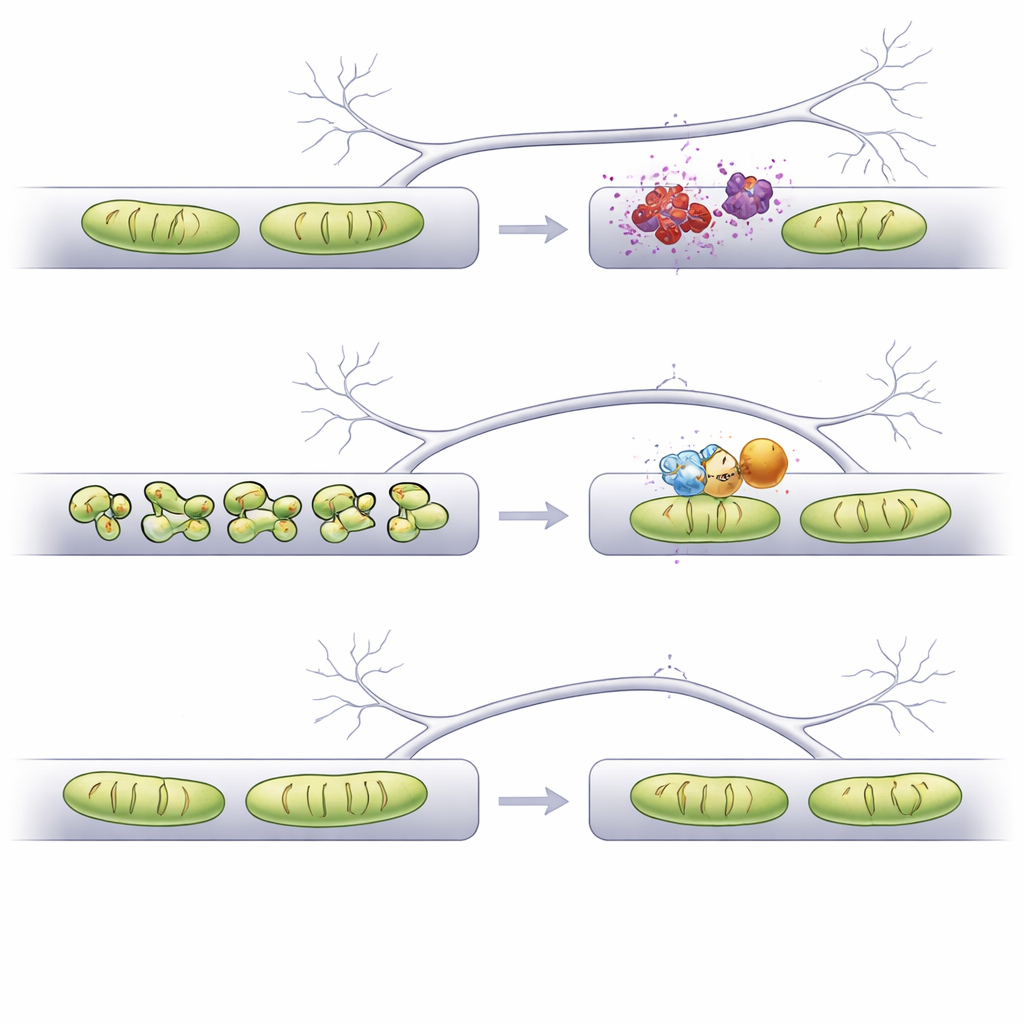
Ce que cela pourrait signifier pour des traitements futurs
Dans l’ensemble, l’étude montre que rallonger simplement les mitochondries ne suffit pas : il faut restaurer leur taille adéquate dans le bon compartiment. En utilisant un flux de travail d’imagerie assisté par IA, les auteurs identifient Fis1 comme une cible particulièrement intéressante : sa réduction stabilise la structure des mitochondries dans dendrites et axones, empêche la perte d’épines dendritiques et évite une gestion calcique anormale aux terminaisons présynaptiques. Ces résultats étayent l’idée qu’un réglage fin de la morphologie mitochondriale, éventuellement par des médicaments ou des molécules antisens ciblant Fis1, pourrait aider à protéger les synapses vulnérables dans l’alpha-synucléinopathie liée à la maladie de Parkinson et, peut-être, dans d’autres affections cérébrales où les mitochondries dysfonctionnent.
Citation: Kim, S.Y., Choi, J., Jang, D.C. et al. Systematic evaluation of mitochondrial morphology regulators for amelioration of neuronal α-synucleinopathy. npj Parkinsons Dis. 12, 58 (2026). https://doi.org/10.1038/s41531-026-01277-z
Mots-clés: Maladie de Parkinson, mitochondries, alpha-synucléine, dysfonction synaptique, neurodégénérescence