Clear Sky Science · fr
Utilité clinique des potentiels évoqués pour le réglage de la stimulation profonde du noyau sous‑thalamique dans la maladie de Parkinson
Pourquoi cette histoire de stimulateur cérébral est importante
Pour de nombreuses personnes atteintes de la maladie de Parkinson, les médicaments finissent par ne plus agir de façon régulière. Elles peuvent osciller entre raideur et mouvements incontrôlés, et l’ajustement du traitement devient un cycle frustrant de consultations. Cet article de synthèse examine comment les médecins peuvent utiliser les échos électriques du cerveau — appelés potentiels évoqués — pour programmer la stimulation cérébrale profonde (SCP) de manière plus rapide et plus objective. Essentiellement, il pose la question de savoir si l’on peut transformer la SCP d’un travail d’essais‑erreurs en un stimulateur cérébral plus personnalisé et guidé par les données.
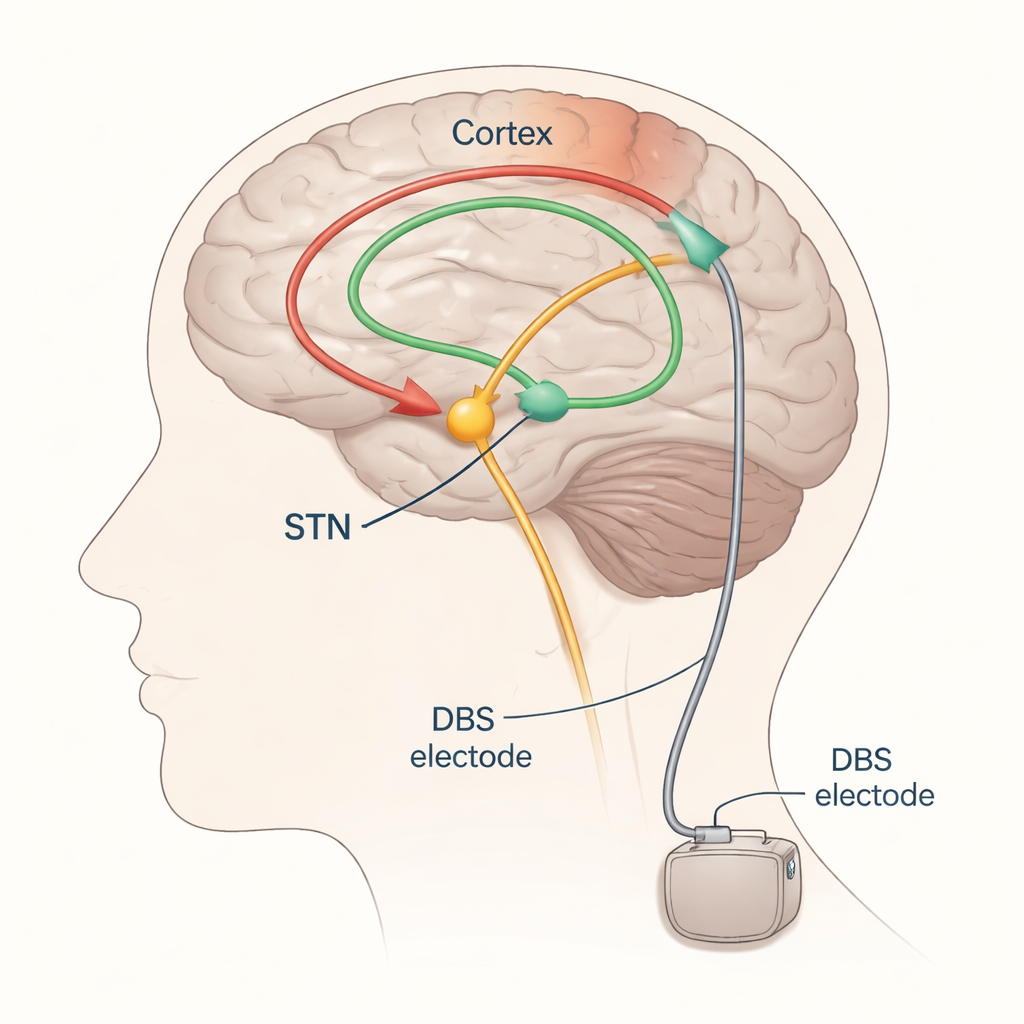
Du tâtonnement à l’ajustement guidé
La SCP pour la maladie de Parkinson cible le plus souvent une petite structure profonde du cerveau appelée noyau sous‑thalamique (NST). Des électrodes y sont implantées et connectées à un générateur d’impulsions placé sous la peau de la poitrine. Bien réglée, la stimulation du NST peut atténuer les tremblements, la lenteur et la raideur, mais si le champ électrique se propage trop loin, il peut stimuler par erreur des voies voisines qui contrôlent les muscles ou la sensibilité, provoquant des effets indésirables comme des contractures ou des picotements. Aujourd’hui, les neurologues ajustent généralement la SCP en modifiant lentement les paramètres et en observant les mouvements et les effets secondaires du patient — une approche qui prend du temps, dépend de l’état du patient le jour J et nécessite souvent plusieurs visites de suivi.
Écouter les échos électriques du cerveau
Les auteurs se concentrent sur les potentiels évoqués — de faibles réponses électriques synchronisées dans le cerveau ou les muscles après une stimulation — comme balises potentielles pour identifier des réglages de SCP favorables ou défavorables. Lorsqu’on stimule le NST, des ondes d’activité se propagent le long des voies nerveuses et peuvent être enregistrées au niveau du cuir chevelu avec un EEG, dans l’activité musculaire avec un EMG, ou parfois avec des détecteurs placés directement sur la surface du cerveau. En stimulant de façon répétée à basse fréquence et en moyennant les réponses, les chercheurs peuvent mettre en évidence des ondes distinctes qui apparaissent à différents délais (en millisecondes) après chaque impulsion. Les ondes précoces, arrivant en environ deux millièmes de seconde, reflètent principalement l’activation de voies motrices rapides passant près de l’électrode. Des ondes légèrement plus tardives, vers trois millisecondes (souvent appelées composante « P3 »), sont considérées comme provenant d’un lien direct entre le cortex frontal et le NST connu sous le nom de voie hyperdirecte. Des ondes encore plus tardives parcourent probablement des boucles plus longues incluant le thalamus et d’autres noyaux profonds.
Trouver la zone idéale et éviter les problèmes
À travers de nombreuses études, un schéma cohérent se dégage : les contacts de l’électrode de SCP qui produisent une composante P3 forte et de courte latence ont tendance à se situer dans la partie la plus utile du NST et sont associés à une meilleure amélioration des symptômes moteurs parkinsoniens ainsi qu’à une « fenêtre thérapeutique » plus large avant l’apparition d’effets indésirables. En revanche, des ondes très précoces liées aux voies motrices et certaines réponses autour de 8–10 millisecondes signalent souvent que la stimulation se propage vers des structures voisines, augmentant le risque de contractions musculaires ou d’autres effets indésirables. Des mesures séparées des potentiels moteurs évoqués (réponses EMG dans les muscles du visage et des membres) et des potentiels évoqués somesthésiques (signaux EEG liés aux voies tactiles) peuvent révéler une activation subtile de la capsule interne ou du lemnisque médial — faisceaux de fibres qui véhiculent les commandes motrices et l’information sensorielle. Détecter ces modifications tôt permet aux cliniciens d’orienter le courant loin des zones à risque en choisissant d’autres contacts ou en ajustant la forme et la polarité des impulsions.
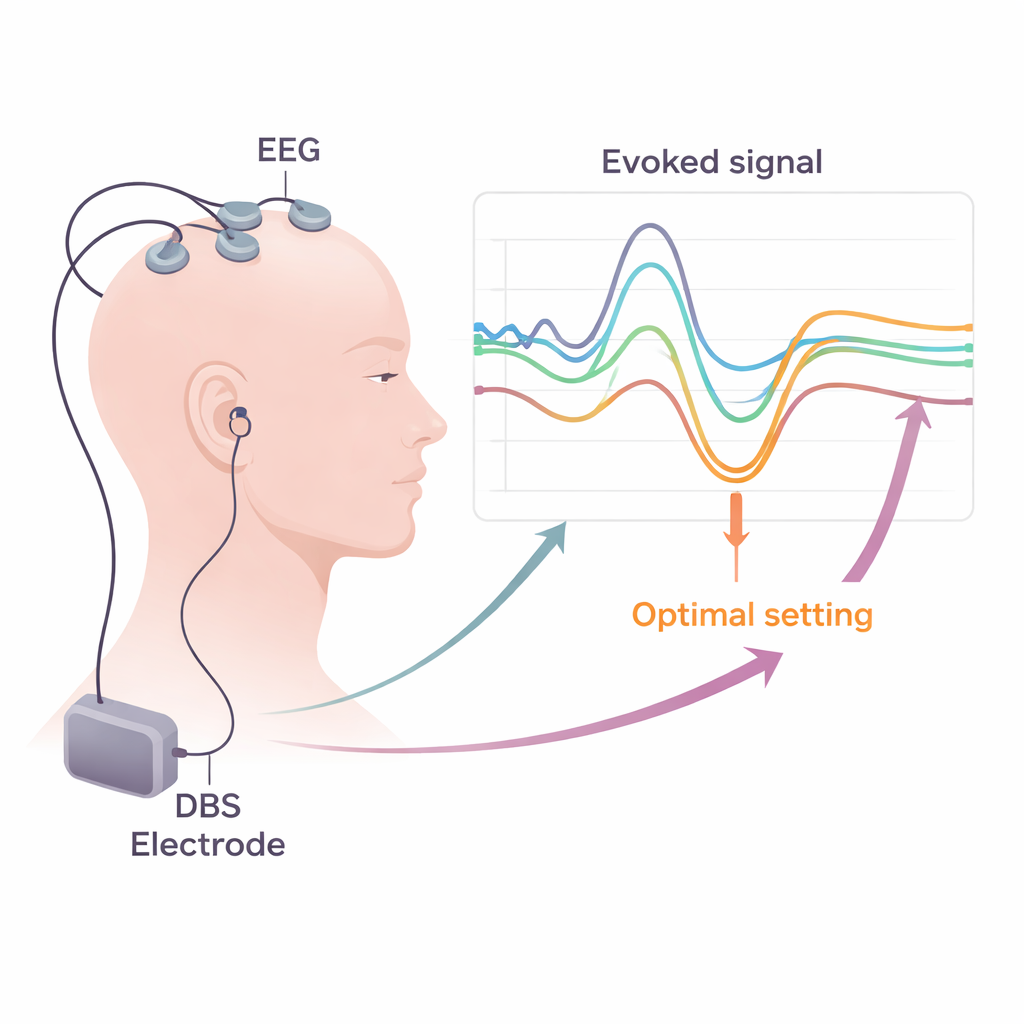
Rendre les outils de laboratoire pratiques en clinique
Transformer ces connaissances en soins de routine exige des solutions pratiques. La revue explique comment les systèmes EEG et EMG standard des hôpitaux peuvent déjà enregistrer la plupart des signaux nécessaires, à condition d’utiliser des fréquences d’échantillonnage élevées et des méthodes soignées pour supprimer le « bruit » électrique induit par les impulsions de SCP. Les auteurs discutent des stratégies pour réduire les artéfacts, telles que des règles de ré‑référencement astucieuses, la soustraction de modèles et des algorithmes informatiques avancés qui séparent l’activité cérébrale réelle des résidus de stimulation. Ils soutiennent que de courtes séances d’essai structurées — combinant de brèves périodes de SCP à basse fréquence, des enregistrements du cuir chevelu et une surveillance musculaire au repos et lors de contractions légères — pourraient être intégrées à la semaine de programmation post‑chirurgicale habituelle. Des cartes de potentiels évoqués pour chaque contact pourraient ensuite être combinées avec l’imagerie et d’autres biomarqueurs pour guider le choix des contacts et des paramètres à utiliser à long terme.
Ce que cela signifie pour les personnes atteintes de Parkinson
L’article conclut que les potentiels évoqués sont des candidats prometteurs pour rendre le réglage de la SCP plus précis, efficace et prévisible. En particulier, la composante P3 de courte latence semble être un marqueur solide indiquant que la stimulation atteint le bon circuit pour soulager les symptômes moteurs de la maladie de Parkinson, tandis que les réponses motrices et sensorielles évoquées peuvent alerter lorsque le courant fuit vers des voies provoquant des effets secondaires. Bien que des travaux supplémentaires soient nécessaires pour standardiser les techniques et démontrer les bénéfices en pratique courante, cette approche vise un avenir où les médecins pourraient « écouter » le cerveau pendant le réglage, cibler rapidement la zone idéale pour chaque patient et réduire le fardeau des essais‑erreurs pour les personnes vivant avec la maladie de Parkinson.
Citation: Hale, B., Latorre, A., Rocchi, L. et al. Clinical utility of evoked potentials for programming subthalamic deep brain stimulation in Parkinsons disease. npj Parkinsons Dis. 12, 54 (2026). https://doi.org/10.1038/s41531-026-01274-2
Mots-clés: Maladie de Parkinson, stimulation cérébrale profonde, potentiels évoqués, cartographie cérébrale, neurophysiologie