Clear Sky Science · fr
Modélisation du comportement de corrosion uniforme du zinc lors d'essais en brouillard salin
Pourquoi cela compte pour les pièces métalliques du quotidien
Des carrosseries de voiture aux lignes électriques, de nombreuses pièces métalliques sont protégées par de fines couches de zinc qui se dissolvent progressivement à la place de l’acier sous-jacent. Les ingénieurs s’appuient largement sur les « essais en brouillard salin » pour estimer la durée de vie de ces revêtements dans des environnements salés agressifs rappelant les routes hivernales ou l’air marin. Pourtant, ces essais sont souvent difficiles à interpréter et ne fournissent pas toujours des réponses quantitatives cohérentes. Cet article aborde ce problème en développant un modèle informatique fondé sur la physique qui prédit la vitesse d’usure des revêtements de zinc sous brouillard salin, avec l’objectif de transformer un test de laboratoire qualitatif en un outil de conception plus fiable.
Comment les revêtements de zinc protègent le métal
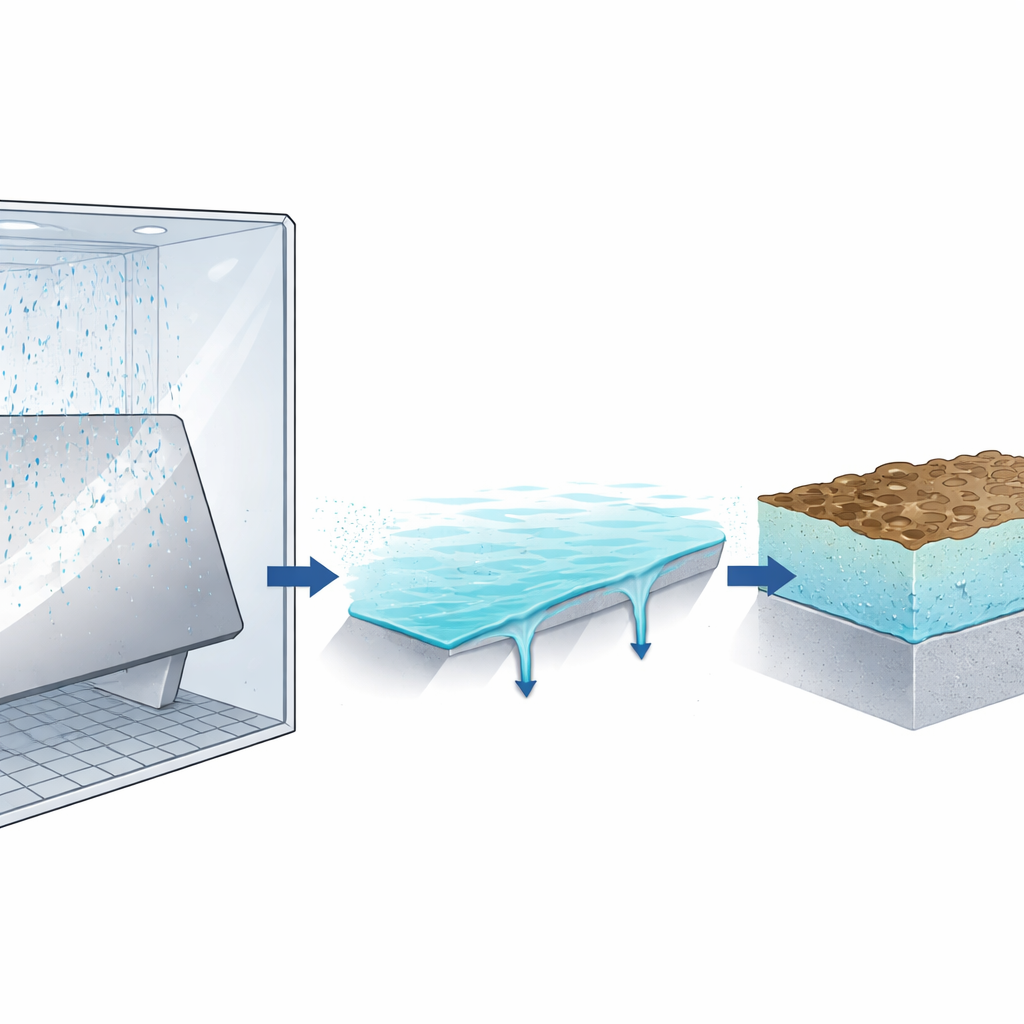
Les revêtements de zinc agissent comme des boucliers sacrificiels : ils se corrodent en premier, préservant l’acier en dessous. En présence d’eau salée, le zinc se dissout en particules chargées (ions), tandis que l’oxygène de l’air réagit pour former une fine couche initialement parsemée de produits de corrosion, principalement de l’hydroxyde de zinc et de l’oxyde de zinc. Avec le temps, cette couche croît et peut ralentir en partie l’attaque. Dans les chambres d’essai en brouillard salin, la surface n’est pas submergée dans une piscine d’eau. Au contraire, un film mince d’humidité salée se forme constamment à partir des gouttelettes pulvérisées, s’épaissit puis ruisselle en cycles. Ce film variable contrôle la quantité d’oxygène et de sel atteignant le métal et la vitesse d’accumulation des ions zinc, ce qui, à son tour, gouverne le taux de corrosion.
Construire un modèle de corrosion depuis les principes
Les auteurs ont développé un modèle numérique qui relie trois éléments clés : les réactions électrochimiques qui dissolvent le zinc, le transport des ions et de l’oxygène à travers la fine couche d’eau, et la formation de produits de corrosion solides qui créent une barrière en croissance. Ils décrivent le mouvement des ions par une équation de diffusion standard, simplifient les effets électriques et traitent la corrosion comme un mélange de processus contrôlés par la réaction et par la diffusion. Une relation particulière, l’équation de Brønsted–Bjerrum, ajuste la vitesse de formation de l’hydroxyde de zinc lorsque la concentration en sel dans le film d’eau devient très élevée, comme c’est souvent le cas dans une couche mince qui s’écoule lentement. Pour garder le modèle réaliste mais gérable, les auteurs supposent que la corrosion est uniforme à la surface et se concentrent uniquement sur la couche de zinc, sans inclure pour l’instant les dommages ultérieurs à l’acier sous-jacent.
Tester le modèle sur des expériences réelles
Pour ajuster le modèle, l’équipe a d’abord simulé un cas plus simple : du zinc pur immergé dans une solution saline diluée. Ils ont ajusté trois quantités incertaines — le taux de précipitation de l’hydroxyde de zinc, la facilité de déplacement des ions zinc dans le film, et la porosité de la couche d’oxyde — jusqu’à ce que les simulations correspondent aux mesures publiées de profondeur de corrosion, d’épaisseur d’oxyde et de zinc dissous dans le liquide. Cette calibration a montré, par exemple, qu’une précipitation plus rapide épaissit la couche d’oxyde et ralentit la corrosion en limitant l’accès de l’oxygène. Une fois calibrés, les mêmes paramètres ont été appliqués à un essai en brouillard salin beaucoup plus réaliste et neutre, mimant l’eau de mer du détroit de Kertch. Là, le modèle a capté un changement important : la corrosion est d’abord surtout gouvernée par les réactions de surface mais, à mesure que la couche d’oxyde et la concentration d’ions augmentent, elle devient limitée par la vitesse à laquelle les espèces peuvent diffuser à travers la couche de plus en plus encombrée.
Pourquoi le mouvement du film d’eau compte
Une caractéristique distinctive des essais en brouillard salin est le comportement instable du film d’eau mince. Les gouttelettes de pulvérisation épaississent progressivement la couche jusqu’à ce que la gravité et les forces de surface provoquent des ruissellements, entraînant le zinc dissous et amincissant brièvement le film. Les auteurs ont inclus cela en laissant l’épaisseur du film croître à un rythme choisi puis se réinitialiser périodiquement à une valeur plus petite, sur la base des périodes de ruissellement mesurées et des angles d’inclinaison des éprouvettes. Les simulations ont révélé que des débits de pulvérisation plus élevés et des angles d’inclinaison plus prononcés augmentent généralement la corrosion au début, en alimentant mieux la surface en solution fraîche. Des intervalles plus longs entre les événements de ruissellement laissent plus de temps à l’accumulation d’ions zinc, ce qui renforce les barrières de diffusion et peut ralentir la corrosion ensuite. Lorsque ces dynamiques de film sont prises en compte, et que la couche d’oxyde de zinc est supposée modérément poreuse, le modèle reproduit les vitesses de corrosion mesurées lors d’essais en brouillard salin généralement à environ 20 % près.

Ce que l’étude signifie pour la durabilité dans le monde réel
Pour faire simple, l’étude montre que la façon dont le film d’eau salée croît, se concentre et s’écoule d’une surface revêtue de zinc est tout aussi importante que la chimie du zinc lui‑même pour déterminer la vitesse à laquelle le revêtement disparaît. Un film d’eau périodiquement renouvelé empêche une accumulation excessive d’ions zinc et peut maintenir des taux de corrosion plus élevés, tandis qu’une croûte d’oxyde dense et continue peut ralentir la corrosion mais finir par se fissurer ou se détacher. En capturant ces compromis dans un seul modèle relativement efficace, ce travail fournit une base pour prédire de manière plus quantitative la durée de vie des pièces revêtues de zinc et pour étendre l’approche à des essais de corrosion industriels plus complexes comprenant des cycles de séchage, des variations de température et, finalement, l’apparition de la corrosion de l’acier une fois le zinc consommé.
Citation: Chen, C., Hofmann, M. & Wallmersperger, T. Modeling the uniform corrosion behavior of zinc in salt spray testing. npj Mater Degrad 10, 37 (2026). https://doi.org/10.1038/s41529-026-00749-0
Mots-clés: corrosion du zinc, essais en brouillard salin, revêtements en zinc, modélisation de la corrosion, film électrolytique