Clear Sky Science · fr
Système tétraèdre 4A : un cadre synergique pour l’intervention panvasculaire renforcé par l’électronique flexible
Repenser les soins pour nos vaisseaux sanguins
La maladie panvasculaire — l’atteinte des vaisseaux sanguins à l’échelle de l’ensemble du corps — est aujourd’hui la première cause de mortalité dans le monde. Elle peut toucher le cœur, le cerveau, les reins et les membres, souvent sans signes avant-coureurs. Cet article propose une nouvelle feuille de route audacieuse pour lutter contre ces troubles en s’appuyant sur des électroniques ultra‑fines et flexibles et sur l’intelligence artificielle. Plutôt que de concevoir chaque intervention comme un acte isolé, les auteurs envisagent un partenariat tout au long de la vie, fondé sur les données, entre le patient et l’appareil, depuis le diagnostic jusqu’à la chirurgie puis le suivi à long terme.
Une grande idée structurée en quatre piliers
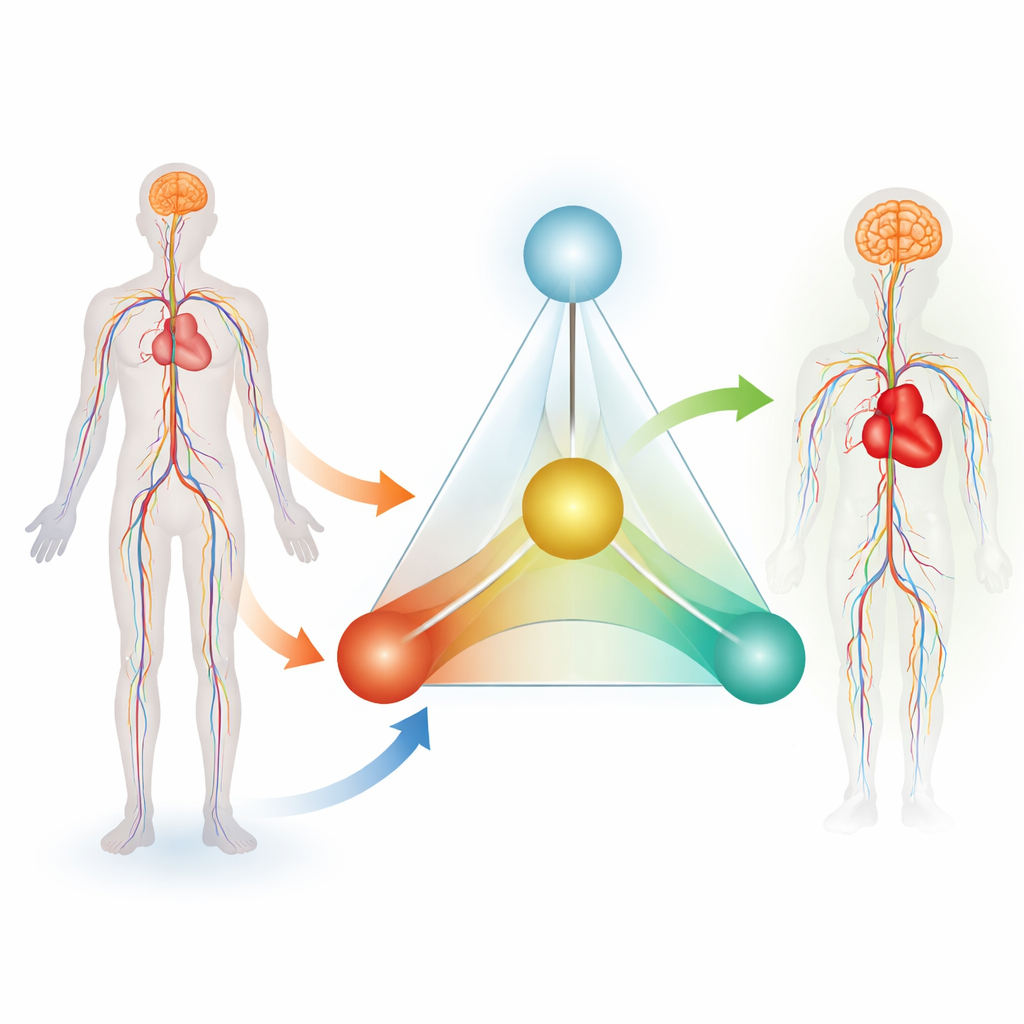
Les auteurs proposent ce qu’ils appellent le « Système tétraèdre 4A », un cadre en quatre parties pour gérer la maladie vasculaire comme un processus continu. Les quatre « A » sont Assessment (évaluation), Assistance, Aftercare (suivi) et AI‑retrofit (rétrofit IA). L’évaluation couvre la manière dont les médecins examinent à la fois le patient et les outils avant une procédure. L’assistance se concentre sur la navigation sûre des instruments dans les artères et les veines tortueuses pendant l’intervention. Le suivi traite de la surveillance du patient ensuite, idéalement en continu. Le rétrofit IA relie ces trois éléments : l’intelligence artificielle apprend de l’ensemble des données générées et renvoie des connaissances pour améliorer les dispositifs et les décisions futures. Ensemble, ces quatre éléments sont représentés par une base à trois faces (Évaluation, Assistance, Suivi) soutenant un sommet (IA), formant un tétraèdre qui incarne une boucle de soins fermée et auto‑améliorante.
Tests doux et implants plus intelligents
Dans la phase d’évaluation, les auteurs mettent en avant des patchs microneedle flexibles qui pénètrent à peine la peau pour prélever le fluide interstitiel. Ce fluide reflète de près la chimie sanguine et peut être prélevé de façon quasi indolore. Des capteurs intégrés dans ces petits aiguillons peuvent suivre des marqueurs d’inflammation, la fonction rénale, la glycémie et bien d’autres paramètres, effectuant ainsi une partie des analyses de laboratoire sur un patch porté sur la peau. Parallèlement, la revue décrit comment les implants traditionnels — stents, valves artificielles, dispositifs de fermeture des malformations cardiaques — pourraient être améliorés avec des capteurs ultra‑fins de pression, de composition chimique et de contrainte. Ces dispositifs « intelligents » n’auraient pas seulement pour but de rouvrir des vaisseaux bouchés ; ils mesureraient en continu les forces mécaniques, le comportement cellulaire et l’environnement chimique au niveau de l’implant, révélant si le vaisseau guérit réellement ou s’il dérive silencieusement vers une complication.
Guider les outils de l’extérieur vers l’intérieur
La phase d’assistance aborde un problème courant des interventions modernes : faire passer fils guides et cathéters à travers des réseaux vasculaires complexes tout en minimisant l’exposition aux rayons X et l’utilisation de produits de contraste. Les auteurs évoquent des patchs échographiques flexibles émergents et des sondes photoacoustiques capables de fournir des images en temps réel des vaisseaux sans radiation. Ils décrivent aussi des fils guides souples et des micro‑cathéters pilotables magnétiquement dont les pointes peuvent être déviées par des champs magnétiques externes et actionnées par des bras robotiques. Associés à des capteurs flexibles et à une imagerie intelligente, ces systèmes visent à faire cheminer des dispositifs à travers des vaisseaux d’un diamètre minime ou fortement sinueux avec une précision sub‑millimétrique, réduisant ainsi les risques de déchirures vasculaires, d’accidents vasculaires cérébraux ou d’échecs de procédure.
Vivre avec un réseau de gardiens silencieux
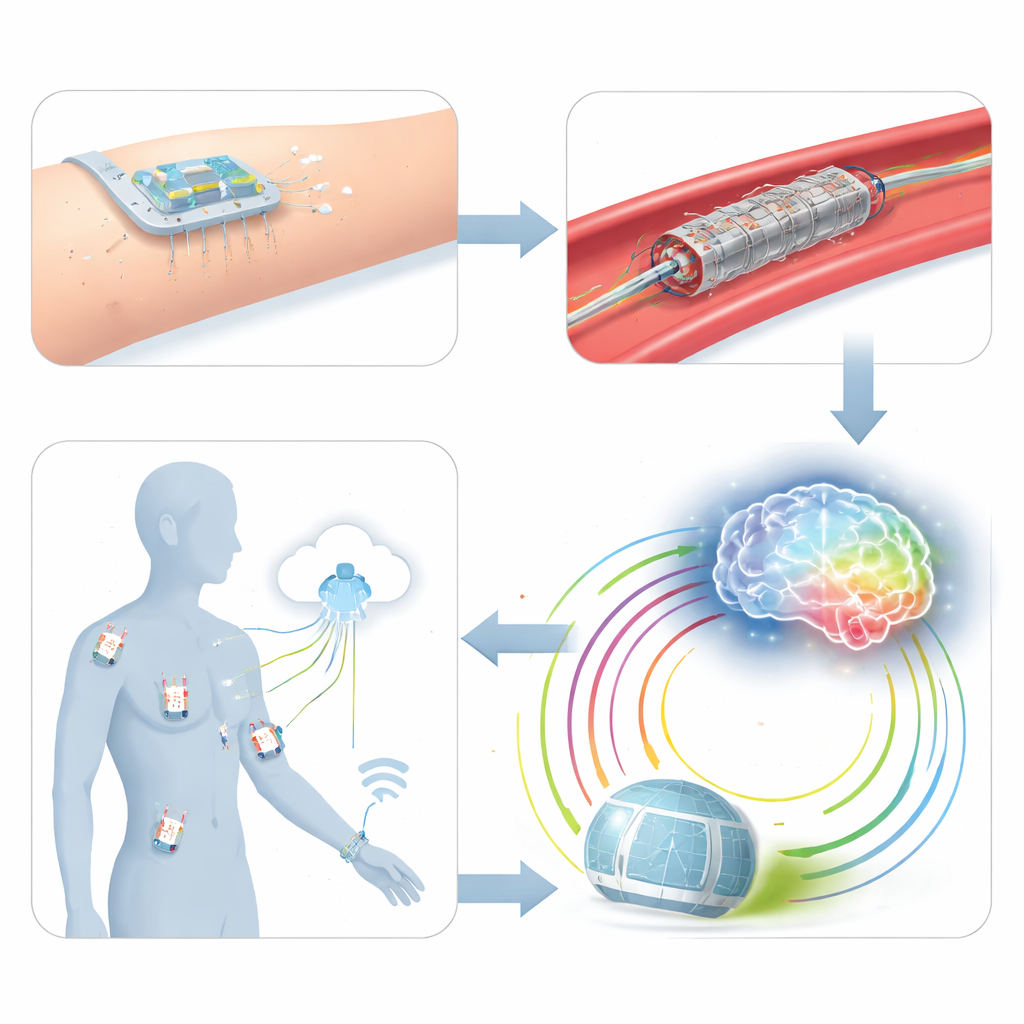
Après une intervention, de nombreux patients retrouvent aujourd’hui des visites cliniques sporadiques et des contrôles brefs, qui peuvent facilement manquer une resténose silencieuse ou la formation de caillots. Dans la phase de suivi, les auteurs imaginent une « Internet des objets médicaux » : un réseau de capteurs flexibles portables, semi‑implantables et entièrement implantables répartis à travers les organes et les profondeurs tissulaires. Des patchs cutanés pourraient surveiller le rythme cardiaque et la respiration, des microneedles suivraient la glycémie et des marqueurs inflammatoires, et des capteurs implantés sur des stents ou des artères observeraient la pression et le flux locaux. Tous ces capteurs transmettraient des données sans fil vers des systèmes cloud, créant un « réseau de capteurs médicaux sans fil » qui maintiendrait les médecins virtuellement au chevet et rendrait compte de l’évolution de la maladie à l’échelle du corps entier, pas seulement au niveau du site traité.
Laisser les algorithmes boucler la boucle
Au sommet du tétraèdre se trouve le rétrofit IA, où des algorithmes transforment des flux de capteurs bruts en soins améliorés. Des modèles d’apprentissage automatique peuvent aider à concevoir des microneedles plus fiables et des stents plus intelligents, reconnaître des schémas à risque dans les données chimiques et de pression avant l’apparition des symptômes, et guider les robots chirurgicaux le long de trajectoires plus sûres. L’apprentissage par renforcement profond — un logiciel qui apprend par essai‑erreur à partir de données historiques — pourrait suggérer comment ajuster les médicaments ou quand ré‑intervenir pour chaque patient. Des grands modèles de langage pourraient un jour synthétiser relevés de capteurs, images et dossiers médicaux en résumés clairs pour les cliniciens et en explications accessibles pour les patients. Dans cette vision, chaque procédure alimente le système en informations, affinant les décisions ultérieures.
Du concept aux soins quotidiens
Pour un lecteur non spécialiste, le message principal est que la prise en charge des maladies vasculaires peut passer de réparations isolées et réactives à un partenariat intelligent et continu entre le corps, l’électronique flexible et l’IA. Les patchs microneedle rendent les tests plus doux, les implants intelligents surveillent de l’intérieur les zones vulnérables, les capteurs portables et implantés suivent l’ensemble du corps, et les algorithmes d’apprentissage relient les informations sur des mois et des années. De nombreux obstacles subsistent — sécurité à long terme et alimentation énergétique, sécurité des données et réglementation — mais les auteurs soutiennent que, dans la décennie à venir, l’approche du tétraèdre 4A pourrait transformer les interventions vasculaires ponctuelles d’aujourd’hui en un système évolutif et personnalisé de protection contre le groupe de maladies le plus meurtrier au monde.
Citation: You, L., Qu, Y., Chen, Y. et al. 4A tetrahedron system: a synergistic framework for panvascular intervention empowered by flexible electronics. npj Flex Electron 10, 35 (2026). https://doi.org/10.1038/s41528-026-00537-5
Mots-clés: électronique flexible, maladies vasculaires, implants intelligents, capteurs portables, IA médicale