Clear Sky Science · fr
Le dépistage génomique néonatal semi-automatisé met en lumière la complexité des comptes rendus
Pourquoi de toutes petites gouttes de sang pourraient contenir de grandes réponses
Dans les jours qui suivent la naissance, la plupart des nouveau-nés passent déjà un test silencieux qui sauve des vies : un prélèvement au talon dont quelques gouttes de sang sont déposées sur une carte. Cette étude explore ce qui se passerait si l’on allait plus loin et lisait beaucoup plus du code génétique du bébé à partir de ce même prélèvement. Les chercheurs d’Australie-Méridionale ont voulu voir si l’ajout d’une analyse ADN à grande échelle aux contrôles néonataux routiniers pourrait, en toute sécurité, repérer plus tôt des affections traitables — sans submerger les familles et les médecins d’informations confuses ou peu utiles.
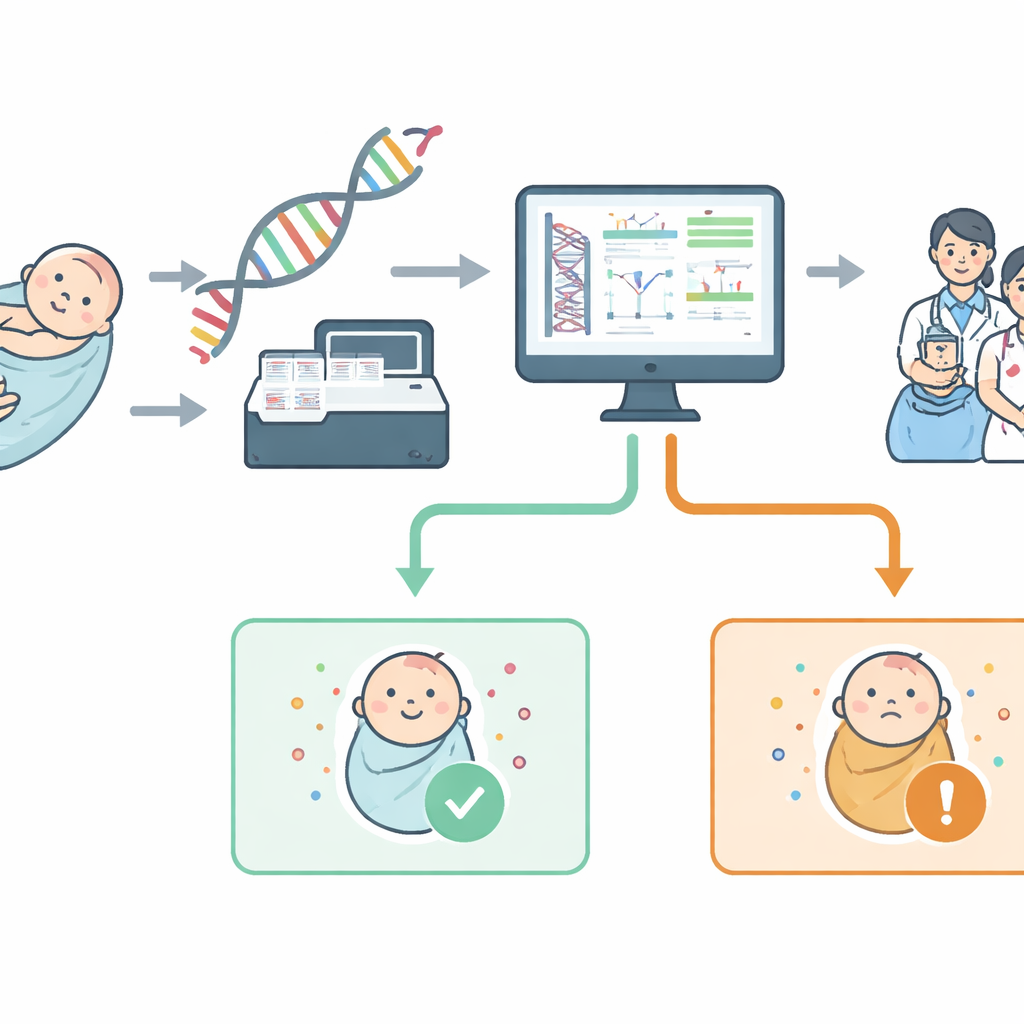
Du prélèvement au scan du génome
Le dépistage néonatal traditionnel recherche quelques dizaines d’affections en mesurant des substances chimiques dans le sang. En revanche, le dépistage génomique lit des segments d’ADN pour repérer directement des modifications causant des maladies dans des gènes précis. Le projet NewbornsInSA a conçu un test fondé sur le séquençage du génome complet, mais a délibérément limité la recherche à un « panneau virtuel » de 613 gènes. Ces gènes ont été choisis avec des médecins locaux selon des règles simples : l’affection doit débuter pendant l’enfance, entraîner des problèmes de santé sérieux, disposer d’une stratégie de traitement ou de prévention significative, et être détectable de manière fiable en laboratoire. Des groupes de patients et d’usagers ont ensuite aidé à regrouper ces affections en catégories correspondant aux systèmes corporels familiers afin que les parents comprennent mieux ce que couvre le test.
Mettre le nouveau test à l’épreuve
Avant de proposer ce contrôle basé sur l’ADN aux nouvelles familles, l’équipe devait démontrer son efficacité. Ils ont utilisé 46 cartes de sang conservées provenant d’enfants dont les diagnostics génétiques étaient déjà connus mais masqués aux analystes. En utilisant le séquençage du génome complet et deux systèmes logiciels distincts, ils ont vérifié si leur pipeline identifiait correctement les nouveau-nés qui avaient effectivement l’une des affections ciblées. Le résultat est encourageant : le processus a trouvé 97 % des cas véritables et n’a produit aucune fausse alerte après examen par des experts. Le cas manqué a mis en évidence une limite clé de tout dépistage fondé sur les gènes — lorsque les preuves scientifiques autour d’une variation d’ADN particulière sont incomplètes, les ordinateurs et même les experts peuvent être contraints de la qualifier « d’incertaine » et de la considérer comme un non-résultat.
Laisser les ordinateurs faire le gros du travail
La lecture d’un génome entier génère des milliers de variants pour chaque bébé, bien trop nombreux pour être examinés un par un par des humains. Pour gérer cela, les chercheurs ont construit un flux de travail semi-automatisé. Des scripts personnalisés, intégrés à une plateforme d’analyse commerciale, passent en revue la liste annotée des variants et écartent automatiquement les nouveau-nés qui ne présentent manifestement aucune anomalie préoccupante, les étiquetant comme « faible probabilité ». Seuls les cas présentant des modifications potentiellement nocives — comme des variants connus causant des maladies ou des perturbations probablement délétères d’un gène — sont transmis à des analystes experts pour un examen approfondi. Parmi les 100 premiers nouveau-nés réels testés, cette automatisation a immédiatement réduit de plus de moitié le nombre de bébés nécessitant un examen manuel, une étape cruciale si ce type de dépistage doit être étendu à l’ensemble de la population.
Bébés réels, décisions réelles
Lorsque l’équipe a appliqué le flux de travail aux 100 premiers nouveau-nés inclus, cinq bébés ont reçu des résultats suggérant une forte probabilité d’une affection spécifique. Il s’agissait notamment de troubles du rythme cardiaque pouvant provoquer des battements irréguliers dangereux, d’un problème métabolique déjà suspecté par le dépistage standard, d’une variation génétique rendant certains antibiotiques risqués pour l’audition, et d’une forme légère d’hyperglycémie héréditaire. Dans chaque cas, le résultat a déclenché un suivi adapté : bilans cardiaques et surveillance continue, alertes électroniques pour éviter certains médicaments, ou planification des soins lors de grossesses futures. Dans le même temps, de nombreux autres résultats n’ont pas été signalés délibérément car ils étaient liés à des symptômes bénins, à des cancers d’apparition à l’âge adulte, à des risques incertains ou à des schémas complexes que les connaissances actuelles ne permettent pas d’interpréter avec confiance chez un nouveau-né sain. Ces décisions délicates ont exigé des heures de lecture de la littérature et de discussions entre généticiens et spécialistes, soulignant que le jugement d’expert reste nécessaire.
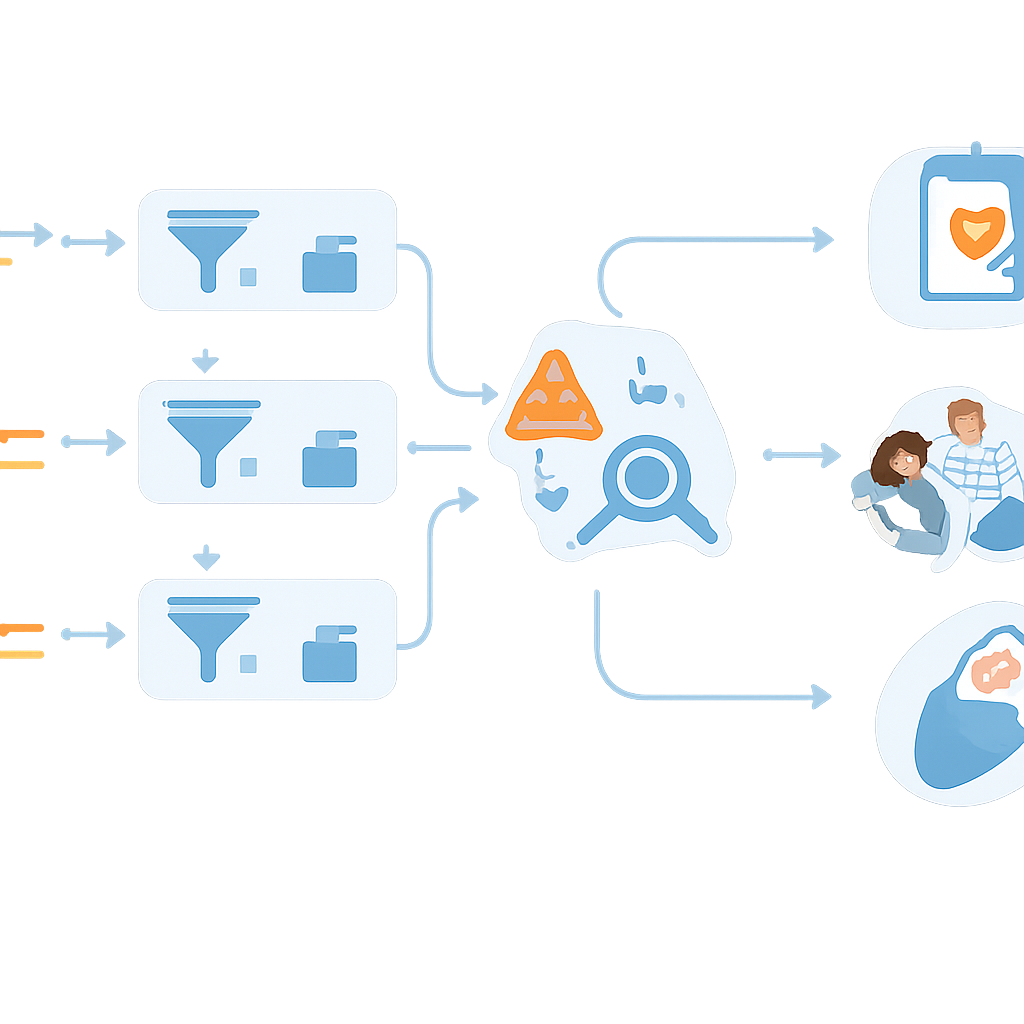
Concilier aide précoce et fardeau futur
Ce travail montre qu’il est techniquement possible d’utiliser les données du génome complet issues d’une minuscule tache de sang pour détecter davantage d’affections infantiles traitables que les tests standard, avec une grande précision et l’appui de logiciels intelligents. Mais il met aussi à nu le fil éthique et pratique sur lequel il faut marcher : chaque gène supplémentaire contrôlé augmente la probabilité de découvrir des informations qui n’aideront pas le bébé maintenant, inquiéteront les parents ou ne deviendront pertinentes que des décennies plus tard. L’approche semi-automatisée et soigneusement organisée de l’équipe NewbornsInSA — où les ordinateurs écartent les négatifs évidents et où les humains se concentrent sur les cas nuancés — offre une feuille de route pour un déploiement responsable du dépistage génomique néonatal, tandis que des études de suivi en cours évaluent ses bénéfices et risques réels pour les familles.
Citation: Chowdhury, A., Marri, S., Anastasi, L. et al. Semi-automated genomic newborn screening highlights complexities in reporting. npj Genom. Med. 11, 13 (2026). https://doi.org/10.1038/s41525-026-00553-4
Mots-clés: dépistage néonatal génomique, séquençage complet du génome, taches de sang séché, interprétation des variants génétiques, détection précoce des maladies rares