Clear Sky Science · fr
Analyse transcriptomique pour découvrir le mécanisme de radiosensibilisation des cancers du sein triple négatifs AR-positifs par inhibition du récepteur aux androgènes
Pourquoi cette étude compte pour les personnes confrontées au cancer du sein
La radiothérapie est un pilier du traitement pour de nombreuses personnes atteintes de cancers du sein agressifs, mais certaines tumeurs sont naturellement plus difficiles à détruire par les rayonnements que d’autres. Cette étude pose une question pratique aux enjeux cliniques réels : une classe de médicaments qui bloquent les signaux hormonaux masculins, déjà utilisée en cancer de la prostate, peut-elle rendre un sous‑ensemble de cancers du sein triple négatifs plus vulnérable à la radiothérapie — et pourquoi cela fonctionne dans certains cas mais pas d’autres ?
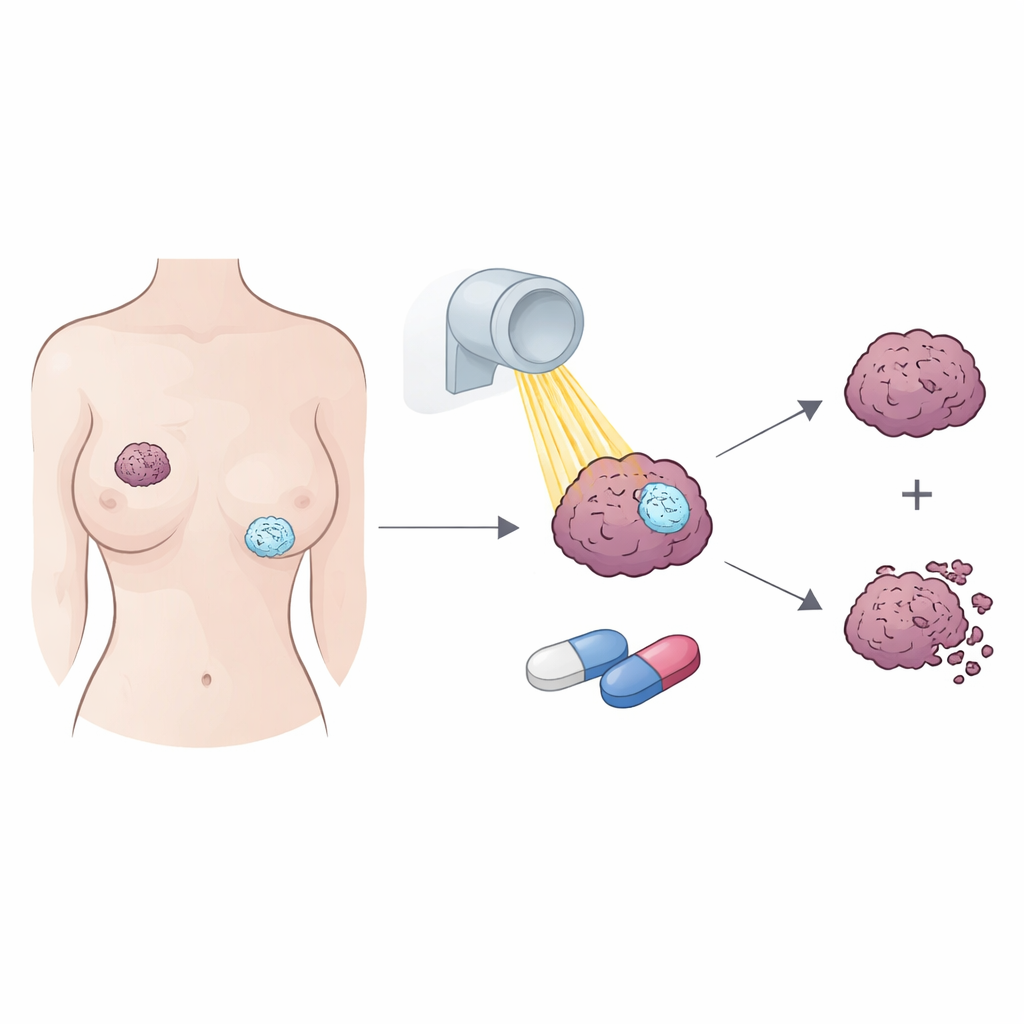
Une forme de cancer du sein difficile à traiter
Les cancers du sein triple négatifs ne présentent pas trois cibles moléculaires courantes — récepteurs estrogeniques, récepteurs progestatifs et HER2 — si bien que les patient·es doivent souvent se reposer uniquement sur la chirurgie, la chimiothérapie et la radiothérapie. Cependant, une partie de ces tumeurs exprime le récepteur aux androgènes, une protéine qui répond à des hormones apparentées à la testostérone et peut stimuler la croissance tumorale. Des travaux antérieurs ont montré que bloquer ce récepteur peut ralentir ces cancers et pourrait renforcer les effets de la radiothérapie, mais les détails du mécanisme et les médicaments ou tumeurs qui en bénéficient le plus restaient incertains.
Tester des bloqueurs hormonaux modernes avec la radiothérapie
Les chercheur·ses ont étudié plusieurs modèles en laboratoire de cellules de cancer du sein triple négatif qui différaient principalement par la quantité de récepteur aux androgènes exprimée. Ils se sont concentrés sur deux anti-androgènes récents, l’apalutamide et le darolutamide, et ont combiné des expositions courtes à ces médicaments avec des doses standard de rayons X. Dans les cellules exprimant des niveaux élevés de récepteur aux androgènes, l’apalutamide augmentait nettement les dommages induits par les radiations, laissant moins de cellules capables de former de nouvelles colonies. Le darolutamide, en revanche, avait peu ou pas d’effet sur la sensibilité aux radiations dans ces mêmes cellules, et aucun des deux médicaments n’aidait les cellules exprimant très peu le récepteur. Ces résultats suggèrent que tous les bloqueurs des androgènes n’agissent pas de la même manière dans le cancer du sein, et que les tumeurs doivent dépendre fortement de ce récepteur pour que la combinaison soit efficace.
Observer le déplacement d’une protéine clé à l’intérieur de la cellule
Pour comprendre ce qui se passe à l’intérieur des cellules cancéreuses après la stimulation hormonale ou la radiothérapie, l’équipe a suivi la localisation du récepteur aux androgènes. Lorsque les cellules étaient exposées à un androgène synthétique, le récepteur se déplaçait dans le noyau, le centre de contrôle où les gènes sont activés ou réprimés. La radiothérapie seule n’expulsait pas le récepteur du noyau ; en réalité, il y restait après le traitement, prêt à influencer l’activité génique. Cependant, lorsque les cellules recevaient l’anti-androgène enzalutamide avant la radiothérapie, les niveaux nucléaires du récepteur diminuaient et une plus grande part restait dans le cytoplasme. Cela étaye l’idée que bloquer l’entrée nucléaire du récepteur gêne sa capacité à lancer un programme génique protecteur après irradiation.
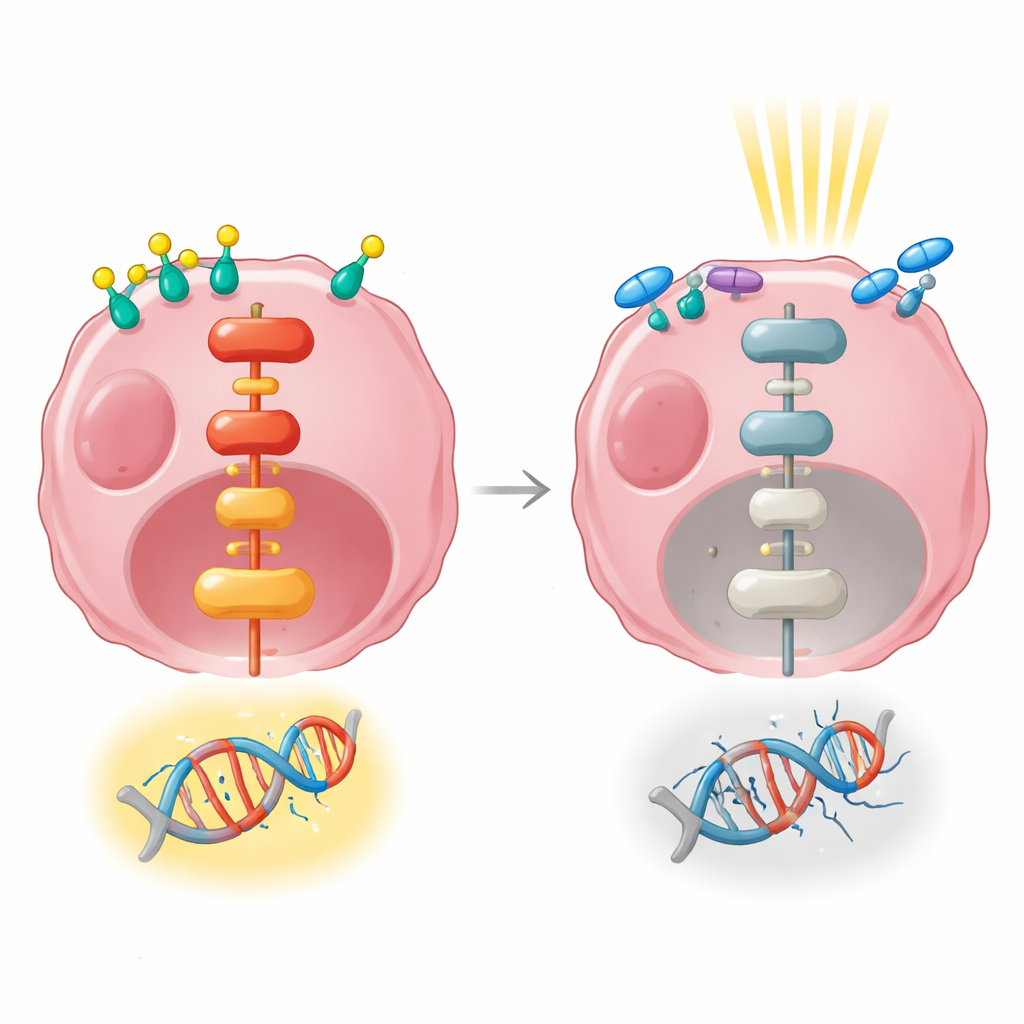
Signaux géniques reliant les hormones à la résistance
Les investigateur·rices ont ensuite utilisé le séquençage de l’ARN pour obtenir un panorama large des gènes dont l’activité augmentait ou diminuait après stimulation hormonale, radiothérapie, ou les deux. Le traitement hormonal seul modifiait l’activité de centaines de gènes et affectait fortement des voies contrôlant la croissance cellulaire, l’adhésion et la communication avec l’environnement. La radiothérapie administrée seule, à un court terme, modifiait beaucoup moins de gènes. Lorsque la stimulation hormonale et la radiothérapie étaient combinées, de nombreuses voies liées à la croissance étaient activées, y compris une voie de signalisation majeure connue sous le nom de MAPK/ERK, qui relaie des signaux de la surface cellulaire vers le noyau. Cette voie est connue pour aider les cellules à survivre et à réparer les dommages de l’ADN.
Explorer une voie de survie qui protège l’ADN
Parce que la signalisation MAPK/ERK revenait systématiquement dans leurs analyses, les chercheur·ses ont testé si l’activation de cette voie pouvait annuler l’avantage de l’inhibition des androgènes pendant la radiothérapie. Ils ont modifié des cellules cancéreuses pour surexprimer une version constitutivement active d’ERK, un élément clé de la voie, puis ont répété le traitement radiations plus apalutamide. Dans ce contexte, l’apalutamide n’augmentait plus la sensibilité des cellules aux radiations : le signal ERK amplifié semblait les protéger. Avec les mesures protéiques, ces résultats désignent la signalisation MAPK/ERK comme un lien critique entre l’activité du récepteur aux androgènes et la capacité de la cellule à réparer les cassures de l’ADN induites par les rayonnements.
Ce que cela signifie pour les soins futurs du cancer du sein
Concrètement, ce travail suggère que certaines tumeurs triple négatives survivent à la radiothérapie en utilisant des signaux liés aux androgènes pour activer un circuit interne de survie qui les aide à réparer l’ADN endommagé. Des médicaments comme l’apalutamide et l’enzalutamide peuvent interrompre ce circuit dans les tumeurs qui dépendent fortement du récepteur aux androgènes, rendant la radiothérapie plus efficace, tandis que les tumeurs à faible expression du récepteur ou dotées de voies de survie alternatives peuvent ne pas en tirer profit. En cartographiant les voies géniques impliquées — en particulier la voie MAPK/ERK — cette étude prépare le terrain à des combinaisons plus ciblées d’inhibiteurs hormonaux, d’inhibiteurs de voies et de radiothérapie qui pourraient améliorer les résultats pour les patient·es atteints de cette forme difficile du cancer du sein.
Citation: McBean, B., Hauk, B., Michmerhuizen, A.R. et al. Transcriptomic analysis to uncover the mechanism of radiosensitization of AR-positive triple-negative breast cancers with AR inhibition. npj Breast Cancer 12, 50 (2026). https://doi.org/10.1038/s41523-026-00916-1
Mots-clés: cancer du sein triple négatif, récepteur aux androgènes, radiothérapie, radiosensibilisation, signalisation MAPK ERK