Clear Sky Science · fr
Réseaux JAK/STAT1-interféron-ISGylation dans la résistance du cancer du sein aux inhibiteurs de FOXM1 et de CDK4/6
Pourquoi cela compte pour le traitement du cancer du sein
De nombreuses femmes atteintes d’un cancer du sein récepteur aux œstrogènes–positif (ER+) reçoivent aujourd’hui des médicaments ciblés modernes qui ralentissent la croissance tumorale en bloquant le cycle cellulaire. Pourtant, presque inévitablement, les tumeurs apprennent à contourner ces traitements et recommencent à croître. Cette étude pose une question cruciale : lorsque les cancers du sein ER+ deviennent résistants à deux grandes classes de médicaments — les inhibiteurs de FOXM1 et les inhibiteurs de CDK4/6 — quels changements à l’intérieur des cellules cancéreuses leur permettent d’échapper au traitement, et ces mêmes changements peuvent-ils révéler de nouvelles façons de les arrêter ?
Un câblage de survie commun dans les tumeurs résistantes
Les chercheurs se sont concentrés sur des cellules de cancer du sein ER+ cultivées en laboratoire jusqu’à ce qu’elles ne répondent plus ni aux médicaments bloquant FOXM1 ni aux inhibiteurs de CDK4/6 tels que le palbociclib et l’abémaciclib. Ils ont découvert que, malgré la résistance à des médicaments différents, ces cellules activaient un système d’alarme interne similaire centré sur les signaux d’interféron et une protéine nommée STAT1. Cette alarme entraîne la production de nombreux « gènes stimulés par l’interféron » et d’une petite protéine appelée ISG15, qui peut être attachée à d’autres protéines comme une étiquette moléculaire. Les cellules résistantes présentaient des niveaux bien plus élevés de STAT1, de STAT1 activé, d’ISG15 libre et de protéines marquées par ISG15 que leurs homologues non résistantes, ce qui suggère que ce réseau constitue une ossature commune de la résistance aux médicaments.
Un manteau protecteur de petites étiquettes moléculaires
En examinant de plus près, l’équipe a observé que les cellules résistantes non seulement produisaient plus d’ISG15, mais augmentaient aussi les enzymes qui fixent ISG15 sur d’autres protéines, un processus connu sous le nom d’ISGylation. Ces enzymes — HERC5, HERC6 et UBE2L6 — étaient fortement élevées, en particulier dans les cellules résistantes aux inhibiteurs de FOXM1. De nombreuses protéines cellulaires, y compris STAT1 lui-même, portaient des étiquettes ISG15 dans les cellules résistantes, souvent à des niveaux supérieurs à ceux des cellules sensibles d’origine. Parce que l’ajout de ces étiquettes peut modifier la durée de vie et le comportement des protéines, l’accumulation de protéines ISGylées semble faire partie des mécanismes par lesquels les cellules cancéreuses se renforcent contre le traitement.
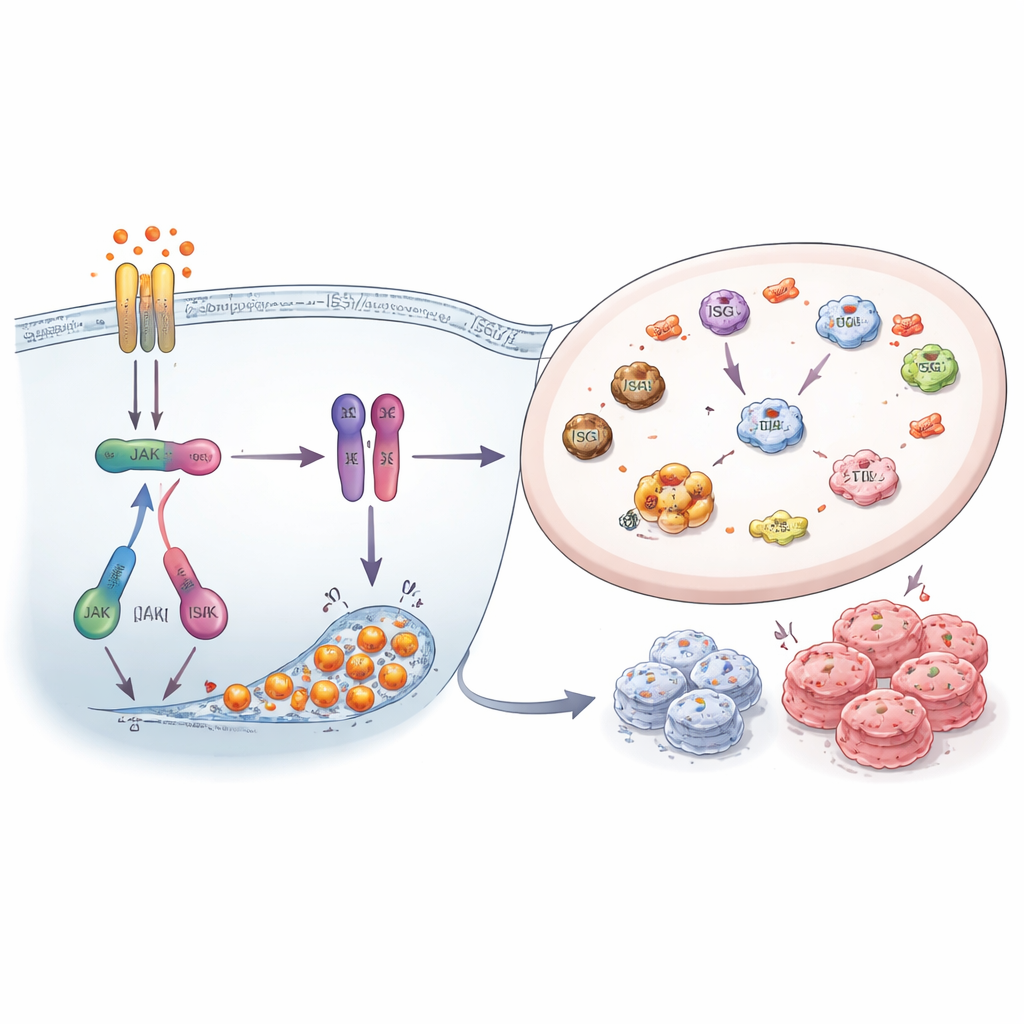
Éteindre l’alarme affaiblit les cellules résistantes
Les enquêteurs ont ensuite demandé si réduire l’activité de ce réseau d’alarme rendrait les cellules résistantes plus vulnérables. Ils ont utilisé des médicaments qui bloquent les kinases JAK — des commutateurs clés en amont de STAT1 — et des petits ARN interférents pour diminuer ISG15, HERC5 et HERC6. Le blocage de la signalisation JAK1/2 a sensiblement réduit l’activité de STAT1, diminué les niveaux d’ISG15 et l’ISGylation, et réduit la taille des colonies formées par les cellules résistantes, en particulier celles résistantes aux inhibiteurs de FOXM1. De même, la suppression directe d’ISG15 et de ses enzymes de marquage a diminué le profil global d’ISGylation et compromis la survie cellulaire. Ces expériences montrent que le système interféron–STAT1–ISG15 n’est pas un simple spectateur, mais soutient activement la croissance et la persistance des cellules cancéreuses résistantes aux médicaments.
Un nouvel espoir dans les stratégies de traitement séquentiel
Une des découvertes les plus encourageantes est que les cellules résistantes n’étaient pas coincées dans un état invincible unique. Les cellules de cancer du sein devenues résistantes aux inhibiteurs de CDK4/6 répondaient encore aux inhibiteurs de FOXM1, et les cellules résistantes aux inhibiteurs de FOXM1 pouvaient encore être ralenties par le palbociclib ou l’abémaciclib. Tant en cultures bidimensionnelles qu’en cultures tridimensionnelles sur Matrigel — qui reproduisent mieux les tumeurs — le changement de classe thérapeutique réduisait fortement la croissance cellulaire et abaissait l’expression des gènes qui pilotent la réplication de l’ADN et la division cellulaire. Parallèlement, les données de patients montraient que des niveaux élevés d’ISG15 et de ses enzymes associées dans les tumeurs ER+/HER2− étaient liés à une survie plus mauvaise, soulignant la pertinence clinique de ce câblage de résistance.
Ce que cela signifie pour les patientes et les thérapies futures
Pour un lecteur non spécialiste, le tableau qui se dégage est que les cancers du sein ER+ résistants se recâblent autour d’un circuit de réponse au stress partagé, utilisant les signaux d’interféron et les étiquettes ISG15 comme une sorte d’armure protectrice. La bonne nouvelle est que cette armure révèle de nouvelles faiblesses. Les médicaments qui bloquent la voie JAK–STAT1–ISG15, et des stratégies de traitement qui enchaînent les inhibiteurs de FOXM1 après les inhibiteurs de CDK4/6 (ou inversement), pourraient permettre de contourner la résistance plutôt que d’en être vaincus. Bien que ces conclusions doivent encore être évaluées dans des essais cliniques, elles offrent une feuille de route plus claire pour transformer une impasse thérapeutique trop fréquente en une nouvelle opportunité de contrôle.
Citation: Ziegler, Y., Kumar, S., Saeh, C.M. et al. JAK/STAT1-interferon-ISGylation networks in breast cancer resistance to inhibitors of FOXM1 and CDK4/6. npj Breast Cancer 12, 44 (2026). https://doi.org/10.1038/s41523-026-00911-6
Mots-clés: cancer du sein ER positif, résistance aux médicaments, inhibiteurs de CDK4/6, inhibiteurs de FOXM1, signalisation par les interférons