Clear Sky Science · fr
Expression des gènes cibles du récepteur aux œstrogènes β révèle de nouvelles fonctions répressives dans le cancer du sein agressif
Pourquoi cette recherche est importante
Le cancer inflammatoire du sein est l’une des formes les plus agressives et mortelles du cancer du sein, se propageant souvent rapidement et laissant peu d’options thérapeutiques ciblées aux patientes. Cette étude explore un capteur hormonal moins connu dans les cellules mammaires, appelé récepteur aux œstrogènes bêta, et montre comment il peut agir comme un frein naturel à la dissémination tumorale. Comprendre le fonctionnement de ce frein interne pourrait ouvrir la voie à de nouveaux traitements qui ralentissent ou préviennent les métastases chez des patientes ayant aujourd’hui de très peu d’alternatives.
Un autre visage du cancer inflammatoire du sein
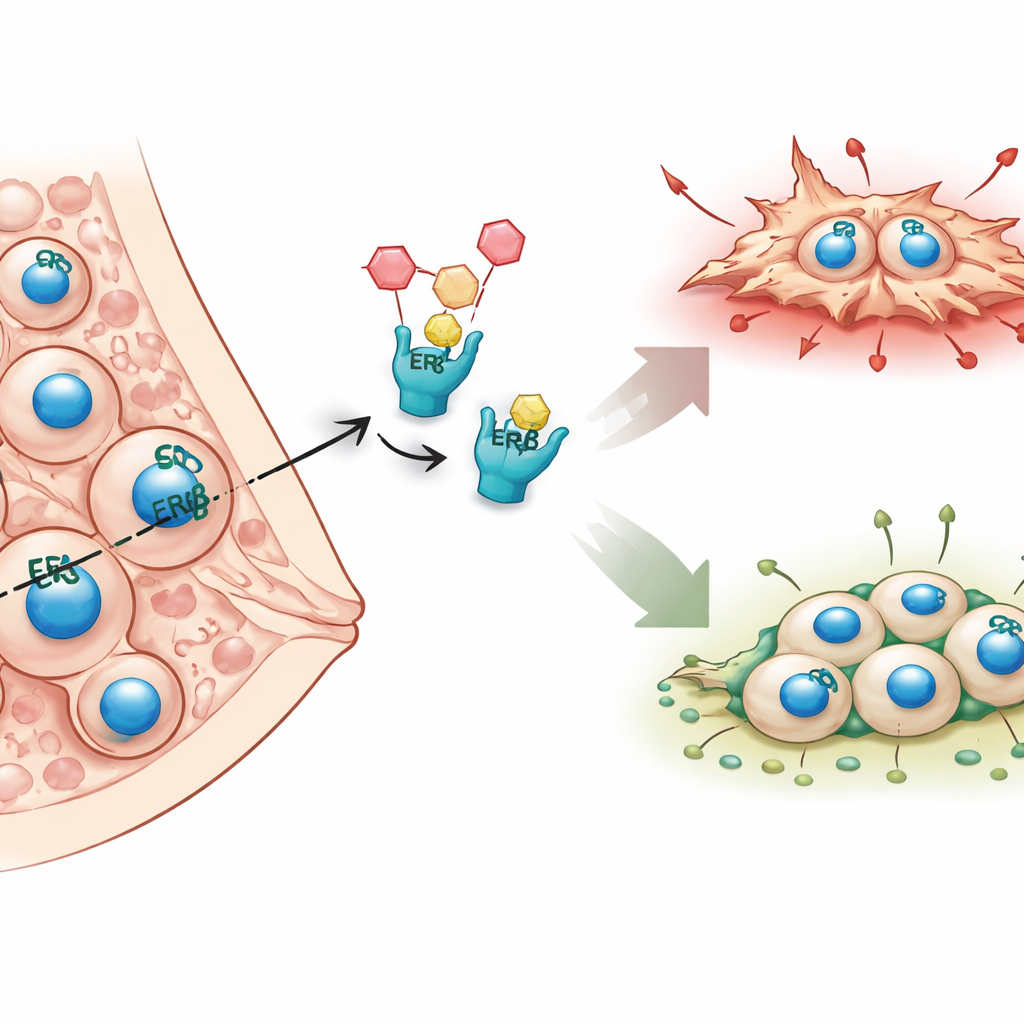
Contrairement à de nombreux cancers du sein qui dépendent du récepteur aux œstrogènes alpha classique, le cancer inflammatoire du sein est généralement dépourvu de cette molécule et ne répond donc pas bien aux thérapies hormonales standards. Les auteurs se concentrent plutôt sur un second récepteur aux œstrogènes, le récepteur β (ERβ), qu’ils avaient précédemment associé à moins de métastases chez des patientes et dans des modèles murins. Des travaux antérieurs suggéraient qu’ERβ ralentit la machinerie interne de la cellule liée au cytosquelette et à la mobilité. Dans cette étude, l’équipe a cherché à cartographier, à l’échelle du génome, comment ERβ modifie l’activité des gènes et quels effecteurs en aval pourraient expliquer son rôle protecteur anti-métastatique.
Lire le manuel d’instructions de la cellule cancéreuse
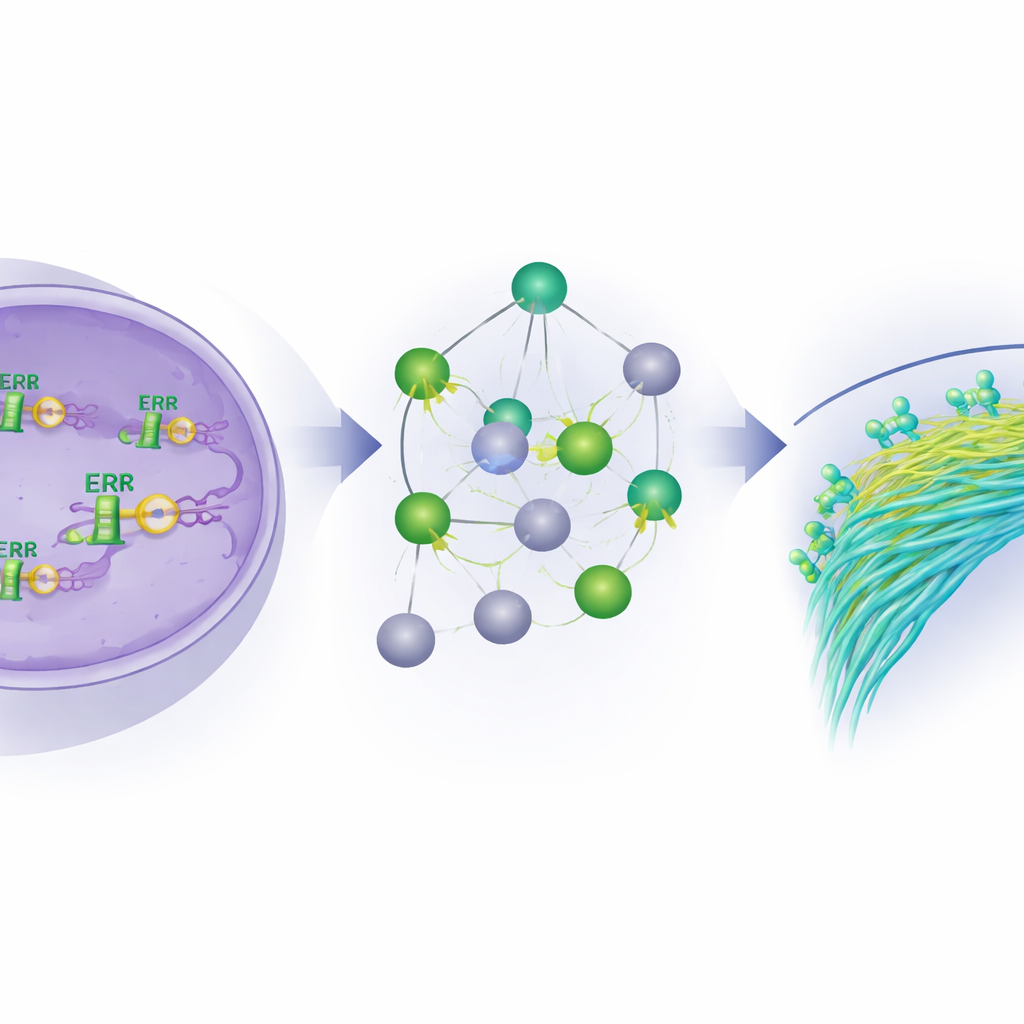
Pour dévoiler l’influence d’ERβ, les chercheurs ont utilisé deux approches de séquençage puissantes sur des lignées cellulaires de cancer inflammatoire du sein. Une méthode, le ChIP-seq, localise précisément où ERβ se fixe sur l’ADN, comme en marquant des pages et des lignes spécifiques dans le manuel d’instructions cellulaire. L’autre méthode, le RNA-seq, mesure quels gènes sont activés ou réprimés quand ERβ est présent, absent ou activé par un médicament sélectif. En comparant ces jeux de données, ils ont trouvé des milliers de sites d’ADN liés à ERβ, la plupart non seulement aux interrupteurs d’expression des gènes mais profondément à l’intérieur ou entre les gènes, suggérant un contrôle étendu. Ils ont également découvert qu’ERβ travaille souvent de concert avec des familles d’autres facteurs de transcription, formant des complexes qui décident collectivement quels gènes sont silencés ou activés.
Reprogrammation de la croissance, du mouvement et du métabolisme
L’analyse intégrée a montré qu’ERβ tend à atténuer les gènes qui favorisent la mobilité cellulaire, le changement de forme et l’invasion, en particulier ceux associés au cytosquelette d’actine et à la signalisation des GTPases Rho — des voies connues pour promouvoir les métastases. Parallèlement, ERβ soutient des programmes génétiques liés au développement tissulaire et à la différenciation cellulaire, poussant les cellules cancéreuses vers un état plus stable et moins agressif. L’étude a également révélé un rôle surprenant d’ERβ dans l’ajustement des voies métaboliques, en particulier celles impliquant les acides gras et les phospholipides, qui constituent carburant et éléments de construction pour les tumeurs à croissance rapide. Fait important, ces effets ont été observés non seulement dans des cellules surproduisant ERβ mais aussi dans des cellules exprimant des niveaux naturels du récepteur, ce qui souligne la pertinence en conditions réelles.
Petits messagers ARN et impact clinique
Au-delà des gènes codant des protéines, l’équipe a examiné les microARN — de petites molécules d’ARN qui ajustent finement l’expression génique. Ils ont identifié des dizaines de microARN dont les niveaux changeaient quand ERβ était supprimé ou restauré, dont beaucoup ont été liés à la suppression tumorale dans le cancer du sein. En reliant ces microARN à leurs gènes cibles, les auteurs ont montré qu’ERβ contrôle indirectement certains effecteurs du cancer, via un réseau régulateur à plusieurs niveaux. Ils se sont ensuite tournés vers des données patientes, en analysant des tumeurs d’individus atteints de cancer inflammatoire et non inflammatoire du sein. Plusieurs gènes contrôlés par ERβ étaient fortement corrélés à la survie des patientes : des niveaux élevés de certains (comme SERPINA1 et HSPB8) prédisaient de meilleurs résultats, tandis que des niveaux élevés d’autres (comme PITX1 et HOMER3) étaient associés à une survie plus mauvaise. Cela positionne ces molécules en aval comme des marqueurs potentiels de pronostic et comme futures cibles thérapeutiques.
Du frein moléculaire aux thérapies futures
Au total, l’étude présente ERβ comme un frein central du comportement invasif des cellules du cancer inflammatoire du sein. En se liant à l’ADN, en s’associant à d’autres régulateurs et en modulant à la fois les réseaux de gènes et de microARN, ERβ étouffe les programmes qui stimulent la migration cellulaire et les métastases tout en favorisant des états plus différenciés et stables et en réorientant le métabolisme tumoral. Pour les patientes, cela suggère que des médicaments activant ERβ ou inhibant ses cibles clés en aval — en particulier celles impliquées dans la mobilité cellulaire et l’utilisation des acides gras — pourraient constituer la base de traitements nouveaux et plus ciblés pour cette maladie difficile à traiter.
Citation: Tastsoglou, S., Karagounis, I.V., Miliotis, M. et al. Estrogen receptor β target gene expression reveals novel repressive functions in aggressive breast cancer. npj Breast Cancer 12, 38 (2026). https://doi.org/10.1038/s41523-026-00905-4
Mots-clés: cancer inflammatoire du sein, récepteur aux œstrogènes bêta, métastase, régulation des gènes, métabolisme du cancer