Clear Sky Science · fr
L’axe CXCL10/CXCR3 est essentiel pour maintenir la dormance immunologique dans le cancer du sein triple négatif
Pourquoi certains cancers dorment plutôt que de se propager
Le cancer du sein peut parfois se comporter comme un agent dormant. Après le traitement initial, quelques cellules tumorales peuvent se cacher dans l’organisme pendant des années, sans croître suffisamment pour être détectées sur les examens—mais restant capables de se réveiller plus tard et de provoquer des métastases menaçant la vie. Cet article explore pourquoi cet état de « sommeil », appelé dormance, survient dans une forme particulièrement agressive de la maladie, le cancer du sein triple négatif, et révèle un signal chimique qui aide le système immunitaire à maintenir ces cellules sous contrôle.
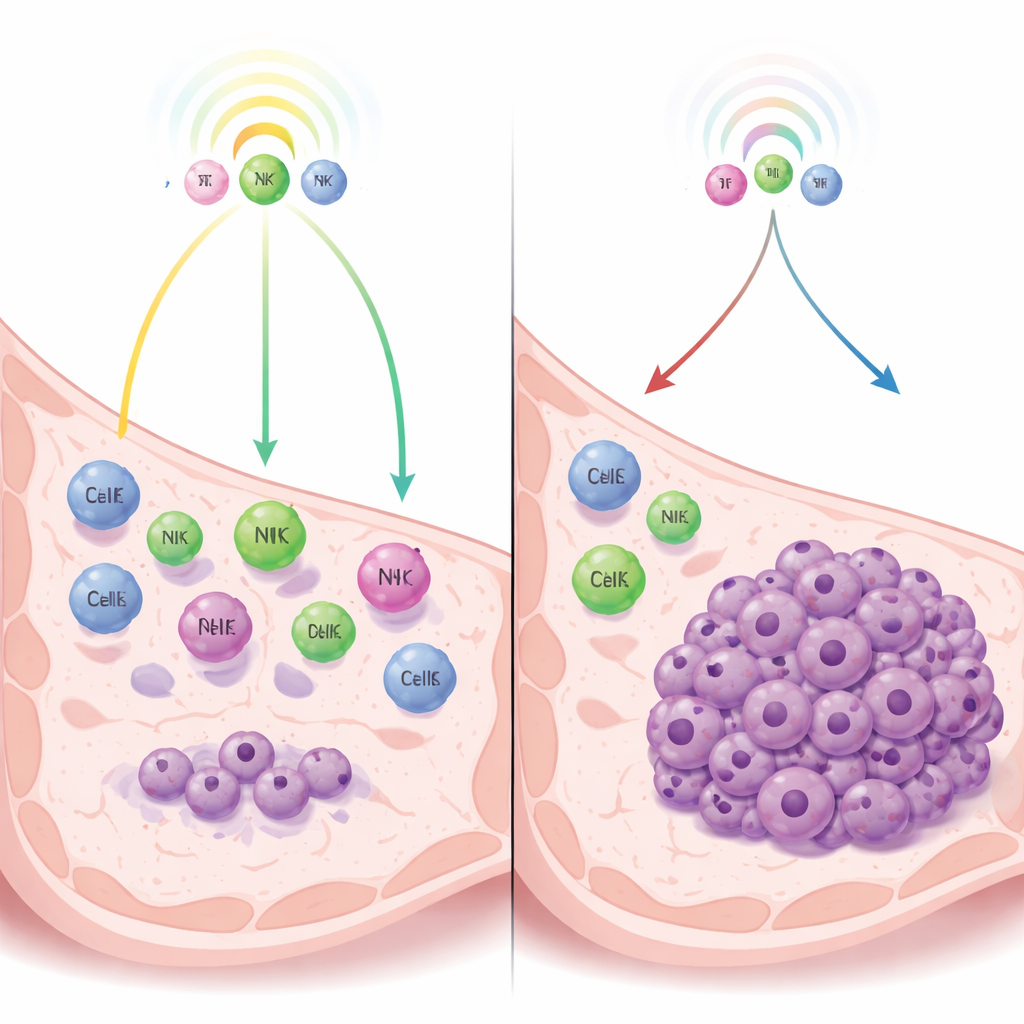
Une lutte de forces entre le cancer et le système immunitaire
Les auteurs s’intéressent à une forme de dormance contrôlée non pas par un manque d’apport sanguin ou des freins cellulaires internes, mais par la surveillance immunitaire—la vigilance constante des cellules immunitaires qui peuvent contenir les tumeurs sans pour autant les éliminer. À l’aide de modèles murins de cancer du sein triple négatif, ils comparent des cellules tumorales qui restent naturellement en dormance avec des cellules étroitement apparentées qui forment des tumeurs à croissance rapide. En examinant quels gènes sont activés, ils constatent que les cellules dormantes activent fortement les voies de l’interféron—des systèmes d’alerte immunitaire qui stimulent la libération de messagers chimiques attirant des cellules immunitaires dans la zone tumorale.
Un messager chimique clé qui maintient les tumeurs silencieuses
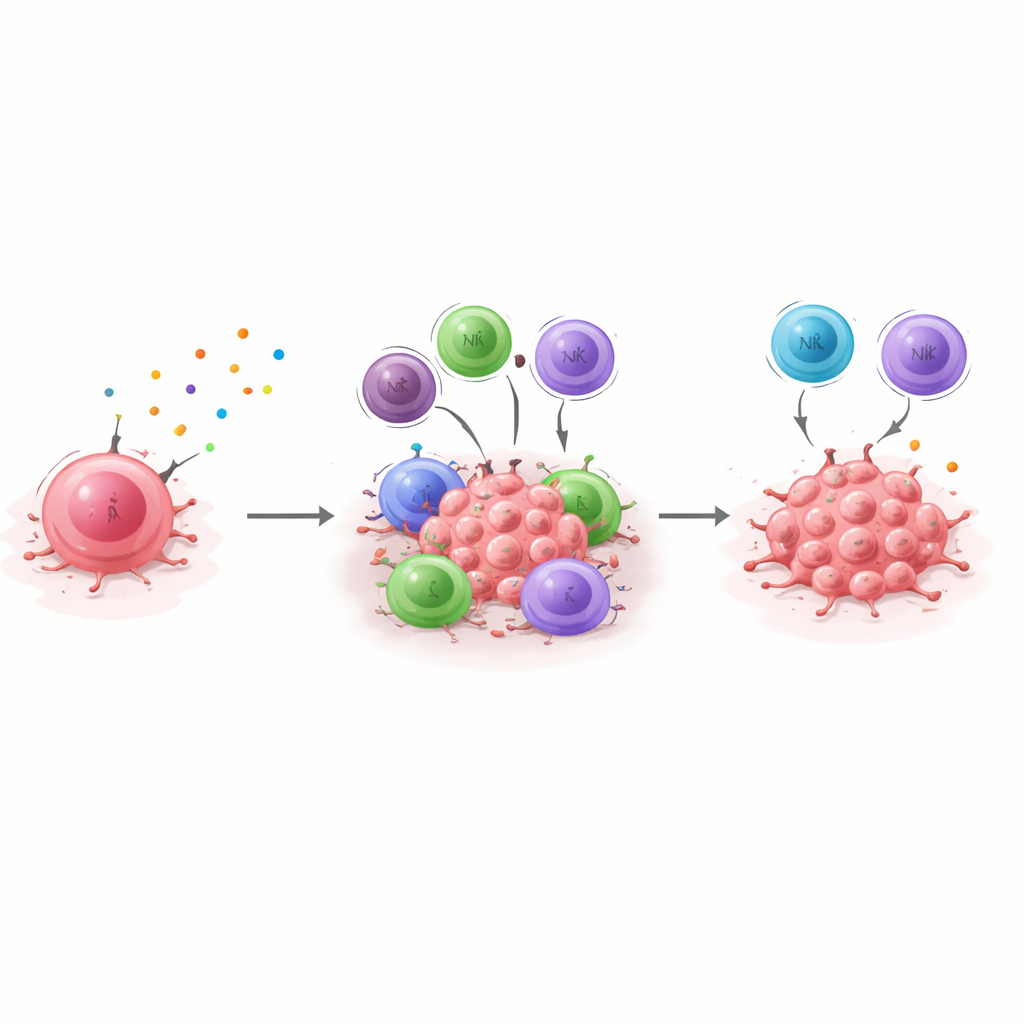
Parmi les nombreuses molécules exprimées dans les cellules dormantes, une ressort : CXCL10, une petite protéine qui agit comme un signal pour les cellules immunitaires portant son récepteur partenaire, CXCR3. Les cellules cancéreuses dormantes produisent beaucoup plus de CXCL10 que leurs homologues agressives. Lorsque les chercheurs suppriment volontairement CXCL10 dans des cellules dormantes et les implantent chez des souris dotées d’un système immunitaire intact, les cellules autrefois silencieuses forment rapidement des tumeurs. Le blocage du récepteur CXCR3 par un anticorps a un effet similaire. Dans les deux cas, les cellules cancéreuses échappent à l’impasse immunitaire et commencent à croître, montrant que l’axe CXCL10/CXCR3 n’est pas seulement corrélé à la dormance—il est nécessaire pour la maintenir.
Comment la modification du voisinage local change l’équilibre
La réduction de CXCL10 ne modifie pas seulement une voie unique ; elle remodèle l’ensemble du paysage immunitaire local. Dans les tumeurs ayant perdu CXCL10, les cellules T CD4 et CD8 bénéfiques sont réduites, tandis que certains myéloïdes susceptibles de supprimer les réponses immunitaires deviennent plus abondants. Les cellules tueuses naturelles (NK) et les cellules dendritiques évoluent également en nombre. Ce schéma apparaît tant dans les tumeurs primaires que dans les poumons, où les cellules cancéreuses peuvent migrer et rester en veille. Même lorsque les métastases pulmonaires sont trop petites pour être visibles au microscope, des marqueurs moléculaires révèlent que davantage de cellules cancéreuses réussissent à coloniser les poumons en l’absence de CXCL10, et que moins de cellules T infiltrent ces tissus. Cependant, chez des souris dépourvues de système immunitaire fonctionnel, la suppression de CXCL10 ne change rien—les cellules dormantes prolifèrent de toute façon—soulignant que ce signal agit via le contrôle immunitaire plutôt que comme frein direct de la croissance des cellules cancéreuses.
Pourquoi plus de signal est utile mais pas un interrupteur magique
L’équipe teste aussi l’inverse : augmenter CXCL10 peut‑il transformer une tumeur agressive en tumeur dormante ? Lorsqu’ils conçoivent des cellules cancéreuses à croissance rapide pour produire davantage de CXCL10, les tumeurs croissent plus lentement et mettent plus de temps à apparaître, et certains types de cellules immunitaires dans le sang augmentent. Cependant, une dormance complète ne se met pas en place ; à terme, toutes les souris développent quand même des tumeurs. Cela suggère que si CXCL10 est essentiel pour maintenir la dormance quand le reste de la machinerie immunitaire est en place, il ne suffit pas à lui seul à créer cet état complexe à partir de zéro. D’autres voies doivent coopérer pour établir un équilibre durable entre l’attaque immunitaire et la survie des cellules cancéreuses.
Des expériences chez la souris au pronostic des patientes
Pour relier leurs résultats à la maladie humaine, les chercheurs établissent une « signature de dormance »—un ensemble de gènes systématiquement plus élevés dans les cellules dormantes et diminuant lorsque CXCL10 est éteint. Ils examinent ensuite de larges bases de données de patientes atteintes de cancer du sein pour voir comment cette signature se rapporte à la survie. Dans le cancer du sein triple négatif, les patientes dont les tumeurs expriment cette signature de dormance à des niveaux plus élevés vivent globalement plus longtemps et tendent à rester en rémission plus d’années, cohérent avec un état de dormance contrôlé par le système immunitaire retardant les récidives. L’effet n’est pas observé de la même manière dans les tumeurs hormonodépendantes, mettant en lumière les différences biologiques entre sous‑types du cancer du sein. Ensemble, les résultats suggèrent que l’axe CXCL10/CXCR3 est un pilier central de la dormance médiée par l’immunité dans le cancer du sein triple négatif, et que mesurer cette signature de dormance pourrait aider à identifier les patientes susceptibles de bénéficier de thérapies renforçant le contrôle immunitaire—ou, à l’inverse, celles qui pourraient nécessiter une surveillance à long terme plus étroite parce que leur cancer est moins bien contenu.
Citation: Yilmaz, A., Haerri, L., Granda, M.E. et al. The CXCL10/CXCR3 axis is essential for sustaining immunological dormancy in triple-negative breast cancer. npj Breast Cancer 12, 36 (2026). https://doi.org/10.1038/s41523-026-00903-6
Mots-clés: cancer du sein triple négatif, dormance tumorale, surveillance immunitaire, signalisation des chimiokines, axe CXCL10 CXCR3