Clear Sky Science · fr
L’analyse spatiale de l’expression génique révèle les moteurs des métastases ganglionnaires extrêmement précoces dans le cancer du sein
Pourquoi ces minuscules cellules voyageuses comptent
Lorsque le cancer du sein se propage au-delà du sein, il s’arrête souvent d’abord dans les ganglions lymphatiques proches — de petits filtres qui aident à combattre les infections. Les médecins savent que la présence de cellules cancéreuses dans ces ganglions signale généralement un risque accru de récidive. Mais ce qui se passe précisément dans les tout premiers instants, lorsque seulement quelques cellules arrivent dans un ganglion, a été presque impossible à observer chez de vrais patients. Cette étude a utilisé un nouveau type de « carte » microscopique de l’activité génique pour observer ces étapes initiales avec un niveau de détail sans précédent, révélant quelles cellules réussissent, quelles cellules échouent, et pourquoi cela importe pour le pronostic des patients.
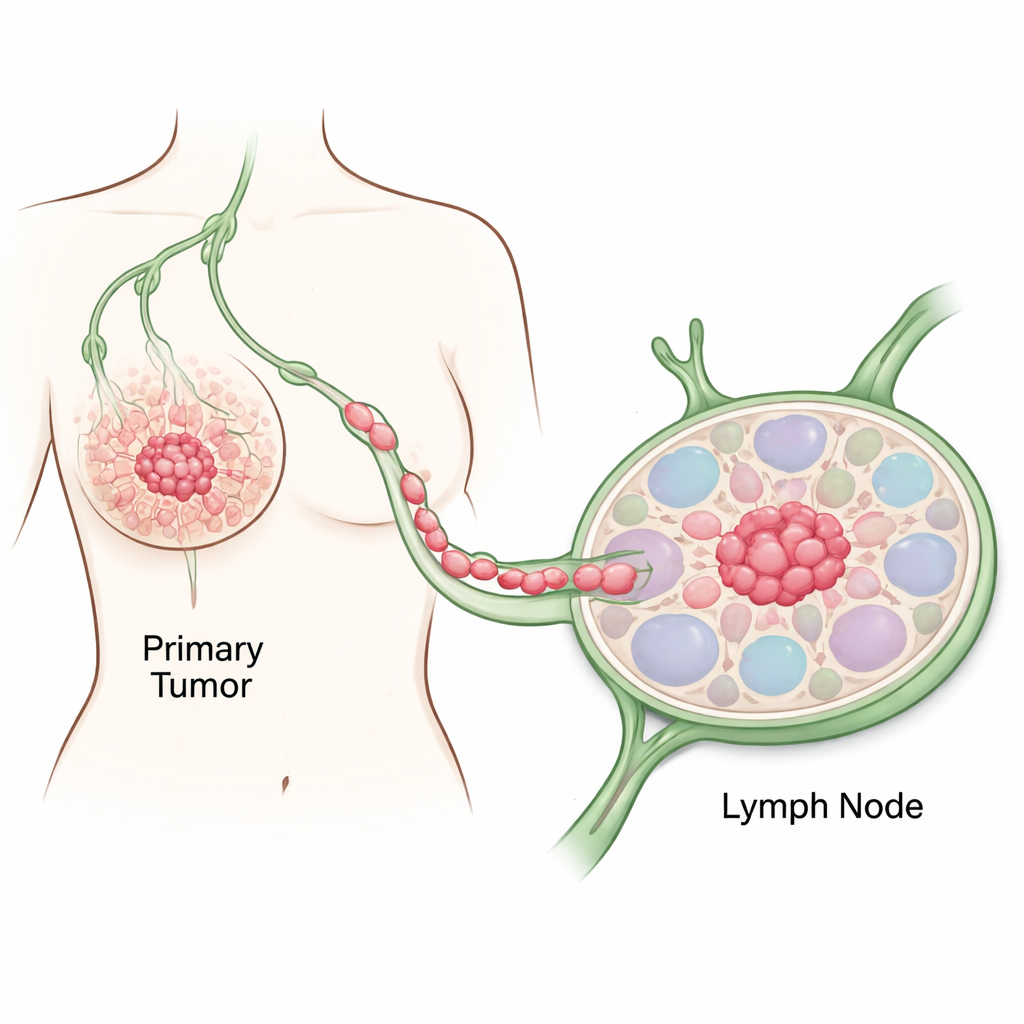
Suivre les premiers pas du cancer
Les chercheurs se sont concentrés sur des tissus prélevés chez une femme de 80 ans atteinte d’un cancer du sein agressif, de type HER2‑positif. Ils ont échantillonné des zones mammaires à l’apparence normale et des régions tumorales voisines, puis ont utilisé plusieurs tests d’ADN et d’ARN pour retracer comment des cellules ordinaires sont devenues cancéreuses. Par rapport au tissu sain, les régions tumorales présentaient des caractéristiques classiques du cancer : adhérence cellulaire perturbée, division cellulaire hyperactive, modifications à grande échelle de la méthylation de l’ADN et mutations clés dans des gènes contrôlant la croissance et la stabilité du génome. Ces changements moléculaires correspondaient à ce que voyaient les pathologistes au microscope, confirmant une progression en étapes des cellules mammaires normales vers des cellules pleinement malignes.
Des cellules qui changent de forme en mouvement
Pour comprendre comment les cellules tumorales commencent à voyager, l’équipe a utilisé une technique à haute résolution qui lit l’activité génique au niveau des cellules individuelles tout en conservant leur position exacte dans le tissu. Cela leur a permis de reconstruire comment les cellules cancéreuses changeaient d’identité en quittant les structures mammaires normales et en se dirigeant vers la métastase. Ils ont constaté que le cancer semblait provenir d’un type particulier de cellule mammaire mature, qui a ensuite adopté progressivement des caractéristiques d’un processus appelé transition épithélio‑mésenchymateuse — une sorte de métamorphose qui aide les cellules à se détacher, se déplacer et envahir les tissus voisins. Plutôt qu’un simple interrupteur marche/arrêt, les cellules occupaient un spectre d’états mixtes, mêlant traits « épithéliaux » (ordonnés, solidement associés) et traits « mésenchymateux » (mobiles, invasifs). Certaines de ces cellules hybrides se dispersaient à travers la tumeur, tandis que d’autres se regroupaient en populations tumorales plus avancées prêtes à se propager vers les ganglions lymphatiques.
Le premier avant‑poste dans un ganglion lymphatique
Dans un ganglion lymphatique jugé indemne de métastase par les tests cliniques standard, les scientifiques ont repéré quelque chose de remarquable : seulement 30 cellules tumorales isolées, occupant une région d’environ 200 micromètres de large — à peu près le double du diamètre d’un cheveu humain. Ces cellules tumorales isolées provenaient de plusieurs états hybrides distincts, chacun avec son propre profil d’activité génique. En regroupant les cellules cancéreuses apparentées, l’équipe a défini six sous‑types aux rôles différents. Un sous‑type, fortement « mésenchymateux », semblait particulièrement apte à résister à la mort cellulaire et à échapper à l’attaque immunitaire. Un autre sous‑type, qui retrouvait davantage de caractéristiques épithéliales, montrait un changement frappant dans son utilisation de l’énergie, favorisant le métabolisme des acides gras. Seul ce groupe métaboliquement réorienté et davantage de type épithélial a réussi à former de petites colonies dans les ganglions lymphatiques, suggérant que le choix du carburant — et pas seulement l’invasivité — aide à déterminer si les premières cellules arrivées peuvent s’implanter.
Un ganglion qui aide discrètement le cancer
L’étude a également examiné comment l’environnement du ganglion lymphatique répondait à ces intrus. Même avant la formation d’une métastase visible, les cellules immunitaires, les cellules vasculaires et le tissu conjonctif envoyaient déjà des signaux qui atténuaient les réponses immunitaires et soutenaient la survie tumorale. Certaines paires récepteur‑ligand entre cellules immunitaires laissaient entrevoir une tolérance immunitaire précoce, tandis que d’autres encourageaient la néovascularisation et le remodelage de l’échafaudage tissulaire. Ensemble, ces changements ont construit une niche étonnamment accueillante pour les cellules cancéreuses adaptées métaboliquement, en les aidant à survivre, croître et potentiellement semer des foyers de dissémination futurs.
Ce que cela signifie pour les patients
En comparant leurs résultats avec de larges bases de données de patients existantes, les chercheurs ont fait une découverte contre‑intuitive. Les cellules les plus aptes à former précocement des colonies ganglionnaires, et même celles présentant les caractéristiques mésenchymateuses les plus marquées, n’étaient pas associées aux pires résultats cliniques. Au contraire, le pronostic était le plus défavorable lorsque les tumeurs contenaient certains types cellulaires hybrides agressifs marqués par une forte activité du cycle cellulaire et des programmes de glycolyse (consommation de sucre) pilotés par des gènes comme MYC. Autrement dit, différents états cellulaires métamorphosés semblent se spécialiser : certains excellent à coloniser discrètement de nouveaux sites, tandis que d’autres entraînent une croissance rapide et des récidives. Comprendre et cibler ces états cellulaires distincts et leurs préférences métaboliques pourrait conduire à des traitements plus précis — capables non seulement de détecter plus sûrement la dissémination précoce, mais aussi d’éliminer les types cellulaires tumoraux les plus susceptibles d’entraîner des rechutes mortelles.
Citation: Nagasawa, S., Kajiya, K., Ishikawa, E. et al. Spatial gene expression analysis reveals drivers of extremely early lymph node metastasis in breast cancer. npj Breast Cancer 12, 28 (2026). https://doi.org/10.1038/s41523-026-00897-1
Mots-clés: métastase du cancer du sein, ganglion lymphatique, transition épithélio-mésenchymateuse, transcriptomique spatiale, métabolisme du cancer