Clear Sky Science · fr
La signalisation CD52 via Siglec‑G des macrophages représente une cible thérapeutique pour l’immunothérapie du cancer
Pourquoi certains cancers du sein échappent au système immunitaire
Le cancer du sein triple négatif est l’une des formes les plus dangereuses de cancer du sein parce qu’il se propage rapidement et qu’il manque de nombreuses cibles thérapeutiques courantes. Cette étude explore une voie récemment découverte que ces tumeurs peuvent utiliser pour se cacher des défenses de l’organisme et montre comment bloquer cet itinéraire d’évasion pourrait améliorer l’efficacité des thérapies à base d’immunité.
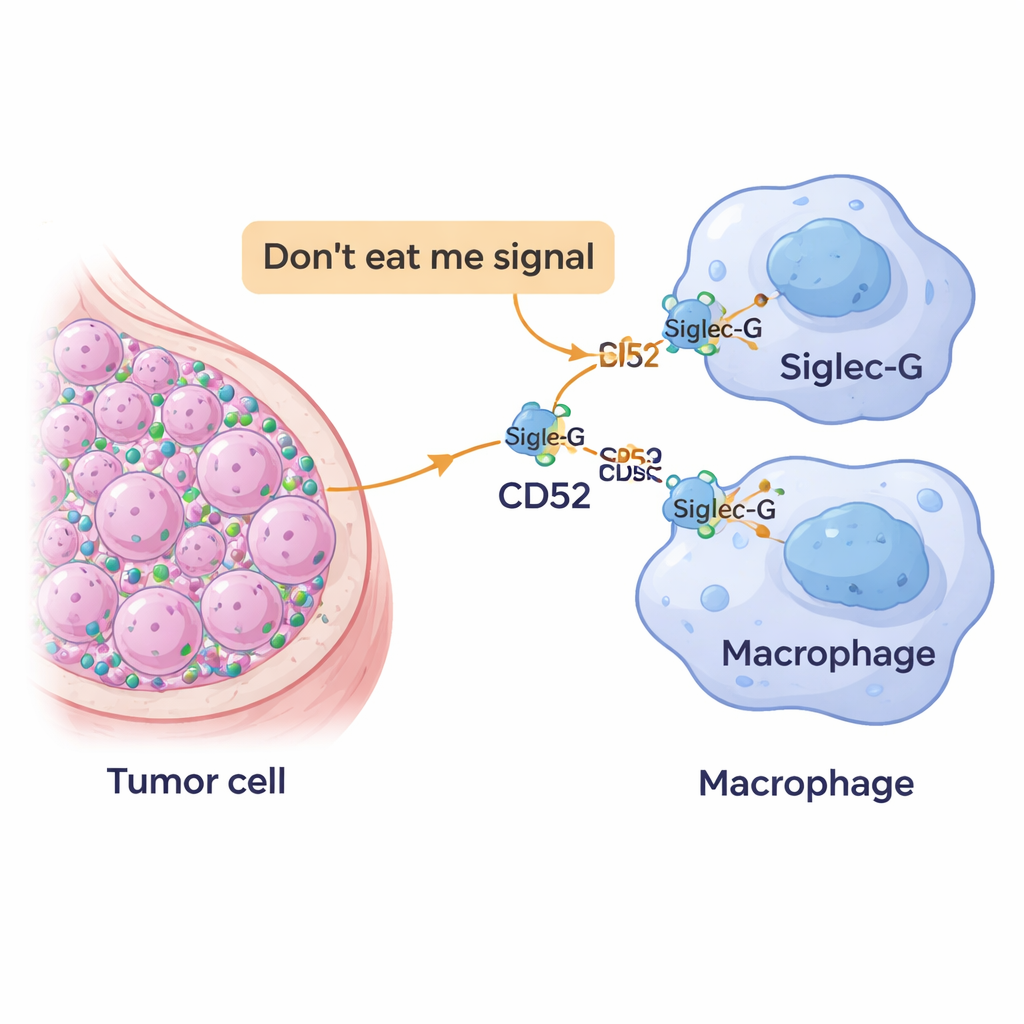
Un nouveau drapeau « ne me mangez pas » sur les cellules cancéreuses
Notre système immunitaire s’appuie sur des cellules « nettoyeuses » appelées macrophages pour patrouiller les tissus et engloutir les cellules dangereuses ou anormales. Pour éviter d’être détruites par erreur, les cellules saines affichent à leur surface des marqueurs qui signifient, en substance, « j’ai ma place ici ». Les cellules cancéreuses détournent souvent ce mécanisme en surexprimant ces signaux protecteurs, les transformant en puissants drapeaux « ne me mangez pas ». Les chercheurs se sont intéressés à une molécule nommée CD52, déjà connue dans les hémopathies et les maladies auto‑immunes, et ont cherché à savoir si les cellules tumorales mammaires l’utilisent aussi pour échapper à l’attaque des macrophages.
Détecter CD52 dans les tumeurs mammaires agressives
L’équipe a analysé de larges bases de données publiques sur le cancer et des échantillons de tissus de patientes. Ils ont constaté que les tumeurs mammaires, en particulier les formes triple négatives, produisaient davantage de CD52 que le tissu mammaire normal. De plus, les tumeurs à forte expression de CD52 avaient tendance à être moins bien différenciées, un trait souvent associé à une maladie plus agressive. Parallèlement, les cellules immunitaires à l’intérieur et autour des tumeurs portaient des niveaux élevés d’une molécule partenaire appelée Siglec‑10 (et son homologue murin Siglec‑G), présente sur les macrophages et capable d’envoyer des signaux inhibiteurs à l’intérieur de ces cellules. Ensemble, ces observations suggéraient que le CD52 des cellules tumorales pourrait dialoguer directement avec Siglec‑G des macrophages pour les empêcher d’accomplir leur rôle.
Désactiver CD52 pour libérer les macrophages
Pour tester cette hypothèse, les scientifiques ont utilisé des outils d’édition génique pour supprimer CD52 dans des cellules de cancer du sein triple négatif murines. Lorsque ces cellules modifiées ont été mises en présence de macrophages en laboratoire, les macrophages ont phagocyté significativement plus de cellules tumorales que lorsqu’ils étaient confrontés à des cellules cancéreuses non modifiées. Il est important de noter que les cellules cancéreuses elles‑mêmes ne présentaient pas de différences de croissance ou de survie après la perte de CD52, ce qui indique que l’effet clé porte sur la reconnaissance immunitaire plutôt que sur la biologie intrinsèque des cellules tumorales. Lorsqu’on a implanté les mêmes cellules tumorales chez la souris, celles dépourvues de CD52 formaient des tumeurs plus petites et étaient entourées de macrophages montrant davantage de signes d’avoir ingéré des cellules cancéreuses. Si les macrophages étaient éliminés chez les souris, cet avantage de croissance disparaissait, confirmant que le rôle principal de CD52 était de protéger les tumeurs contre la phagocytose.
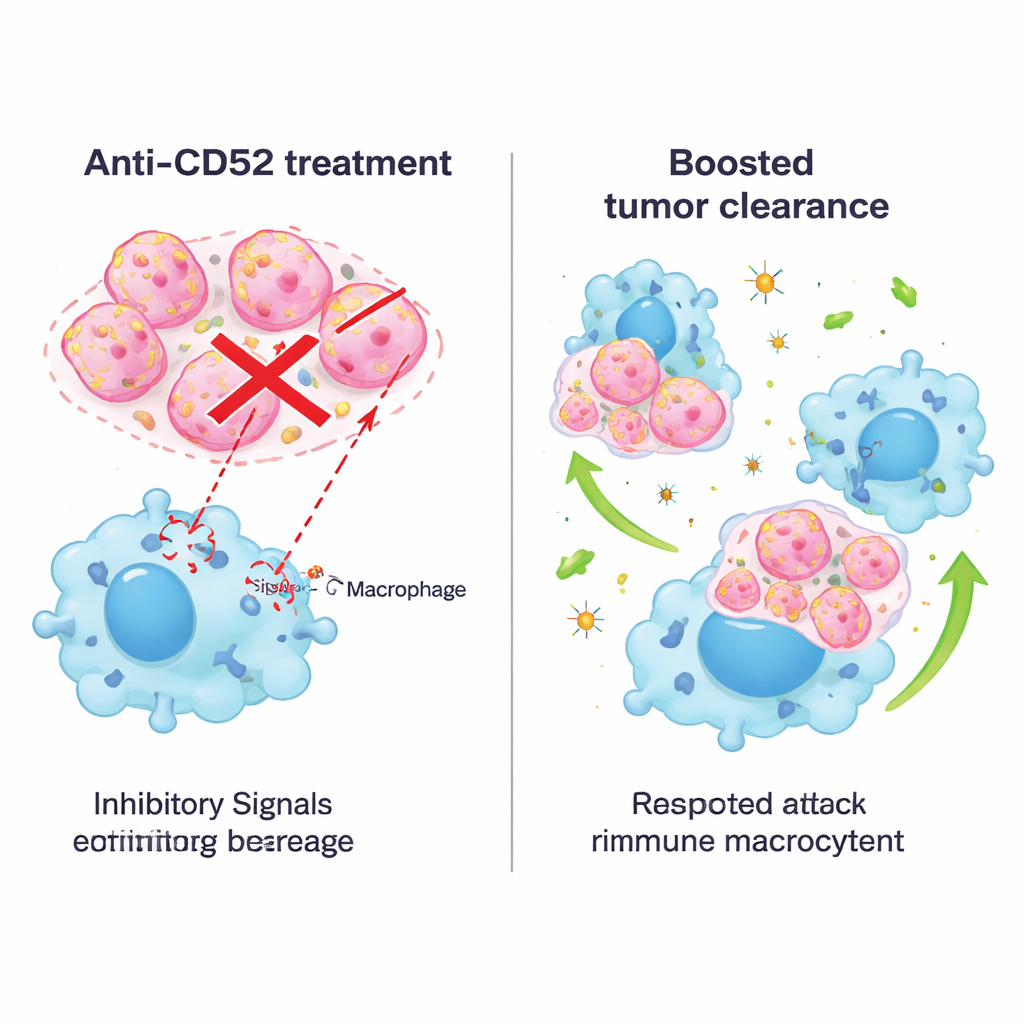
Bloquer le signal avec des anticorps et combiner les traitements
Étant donné que des médicaments ciblant CD52 sont déjà utilisés dans d’autres maladies, les chercheurs ont ensuite testé un anticorps bloqueur dans des modèles murins. Le traitement des souris porteuses de tumeurs par un anticorps anti‑CD52 a réduit la croissance tumorale, prolongé la survie et n’a pas provoqué de dommages organiques évidents ni de perte de poids. In vitro, des anticorps similaires ont renforcé la capacité des macrophages murins et humains à engloutir des cellules de cancer du sein de plusieurs sous‑types, pas seulement triple négatif. L’équipe a ensuite combiné le blocage de CD52 avec une thérapie anti‑PD‑1, un médicament de blocage des points de contrôle largement utilisé visant les lymphocytes T. Dans un modèle murin spontané de cancer du sein triple négatif, la combinaison a été plus efficace que chaque traitement pris isolément : les tumeurs ont davantage régressé, les macrophages sont devenus plus inflammatoires et actifs, et des lymphocytes T plus efficaces pour tuer les cellules cancéreuses ont infiltré la tumeur tandis que moins de lymphocytes T « épuisés » y restaient.
Ce que cela signifie pour la prise en charge future du cancer du sein
Ce travail met en évidence CD52 comme un signal « ne me mangez pas » jusque‑ici méconnu que les cellules du cancer du sein triple négatif utilisent pour se protéger des macrophages. En interrompant la communication entre le CD52 sur les cellules tumorales et Siglec‑G sur les macrophages, les chercheurs ont pu réveiller à la fois l’immunité innée et, indirectement, les lymphocytes T, surtout en association avec le blocage de PD‑1. Bien que des études de sécurité et des essais cliniques supplémentaires soient nécessaires — car CD52 est aussi présent sur de nombreuses cellules immunitaires normales — ces résultats pointent vers une stratégie prometteuse de double‑blocage des points de contrôle qui pourrait aider à transformer des tumeurs du sein résistantes à l’immunité en tumeurs plus réceptives à l’immunothérapie.
Citation: Qin, X., Chang, Y., Qiu, Y. et al. CD52 signaling via macrophage Siglec-G represents a therapeutic target for cancer immunotherapy. npj Breast Cancer 12, 29 (2026). https://doi.org/10.1038/s41523-026-00895-3
Mots-clés: cancer du sein triple négatif, macrophages, immunothérapie, CD52, blocage des points de contrôle