Clear Sky Science · fr
Co‑administration de la chimiokine CXCL9 et du ligand costimulatoire TNFSF9 par des cellules souches mésenchymateuses reprogramme le microenvironnement immunitaire du cancer du sein triple négatif
Pourquoi cette nouvelle approche contre le cancer du sein est importante
Le cancer du sein triple négatif est l’une des formes les plus dangereuses de cancer du sein car il croît rapidement, se propage tôt et ne présente pas les cibles hormonales courantes sur lesquelles reposent de nombreux traitements. L’immunothérapie a suscité de grands espoirs, mais chez de nombreux patients, les cellules protectrices de l’organisme n’infiltrent tout simplement pas suffisamment la tumeur pour être efficaces. Cette étude explore une stratégie inventive : utiliser des cellules porteuses vivantes comme des « camions de livraison » guidés qui apportent des signaux stimulant l’immunité directement dans des tumeurs difficiles à traiter, rendant potentiellement davantage de patients éligibles à des traitements immunitaires puissants.
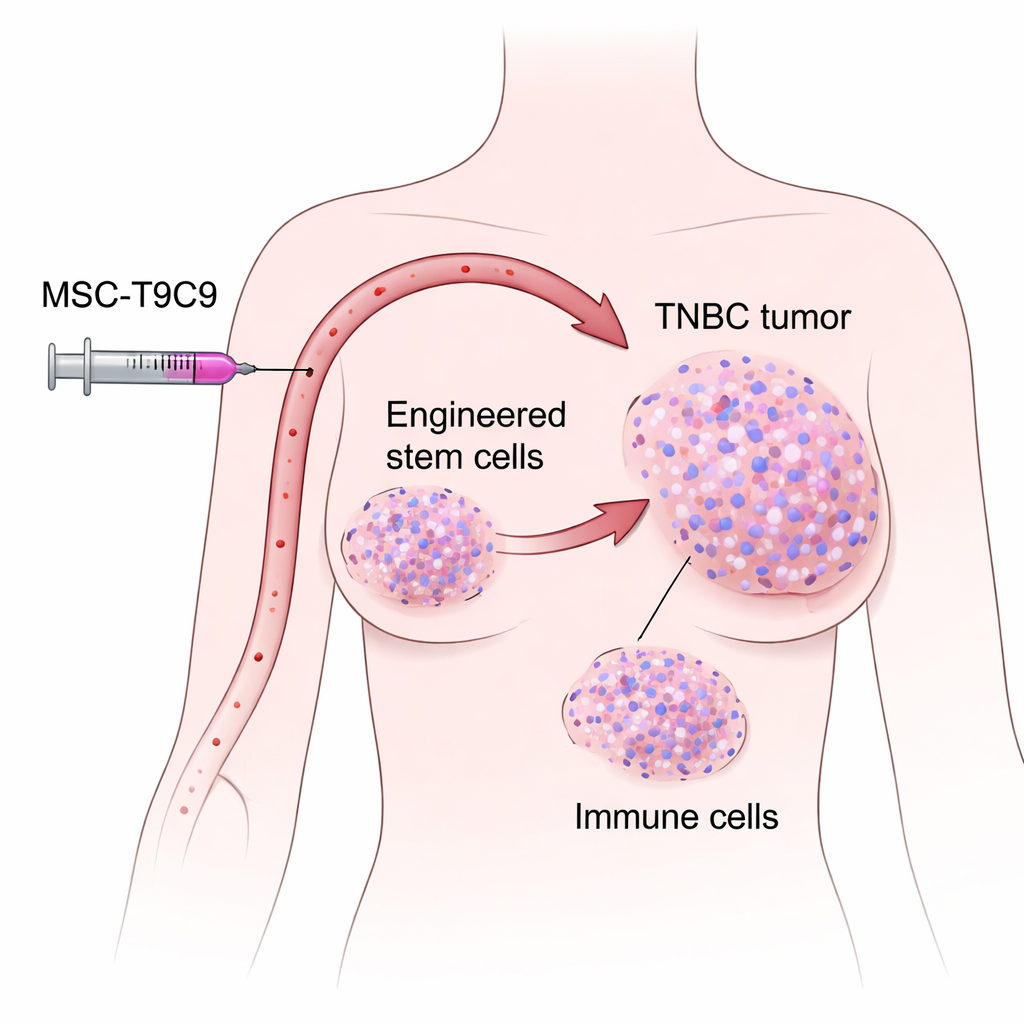
Un cancer difficile avec trop peu d’aide immunitaire
Les traitements standards du cancer du sein triple négatif — chirurgie, chimiothérapie et radiothérapie — ne préviennent souvent pas les rechutes, et la survie moyenne en cas de maladie avancée reste inférieure à deux ans. Une raison clé est que nombre de ces tumeurs sont « froides », c’est‑à‑dire qu’elles contiennent peu de cellules immunitaires combattant le cancer. De grandes bases de données de patients ont montré que les personnes dont les tumeurs produisent naturellement des quantités plus élevées de deux molécules liées à l’immunité, CXCL9 et TNFSF9, tendent à vivre plus longtemps et présentent davantage de lymphocytes T et de cellules NK dans leurs tumeurs. CXCL9 est un signal chimique qui attire les cellules immunitaires vers les tissus, tandis que TNFSF9 agit comme un interrupteur « go » supplémentaire qui aide ces cellules à attaquer plus fortement. Le schéma suggérait que l’augmentation de ces deux signaux directement dans les tumeurs pourrait faire pencher la balance en faveur du système immunitaire.
Transformer des cellules souches en « camions » de livraison intelligents
Les chercheurs se sont concentrés sur des cellules souches mésenchymateuses issues de cordons ombilicaux humains donnés. Ces cellules ont une propriété utile : lorsqu’elles sont injectées dans le sang de souris porteuses de tumeurs mammaires, elles migrent naturellement vers les sites tumoraux et y persistent pendant des jours, tout en évitant dans une large mesure les organes normaux. L’équipe a modifié génétiquement ces cellules souches pour qu’elles libèrent CXCL9 et exposent TNFSF9 à leur surface, créant une thérapie cellulaire à double fonction qu’ils nomment MSC‑T9C9. Des tests en laboratoire ont montré que les cellules modifiées sécrètent de fortes quantités de CXCL9 et activent puissamment les lymphocytes T et les cellules NK de souris, sans modifier leur propre comportement de croissance ni provoquer de tumeurs elles‑mêmes. Cela en faisait des candidats prometteurs comme stimulateurs immunitaires ciblés.
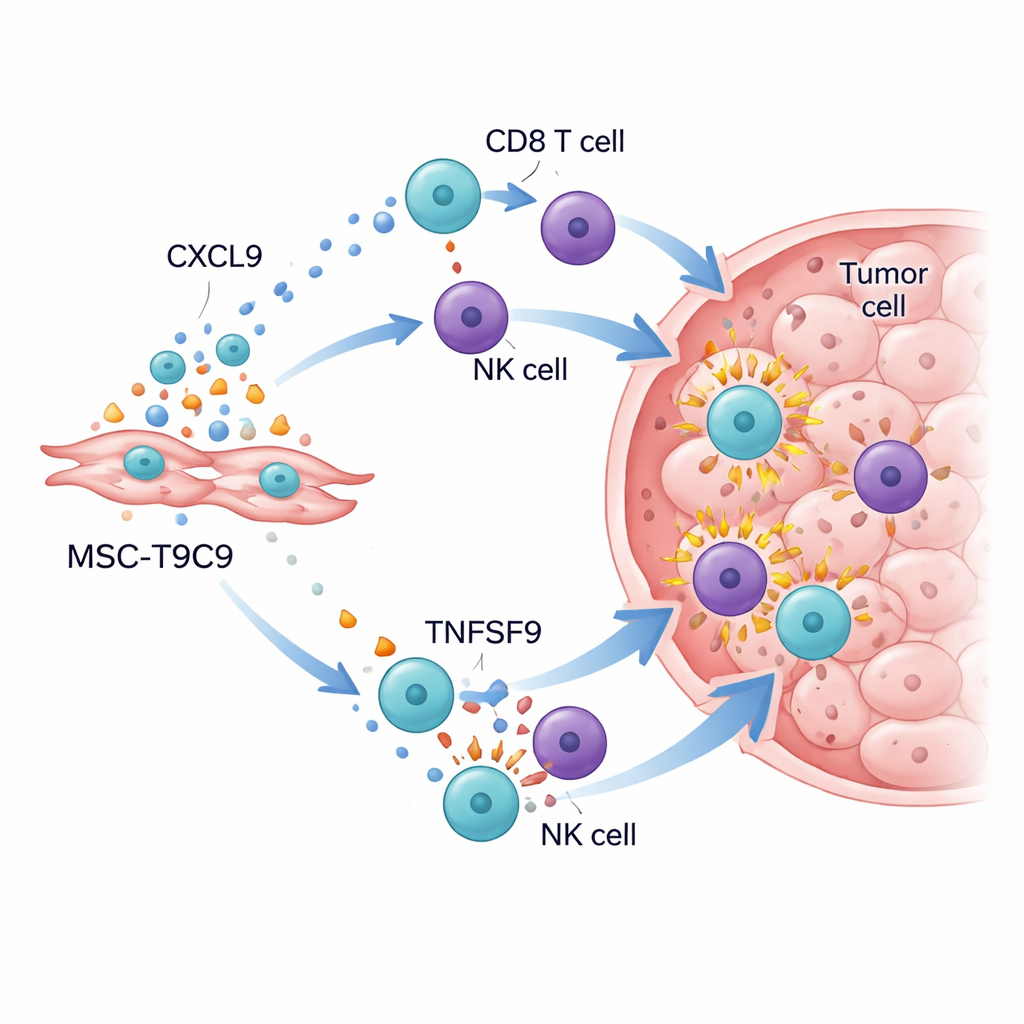
Réveiller le champ de bataille immunitaire de la tumeur
Lorsque les cellules modifiées ont été administrées à des souris porteuses de tumeurs mammaires triple négatives, les résultats ont été frappants. Chez des souris immunocompétentes, des injections répétées de MSC‑T9C9 ont considérablement ralenti la croissance tumorale et augmenté la mort des cellules cancéreuses, tandis que les cellules souches témoins avaient peu d’effet. L’analyse détaillée des tumeurs a montré une augmentation spectaculaire du nombre de lymphocytes T « tueurs » CD8 et de cellules NK, ainsi que des niveaux plus élevés de molécules d’attaque puissantes telles que la granzyme B, l’interféron‑γ, le facteur de nécrose tumorale‑α et l’interleukine‑2. Parallèlement, le microenvironnement tumoral a quitté un état suppressif : les macrophages inflammatoires bénéfiques ont augmenté et, bien que les cellules T régulatrices restent présentes, elles ont été dépassées en nombre par la nouvelle vague de combattants. Chez des souris déficientes en immunité, où les lymphocytes T et les cellules NK sont absents, MSC‑T9C9 n’a pas ralenti la croissance tumorale, confirmant que son bénéfice dépend de la mobilisation des défenses de l’organisme.
Préparer les tumeurs à la thérapie par inhibition des points de contrôle
Les médicaments immunothérapeutiques modernes, comme les anticorps anti‑PD‑1, relâchent les « freins » moléculaires sur les lymphocytes T, mais ils fonctionnent mieux lorsqu’un nombre suffisant de lymphocytes T est déjà présent dans la tumeur. L’étude a montré que MSC‑T9C9 non seulement attirait davantage de lymphocytes T CD8 dans les tumeurs, mais les poussait aussi vers un état fortement actif, tout en restant sensible aux freins, marqué par le récepteur PD‑1. Dans un modèle murin, la combinaison de MSC‑T9C9 avec un médicament anti‑PD‑1 a produit la réduction tumorale la plus importante et la survie la plus longue comparativement à chaque traitement seul. Des analyses de bases de données de cancers humains soutiennent cette idée : les patients présentant des niveaux combinés plus élevés de TNFSF9 et CXCL9 étaient plus susceptibles de bénéficier des thérapies de blocage des points de contrôle, suggérant que la même biologie pourrait s’appliquer chez l’humain.
Sécurité et promesses futures
Tout traitement qui stimule l’immunité suscite des inquiétudes quant à des effets indésirables dangereux tels qu’une inflammation généralisée ou des lésions d’organes. De manière encourageante, les souris recevant MSC‑T9C9 ont conservé un poids et un comportement normaux, n’ont montré aucune lésion évidente des principaux organes et présentaient des analyses sanguines et hépato‑rénales normales. Fait important, l’augmentation de l’activité immunitaire est restée en grande partie confinée à la tumeur elle‑même, et les signaux inflammatoires dans la circulation sanguine n’ont pas augmenté. Bien que des travaux supplémentaires soient nécessaires avant des essais humains — y compris des tests dans des modèles plus réalistes et des études minutieuses de l’ajustement des doses — cette étude suggère que guider des cellules souches génétiquement modifiées vers les tumeurs pour attirer et activer les cellules immunitaires pourrait offrir une manière ciblée et plus sûre de transformer les cancers du sein triple négatifs « froids » en cancers « chauds » mieux réceptifs à l’immunothérapie.
Citation: Ye, P., Wen, Y., Liu, R. et al. Co-delivery of chemokine CXCL9 and costimulatory ligand TNFSF9 by mesenchymal stem cells reprograms the immune microenvironment for triple-negative breast cancer. npj Breast Cancer 12, 30 (2026). https://doi.org/10.1038/s41523-026-00893-5
Mots-clés: cancer du sein triple négatif, immunothérapie, cellules souches mésenchymateuses, microenvironnement tumoral, blocage des points de contrôle