Clear Sky Science · fr
Interleukine-1α d’origine hôte induit l’immunosuppression tumorale en reprogrammant les cellules myéloïdes associées à la tumeur
Pourquoi cette recherche est importante pour les patients atteints de cancer
L’immunothérapie a transformé le traitement de certains cancers, mais de nombreuses tumeurs mammaires continuent d’échapper au système immunitaire. Cet article explore un coupable moins connu : une molécule de signalisation appelée interleukine‑1 alpha (IL‑1α) produite non pas par les cellules cancéreuses elles‑mêmes, mais par des cellules normales de l’organisme. Les auteurs montrent que l’IL‑1α d’origine hôte peut subtilement transformer les cellules immunitaires en alliées de la tumeur, et que bloquer ce signal chez la souris peut entraîner la diminution ou la disparition des tumeurs mammaires. Comprendre ce basculement pourrait aider les cliniciens à concevoir des traitements rendant l’immunothérapie plus efficace pour le cancer du sein.
Un influenceur caché dans le voisinage tumoral
Les cancers ne se développent pas isolément ; ils vivent dans un « voisinage » animé d’un grand nombre de cellules immunitaires, de vaisseaux sanguins et de tissu conjonctif, connu sous le nom de microenvironnement tumoral. Parmi les résidents les plus importants figurent les cellules myéloïdes, en particulier les macrophages, qui peuvent soit attaquer les tumeurs soit les protéger. Les manuels classiques divisent les macrophages en M1 (anti‑tumeur) et M2 (pro‑tumeur), mais les tumeurs réelles présentent de nombreuses nuances intermédiaires. Les auteurs se sont concentrés sur l’IL‑1α, une molécule normalement produite par des tissus non cancéreux, pour déterminer si ce signal d’origine hôte oriente les cellules myéloïdes entrantes vers des rôles utiles ou nuisibles au sein des tumeurs mammaires.
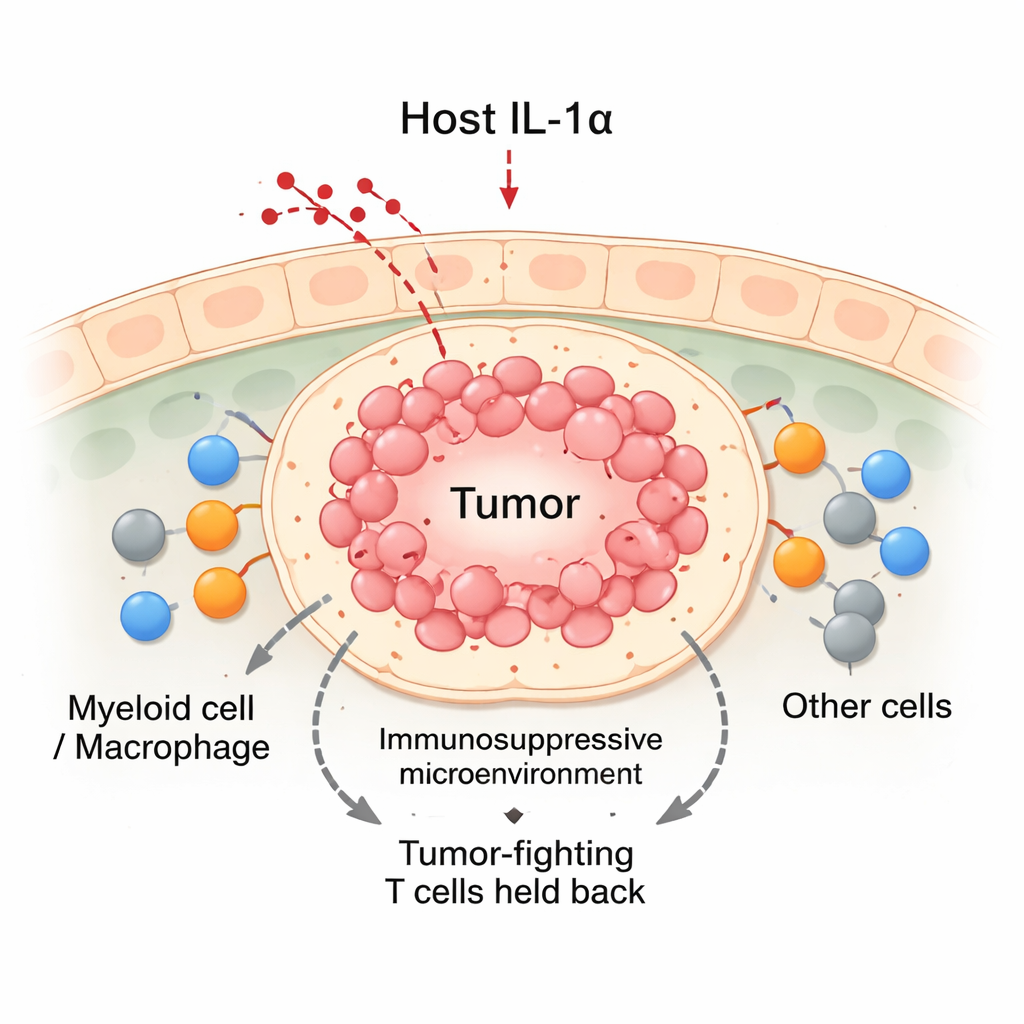
Éteindre l’IL‑1α renverse l’équilibre en défaveur des tumeurs
En utilisant des modèles murins du cancer du sein, l’équipe a comparé des animaux normaux à d’autres génétiquement modifiés pour ne pas exprimer l’IL‑1α. Lorsque des cellules de cancer du sein ont été transplantées dans les glandes mammaires, les tumeurs des souris normales ont progressé régulièrement. En revanche, les tumeurs chez les souris déficientes en IL‑1α ont d’abord crû pendant environ deux semaines puis ont fréquemment régressé. Ces tumeurs en régression contenaient globalement plus de cellules immunitaires, notamment une poussée de cellules T CD8 « tueuses » et de cellules myéloïdes. Bien que les souris déficientes en IL‑1α présentaient moins de globules blancs en circulation, elles accumulaient beaucoup plus de cellules immunitaires au site tumoral. Des analyses détaillées ont montré que les cellules T CD8 infiltrantes dans les tumeurs sans IL‑1α étaient plus actives, produisant davantage de molécules cytotoxiques et présentant moins de signes d’épuisement.
Comment l’IL‑1α reconfigure les cellules myéloïdes associées à la tumeur
Pour comprendre l’action de l’IL‑1α au niveau cellulaire, les chercheurs ont utilisé le séquençage ARN unicellulaire pour examiner des milliers de cellules individuelles provenant des tumeurs. Ils ont découvert que seule une petite sous‑population de macrophages associés à la tumeur — ceux marqués par un récepteur appelé CX3CR1 — produisait l’IL‑1α. Chez les souris normales, de nombreux monocytes entrants mûrissaient en ces macrophages CX3CR1 positifs, associés à un comportement immunosuppresseur. Chez les souris dépourvues d’IL‑1α, cette voie de maturation était perturbée. À la place, les cellules myéloïdes étaient plus susceptibles de devenir des macrophages inflammatoires iNOS‑positifs, un profil associé à une activité anti‑tumorale. Sur le plan fonctionnel, les cellules myéloïdes provenant des tumeurs déficientes en IL‑1α étaient moins capables d’induire des freins comme PD‑1 et CTLA‑4 sur les lymphocytes T, et montraient une moindre capacité à freiner la prolifération des T.
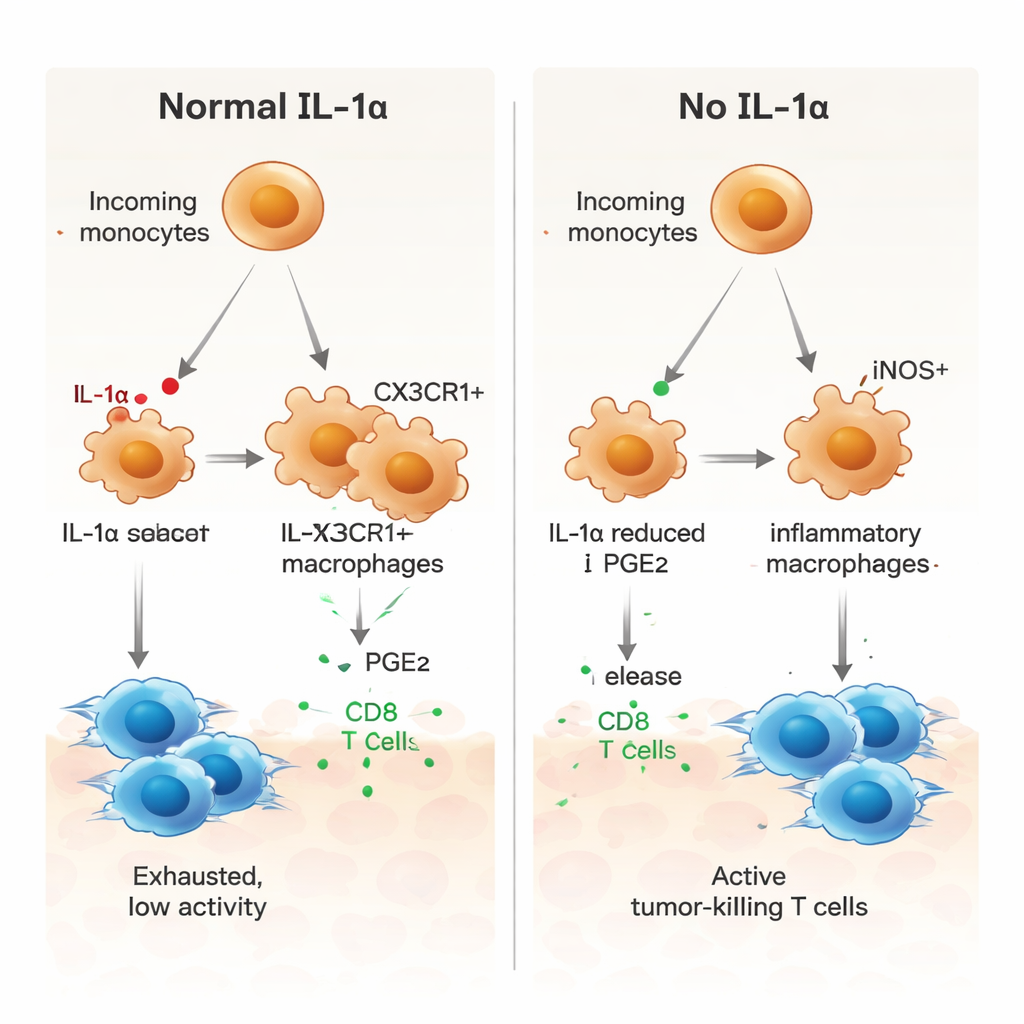
Un rôle clé pour un messager lipidique, la PGE2
Les auteurs se sont ensuite demandé comment l’IL‑1α pousse les cellules myéloïdes vers un état pro‑tumeur. L’analyse des communications à partir des données unicellulaires a pointé plusieurs voies de signalisation, dont une impliquant la prostaglandine E2 (PGE2), un médiateur lipidique connu pour favoriser l’immunosuppression. Dans les tumeurs dépourvues d’IL‑1α, les macrophages exprimaient des niveaux inférieurs de récepteurs pour le facteur de croissance des macrophages (M‑CSF), des récepteurs de TGF‑β et d’un récepteur de la PGE2, et les cellules stromales voisines produisaient moins des enzymes qui synthétisent la PGE2. En culture, des macrophages dérivés de la moelle osseuse de souris déficientes en IL‑1α présentaient un profil plus inflammatoire, avec plus d’iNOS et moins de CX3CR1. L’ajout de PGE2 inversait ce changement et rétablissait un profil plus suppressif, tandis que le blocage de la PGE2 chez des macrophages normaux les poussait vers un état pro‑inflammatoire. Les macrophages sans IL‑1α stimulaient également plus fortement la prolifération des cellules T CD8 spécifiques de la tumeur, un effet atténué lorsque la PGE2 était réintroduite.
Relier les résultats murins à l’immunité humaine
Pour vérifier si leurs données murines reflètent la biologie humaine, l’équipe a comparé les signatures géniques des différentes sous‑populations de macrophages murins à un large panel de cellules myéloïdes humaines orientées vers divers états en laboratoire. Les groupes de macrophages provenant des tumeurs chez les souris normales ressemblaient à des cellules humaines poussées vers des états de type M2 et d’affaiblissement immunitaire par des molécules telles que IL‑10, IL‑4 et les glucocorticoïdes. En revanche, les mêmes groupes issus de tumeurs déficientes en IL‑1α correspondaient à des cellules humaines dans des conditions plus inflammatoires et moins suppressives. Notamment, les profils géniques liés à la signalisation de la PGE2 étaient enrichis dans les macrophages dépendants de l’IL‑1α mais absents en l’absence d’IL‑1α, renforçant l’idée que IL‑1α et PGE2 agissent de concert pour établir une niche immunosuppressive.
Ce que cela pourrait signifier pour les futures thérapies du cancer du sein
En termes clairs, cette étude suggère qu’une molécule d’origine hôte, l’IL‑1α, peut discrètement ordonner à certains macrophages de protéger la tumeur et de contenir l’activité des cellules T tueuses, en partie via la voie de la PGE2. Lorsque l’IL‑1α est supprimée chez la souris, les macrophages basculent vers un état plus inflammatoire et anti‑tumoral, les cellules T CD8 deviennent plus actives, et les tumeurs mammaires transplantées sont souvent rejetées. Comme les immunothérapies actuelles visent déjà à réactiver les lymphocytes T épuisés, les combiner avec des approches bloquant l’IL‑1α ou sa voie en aval via la PGE2 pourrait encore orienter le microenvironnement tumoral en faveur du système immunitaire du patient. Bien que des études supplémentaires soient nécessaires pour évaluer la sécurité et l’efficacité chez l’homme, ces résultats mettent en lumière l’IL‑1α comme une nouvelle cible prometteuse pour rendre le cancer du sein plus vulnérable à l’attaque immunitaire.
Citation: Keerthi Raja, M.R., Gupta, G., Atkinson, G. et al. Host-derived interleukin-1α drives tumor immunosuppression by reprogramming tumor-associated myeloid cells. npj Breast Cancer 12, 26 (2026). https://doi.org/10.1038/s41523-026-00890-8
Mots-clés: immunothérapie du cancer du sein, microenvironnement tumoral, macrophages, interleukine-1 alpha, prostaglandine E2