Clear Sky Science · fr
Régulation microbienne des molécules de signalisation associées au stress et rôle dans la santé et la maladie
Comment de minuscules habitants intestinaux façonnent notre réaction au stress
La plupart d’entre nous considèrent le stress comme quelque chose qui se passe dans la tête, mais cet article montre que certains des acteurs les plus importants de notre réponse au stress vivent dans notre intestin. Les microbes qui colonisent nos intestins font bien plus que faciliter la digestion : ils peuvent produire, dégrader et remodeler les hormones mêmes qui contrôlent la manière dont notre corps réagit à la pression, à la peur et à la douleur. Comprendre ce partenariat caché pourrait ouvrir de nouvelles voies pour soulager des affections telles que la maladie inflammatoire de l’intestin, la dépression et d’autres maladies liées au stress.
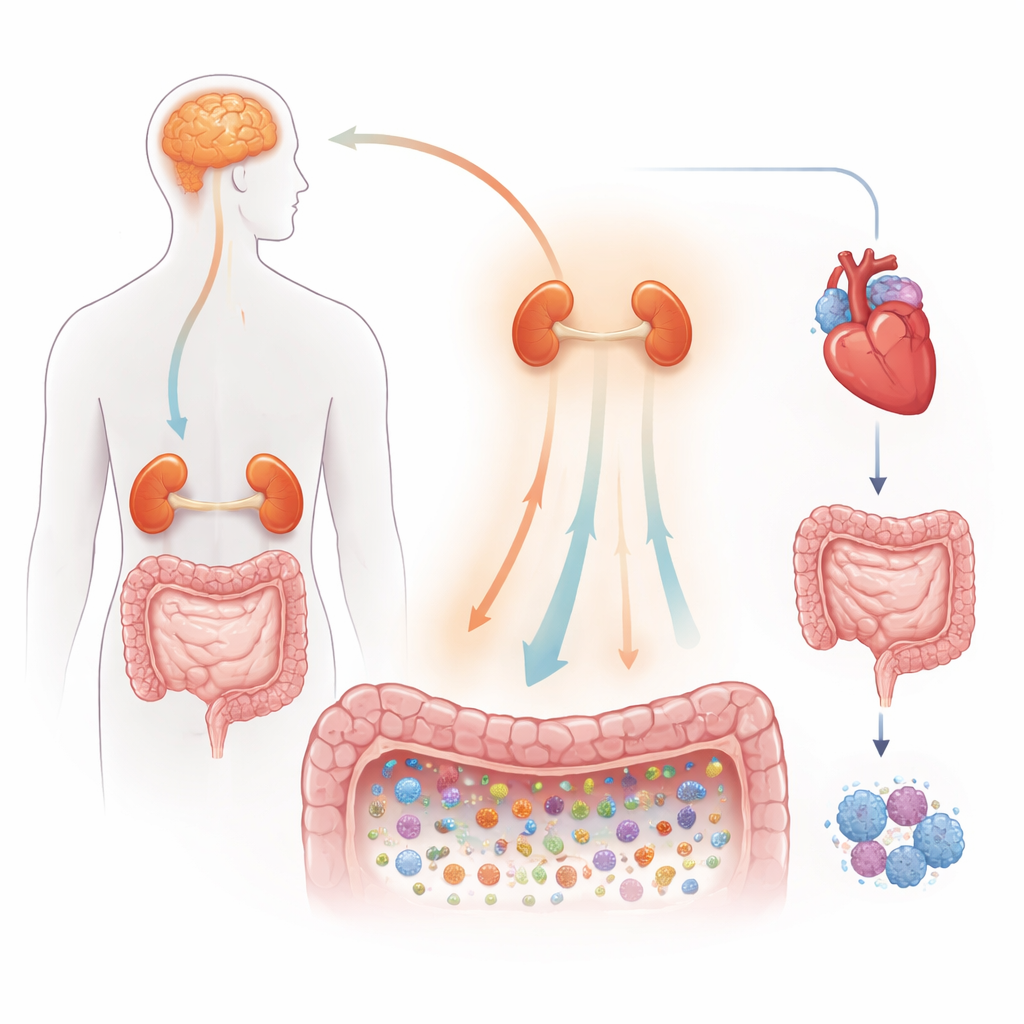
Le système d’alarme intégré du corps
Les auteurs commencent par décrire le fonctionnement habituel de la réponse au stress. Lorsqu’on fait face à un défi, le cerveau active une chaîne de commandement qui passe par l’hypophyse et les glandes surrénales, inondant le corps de messagers chimiques tels que des catécholamines proches de l’adrénaline et des hormones stéroïdes appelées glucocorticoïdes. Ces signaux augmentent la fréquence cardiaque, redirigent le flux sanguin, modifient le mouvement intestinal et ajustent le système immunitaire pour une réponse de « lutte ou fuite ». Des nerfs reliés directement au tube digestif fournissent une voie rapide pour transmettre des signaux à l’intestin, resserrant ou relâchant la barrière intestinale et modifiant l’environnement local où vivent les microbes. Cela fait de l’intestin un carrefour clé où la biologie du stress et le microbiome se rencontrent en continu.
Des microbes qui écoutent et répondent aux signaux de stress
Des recherches menées sur plusieurs décennies révèlent que de nombreuses bactéries peuvent détecter et utiliser nos molécules liées au stress. Des expériences anciennes ont montré que certaines bactéries intestinales et pathogènes se multiplient plus rapidement et deviennent plus agressives lorsqu’elles sont exposées à des catécholamines comme la noradrénaline et l’adrénaline. D’autres travaux ont démontré que des bactéries peuvent absorber ces molécules, les convertir en formes nouvelles, ou même produire des composés similaires elles-mêmes à partir d’acides aminés tels que la tyrosine. Parallèlement, les enzymes de l’hôte « éteignent » souvent les catécholamines en leur attachant de petits groupes chimiques ; des bactéries intestinales dotées des outils appropriés peuvent couper ces groupes, restaurant ainsi la forme active. Chez des souris dépourvues de microbes, la plupart des messagers de stress dans l’intestin sont bloqués sous forme inactive, mais l’introduction de bactéries spécifiques restaure le pool actif, montrant que les microbes contrôlent directement la disponibilité de ces signaux.
Modifier les stéroïdes du stress de l’intérieur
La revue se tourne ensuite vers les glucocorticoïdes, ces hormones stéroïdes connues pour maîtriser l’inflammation et aider l’organisme à faire face au stress chronique. De petites quantités de ces hormones pénètrent dans l’intestin depuis la circulation sanguine ou sont produites localement dans l’épithélium intestinal, où elles rencontrent des communautés bactériennes denses. De nombreux microbes intestinaux possèdent des enzymes spécialisées capables d’amoindrir, de réarranger ou de réduire ces molécules stéroïdes. Certains enlèvent des chaînes latérales pour les transformer en androgènes, qui agissent davantage comme des hormones sexuelles et peuvent influencer la pression artérielle voire des cancers hormono-dépendants. D’autres retirent des groupes chimiques particuliers, affaiblissant la capacité de l’hormone à se lier à son récepteur, ou réduisent encore la structure afin qu’elle ne puisse plus être recyclée en formes puissantes. D’autres enfin inversent les étapes d’« inactivation » de l’organisme en enlevant des groupes sulfate ou des moieties ressemblant à des sucres, rétablissant les stéroïdes dans une circulation active. Ensemble, ces actions font du microbiome un bouton de contrôle dynamique sur l’intensité et l’équilibre des stéroïdes.
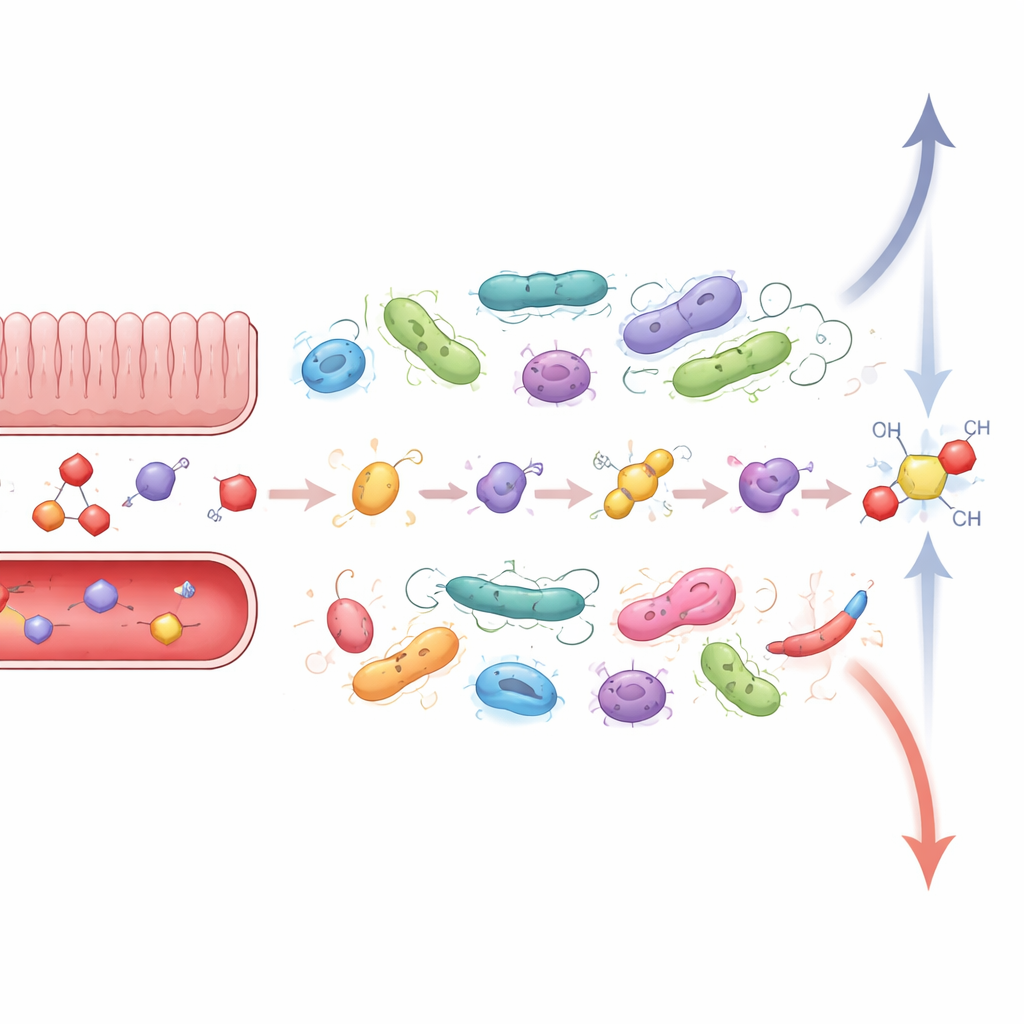
Quand stress, inflammation et microbes s’alimentent mutuellement
Ces échanges chimiques intimes prennent toute leur importance dans les maladies où stress et microbiote sont déjà perturbés. La maladie inflammatoire de l’intestin (MII) en est un bon exemple : les patients présentent une inflammation intestinale chronique, des communautés microbiennes altérées et une sensibilité accrue au stress de la vie. Les hormones du stress peuvent fragiliser la barrière intestinale, permettant à davantage de microbes et de leurs produits de traverser et d’exciter le système immunitaire. En même temps, la MII est associée à des proliférations d’espèces capables de remodeler le cortisol et les stéroïdes associés, ainsi qu’à des pertes de bactéries productrices d’acides gras à chaîne courte, de petits produits de fermentation qui aident normalement à sceller la barrière et à calmer l’inflammation. Des études animales suggèrent que ces changements microbiens peuvent amplifier les déséquilibres hormonaux et l’activité immunitaire, enfermant les patients dans un cercle vicieux où le stress aggrave la maladie intestinale et la maladie intestinale renforce le stress.
Nouvelles approches pour apaiser la boucle intestin–stress
Parce que les microbes siègent à l’intersection des signaux de stress et de l’inflammation, ils constituent des cibles attractives pour de nouvelles thérapies. L’article met en lumière des travaux montrant que des régimes riches en fibres comme l’inuline peuvent augmenter les produits de fermentation bénéfiques, réduire l’inflammation intestinale et atténuer certains dommages liés au stress dans des modèles de MII. Des souches probiotiques de Lactobacillus ont été trouvées pour renforcer la barrière intestinale, réduire les pics hormonaux induits par le stress et diminuer la sensibilité à la douleur chez l’animal. L’administration directe d’acides gras à chaîne courte dans le côlon peut réduire les comportements d’anxiété chez la souris et atténuer les réponses en cortisol au stress social chez l’humain. Ces succès préliminaires suggèrent que des probiotiques, prébiotiques et métabolites microbiens conçus avec soin pourraient aider à réinitialiser la réponse au stress en remodelant la gestion des hormones dans l’intestin.
Ce que cela signifie pour la santé quotidienne
Pour conclure, les auteurs soutiennent que les microbes intestinaux doivent être considérés comme des partenaires actifs de notre biologie du stress, et non comme de simples spectateurs. En produisant, modifiant et recyclant les molécules de signalisation liées au stress, le microbiome peut influencer l’intensité de nos réactions face aux défis, la rapidité de notre récupération et la probabilité que le stress nous entraîne vers une maladie chronique. Cela ne signifie pas qu’un microbe « magique » unique guérira le stress, mais cela suggère que protéger et nourrir un écosystème intestinal sain peut être l’un des outils les plus puissants pour renforcer la résilience. À mesure que les chercheurs cartographieront ces interactions microbe–hormone avec plus de précision et les testeront chez l’humain, des stratégies quotidiennes favorisant la santé intestinale pourraient devenir une composante centrale de la gestion du stress, de l’humeur et des affections inflammatoires.
Citation: Sie, C., Tropini, C. Microbial regulation of stress-associated signaling molecules and its role in health and disease. npj Biofilms Microbiomes 12, 65 (2026). https://doi.org/10.1038/s41522-026-00932-w
Mots-clés: microbiote intestinal, hormones du stress, axe microbiote-intestin-cerveau, maladie inflammatoire de l’intestin, endocrinologie microbienne