Clear Sky Science · fr
Élimination ciblée des infections de mammite à Staphylococcus aureus avec des systèmes de délivrance CRISPR-Cas basés sur des phages synthétiques
Combattre une infection coûteuse pour la filière laitière
Le lait des vaches et d’autres animaux d’élevage peut être compromis par une infection douloureuse de la glande mammaire appelée mammite, souvent provoquée par la bactérie Staphylococcus aureus. Le traitement de ces infections requiert généralement des cures longues d’antibiotiques, coûteuses, stressantes pour les animaux et contribuant à l’essor de la résistance aux antibiotiques. Cette étude explore une approche radicalement différente : transformer un parasite naturel des bactéries ressemblant à un virus en une arme de précision capable de couper l’ADN bactérien de façon sélective et d’éliminer les infections sans propager de gènes de résistance.
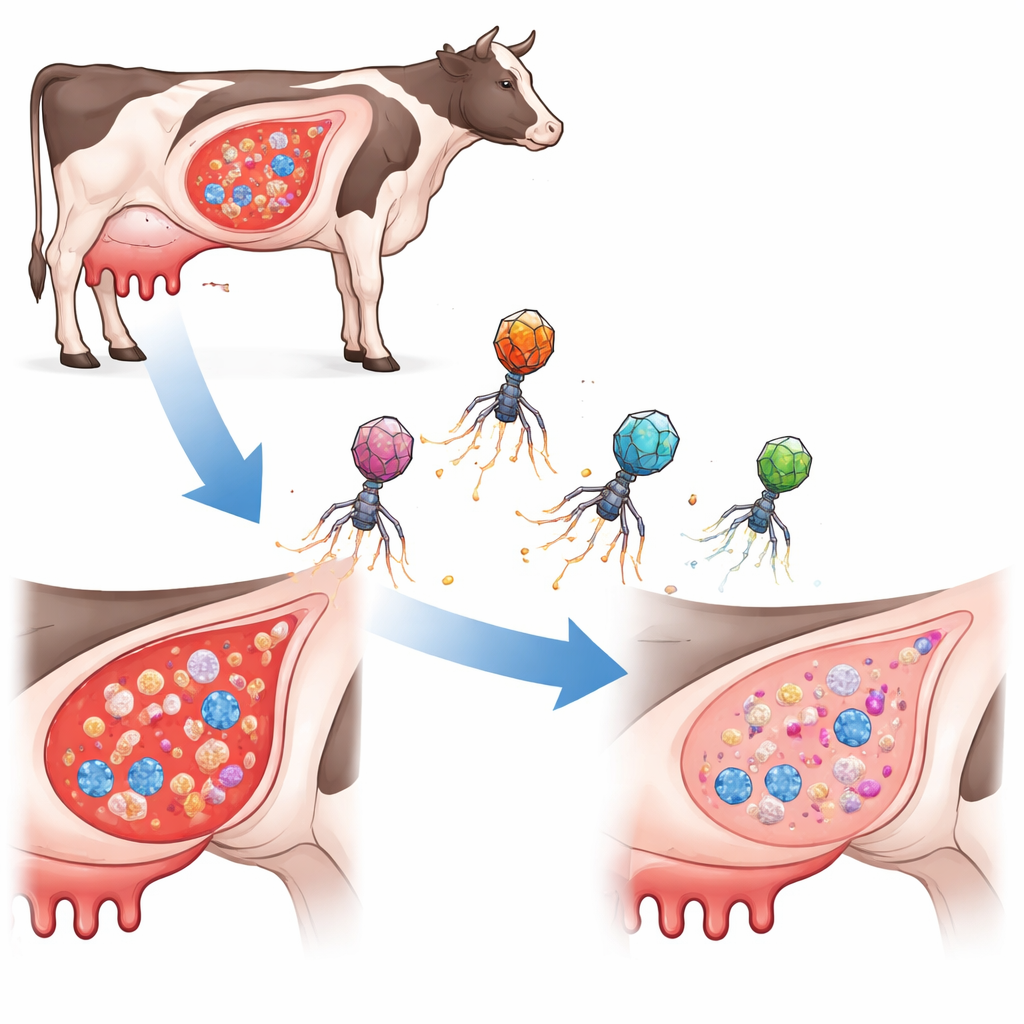
Un nouveau type de chasseur bactérien ciblé
Plutôt que d’utiliser des antibiotiques traditionnels ou des bactériophages ordinaires (virus infectant les bactéries), les chercheurs ont conçu de petits éléments porteurs d’ADN appelés îlots chromosomiques induits par phage. Dans la nature, ces îlots se font transporter dans des capsides de phage pour sauter d’une cellule bactérienne à une autre. Ici, l’équipe les a reconstruits sous forme d’« ePICI » qui portent l’outil d’édition génétique CRISPR‑Cas9 ainsi que de courtes séquences guides ciblant trois petits ARN régulateurs importants chez S. aureus. Lorsqu’un ePICI pénètre dans une cellule cible, Cas9 est produit et coupe le chromosome bactérien au site choisi, tuant la cellule de l’intérieur. Fait crucial, ces particules ingénierées ne se répliquent pas seules, ce qui limite leur diffusion et réduit le risque de transfert accidentel de gènes nocifs.
Comment le bouclier bactérien change la donne
S. aureus survit souvent au traitement en formant des biofilms — des communautés collantes où les cellules sont enfermées dans une matrice auto‑produite. L’équipe a comparé deux types courants de matrice : l’une principalement constituée d’une protéine appelée Bap, et l’autre faite d’un polymère sucré connu sous le nom de PIA/PNAG. Dans des tests en laboratoire, les biofilms riches en Bap protégeaient fortement les bactéries contre les ePICI et contre un phage auxiliaire standard, agissant comme une armure dense qui bloquait l’infection. En revanche, les biofilms à base du polymère sucré facilitaient l’élimination des bactéries, probablement parce que des enzymes présentes sur les capsides virales peuvent dégrader ces sucres et aider les particules à atteindre leurs cibles.
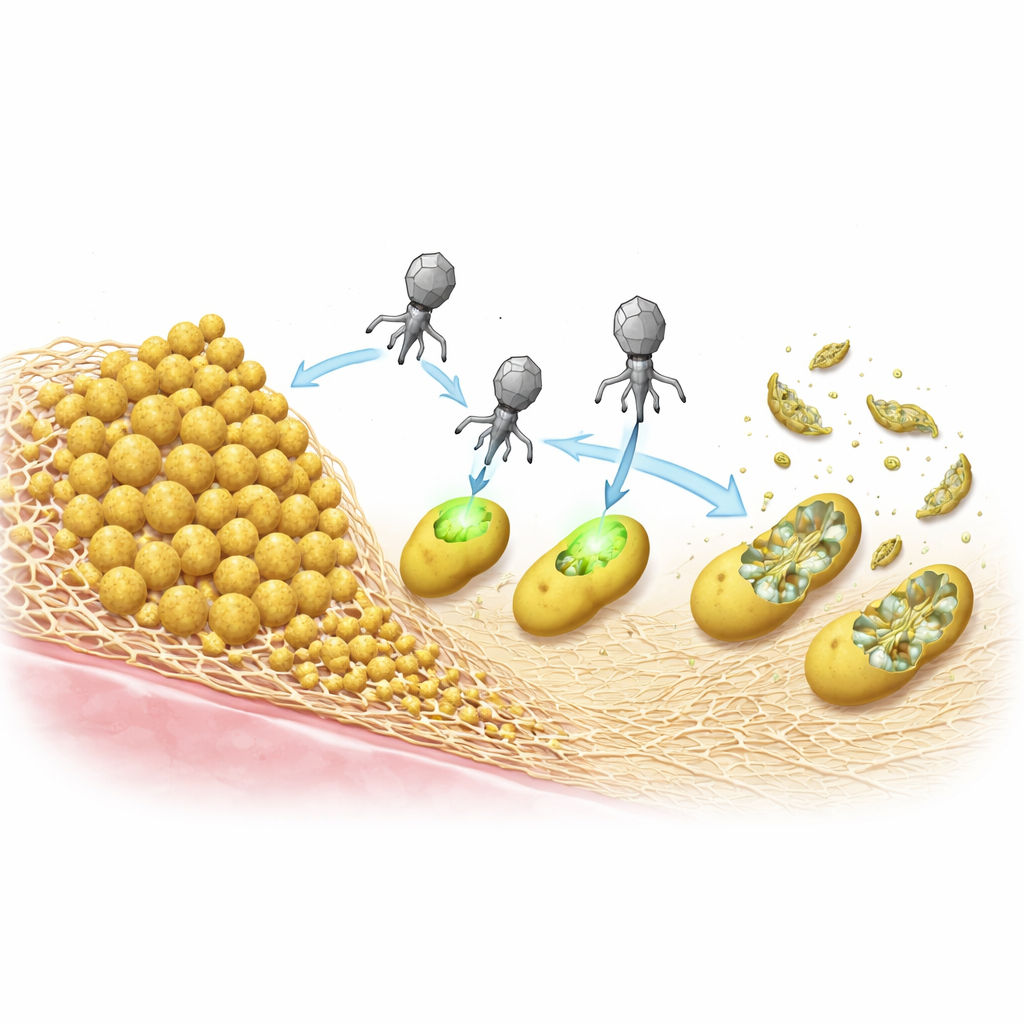
Tuer les bactéries sans intégrer leur ADN
Une fois à l’intérieur d’une cellule, les ePICI peuvent s’intégrer au chromosome bactérien, mais les chercheurs ont voulu savoir si cette étape était réellement nécessaire pour tuer. Ils ont créé une version incapable de s’intégrer et ont montré que, tant que la particule était produite correctement dans la souche source, elle était tout aussi létale pour S. aureus que l’originale. Cela signifie que le système CRISPR peut s’exprimer directement depuis l’ADN circulaire entrant, accomplir sa tâche, puis disparaître à mesure que la cellule meurt. Cette action sans intégration réduit en outre les chances de transfert de gènes non désiré et distingue ces particules de la thérapie par phages classique, qui repose sur la réplication virale et la lyse cellulaire pour se propager.
De la boîte de Petri aux glandes mammaires infectées
Parce que les souches productrices de Bap sont courantes dans la mammite laitière, l’équipe a testé leur construction la plus performante, appelée ePICIrsaE, dans un modèle murin qui reproduit l’infection de la mamelle. Dans le lait et en cultures de laboratoire, les biofilms riches en Bap réduisaient nettement l’activité des ePICI. Pourtant, à l’intérieur de la glande mammaire, des doses répétées d’ePICIrsaE ont fortement diminué le nombre de bactéries pour toutes les souches testées, y compris celles produisant Bap. Son efficacité était comparable à celle de la vancomycine, un antibiotique puissant de dernier recours. Les résultats suggèrent que les conditions dans les tissus vivants — comme une production réduite de Bap, la présence de bactéries en suspension ou des composants utiles du lait — permettent aux particules ingénierées de fonctionner bien mieux que dans des biofilms statiques en laboratoire.
Ce que cela pourrait signifier pour les exploitations et au‑delà
L’étude montre que des systèmes CRISPR empaquetés dans des phages et ne se répliquant pas peuvent éliminer sélectivement S. aureus dans une infection difficile liée aux biofilms sans se propager ni provoquer l’éclatement massif des cellules. Bien que des doses élevées de particules soient nécessaires et que l’extension de la souris à la vache pose des défis, ces particules offrent une alternative prometteuse et contrôlable aux antibiotiques pour des infections localisées comme la mammite. Plus largement, ce travail souligne que des traitements peu convaincants dans des essais simples en laboratoire peuvent réussir dans l’environnement complexe d’un animal, et ouvre la voie à des bibliothèques d’ePICI personnalisés adaptés à différentes bactéries, capsides virales et séquences guides.
Citation: Garmendia-Antoñana, N., Dorado-Morales, P., Gil, C. et al. Targeted elimination of Staphylococcus aureus mastitis infections with synthetic phage-based CRISPR-Cas delivery systems. npj Biofilms Microbiomes 12, 67 (2026). https://doi.org/10.1038/s41522-026-00931-x
Mots-clés: mammite bovine, Staphylococcus aureus, thérapie CRISPR, traitement à base de phages, infections en biofilm