Clear Sky Science · fr
Le microbiote intestinal médie des comportements de type dépressif chez des souris infectées chroniquement par Echinococcus multilocularis
Quand une infection cachée affecte l’esprit
La plupart des gens pensent aux parasites comme à un problème de l’intestin ou du foie, pas de l’esprit. Pourtant, de nombreux patients atteints d’infections prolongées rapportent une humeur dépressive, de la fatigue et une difficulté à prendre du plaisir. Cette étude explore un lien surprenant : comment une infection chronique par un ténia qui s’installe dans la cavité corporelle et le foie pourrait, via des modifications des bactéries intestinales et de la chimie corporelle, induire des comportements de type dépressif chez la souris. Comprendre cette chaîne d’événements pourrait éventuellement ouvrir de nouvelles pistes pour protéger la santé mentale des personnes vivant avec des infections tenaces.
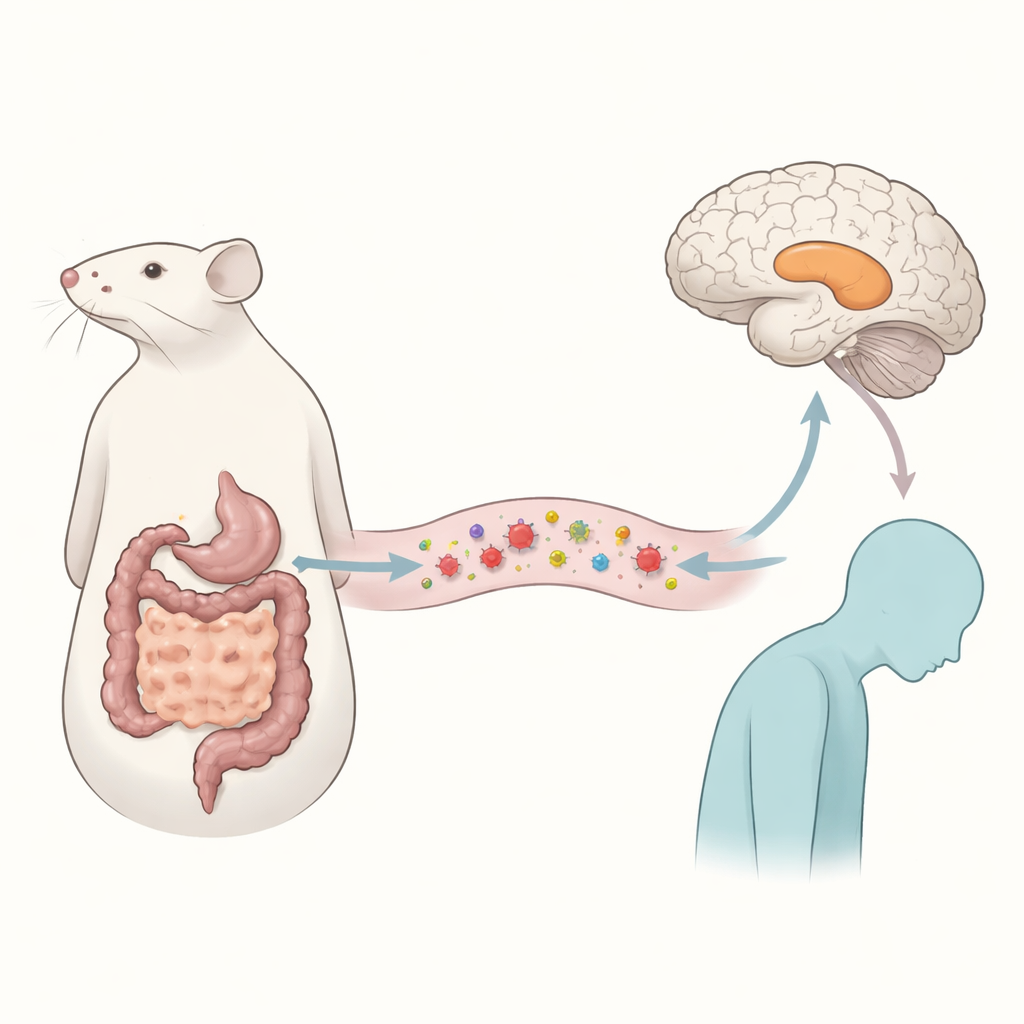
Un passager parasitaire et des altérations de l’humeur
Les chercheurs se sont concentrés sur Echinococcus multilocularis, le parasite responsable de l’échinococcose alvéolaire, une maladie sévère qui attaque principalement le foie. Les patients atteints signalent souvent une mauvaise santé mentale, mais les raisons restaient floues. Pour investiguer, l’équipe a infecté des souris par le parasite et attendu deux mois, suffisamment pour reproduire une infection chronique. Les animaux ont ensuite passé une batterie de tests comportementaux conçus pour distinguer un simple état de maladie de changements d’humeur plus spécifiques. Les souris infectées se déplaçaient autant que les saines et apprenaient et retenaient les tâches normalement, mais elles présentaient des signes nets de comportements de type dépressif : moins d’intérêt pour des récompenses sucrées et plus d’immobilité dans des tests de stress souvent interprétés comme des marqueurs d’états de désespoir chez les rongeurs.
Modifications cérébrales subtiles et signaux immunitaires
En examinant le cerveau, les scientifiques se sont focalisés sur l’hippocampe et l’amygdale, régions impliquées dans l’émotion et le stress. La structure globale de ces zones restait intacte, mais au microscope certains neurones semblaient rétrécis ou d’une morphologie anormale, et l’enveloppe extérieure de leurs noyaux paraissait plissée. Les cellules immunitaires résidentes du cerveau, les microglies, étaient plus nombreuses dans certaines régions et présentaient des formes plus simples et moins ramifiées — des signes d’un passage de leur état calme et surveillant à un état activé. Parallèlement, tant le tissu intestinal que le sang des souris infectées contenaient des niveaux plus élevés de molécules inflammatoires, en particulier les cytokines IL‑6 et MCP‑1, et les gènes codant certaines de ces molécules étaient plus actifs dans l’hippocampe. Ensemble, ces observations indiquent un état inflammatoire chronique qui s’étend de l’intestin au cerveau et perturbe l’équilibre des cellules immunitaires cérébrales.
Bactéries intestinales et messagers chimiques en perte
L’équipe a ensuite évalué si la communauté microbienne intestinale pouvait jouer un rôle. Par séquençage de l’ADN, ils ont constaté que l’infection remodelait le microbiote intestinal : des groupes bénéfiques comme Lactobacillus et Bifidobacterium ont fortement diminué, tandis que d’autres genres, notamment Ruminococcus et Prevotella, ont augmenté. Les souris présentant moins de bactéries « amies » avaient tendance à montrer des niveaux plus élevés de cytokines inflammatoires dans l’intestin et le sang. Parallèlement, des analyses sanguines et un profilage métabolique étendu ont révélé que des éléments clés de la voie tryptophane–sérotonine étaient épuisés. Les taux de tryptophane (un acide aminé alimentaire), de son intermédiaire N‑acétyl‑sérotonine et du neurotransmetteur sérotonine (5‑HT) ont tous diminué chez les animaux infectés. Ces changements reflètent des altérations rapportées chez des personnes souffrant de dépression majeure et étaient fortement corrélés à l’abondance de certains microbes intestinaux.
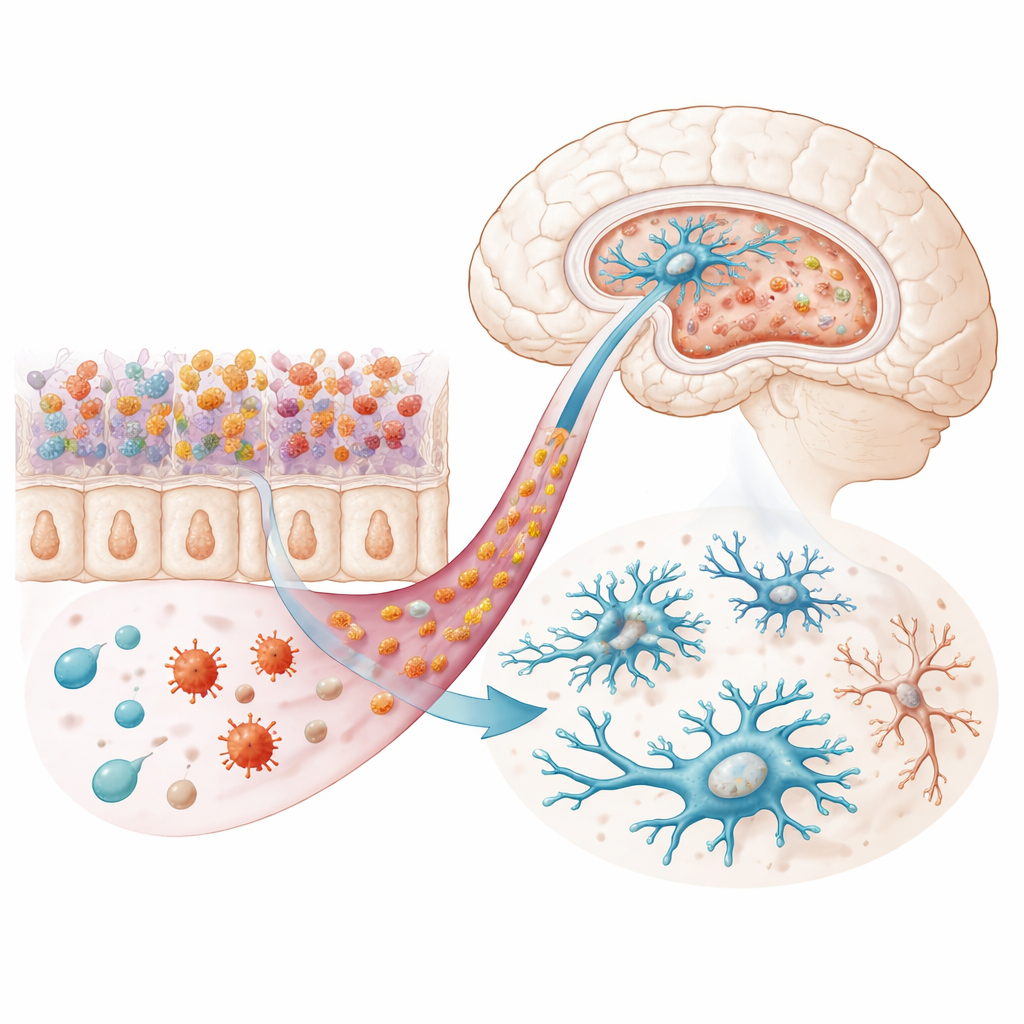
Transférer le microbiome, transférer l’humeur
Pour tester si le microbiote altéré suffisait à modifier le comportement, les chercheurs ont réalisé des transplantations fécales de microbiote. Ils ont d’abord vidé le microbiote de souris saines avec des antibiotiques, puis introduit des selles de donneurs infectés ou non infectés. De manière remarquable, les receveurs du microbiote provenant de donneurs infectés ont développé des comportements de type dépressif et une évitement anxieux du centre d’une aire ouverte, bien qu’ils n’aient jamais été exposés au parasite. Ces souris présentaient également une inflammation accrue, des niveaux réduits de tryptophane et de molécules liées à la sérotonine dans le sang, et des microglies ressemblant à celles des animaux directement infectés — plus nombreuses dans certaines régions, moins ramifiées et remplies de structures de type lysosome suggérant un stress cellulaire accru ou une activité de « nettoyage » renforcée.
Qu’est-ce que cela signifie pour la santé humaine
Pour un non-spécialiste, le message principal est qu’une infection chronique dans l’organisme peut perturber les habitants microbiens de l’intestin et les messagers chimiques qu’ils contribuent à produire, et que cela peut à son tour influencer les cellules immunitaires du cerveau et les circuits de l’humeur. L’étude ne prétend pas que ce ténia provoque la dépression clinique chez l’homme, mais elle offre une feuille de route détaillée montrant comment un parasite persistant, un intestin inflammé, un microbiote perturbé et une chimie tryptophane–sérotonine altérée pourraient agir de concert pour générer des comportements de type dépressif. Ce tableau émergent suggère que traiter les complications psychiatriques des infections chroniques pourrait un jour inclure non seulement l’élimination du parasite, mais aussi l’apaisement de l’inflammation et la restauration d’un microbiome intestinal sain.
Citation: Wen, R., Xin, Y., Bao, S. et al. The gut microbiota mediates depression-like behaviors in mice with chronic Echinococcus multilocularis infection. npj Biofilms Microbiomes 12, 63 (2026). https://doi.org/10.1038/s41522-026-00929-5
Mots-clés: axe intestin–cerveau, microbiome, infection parasitaire, dépression, métabolisme du tryptophane