Clear Sky Science · fr
La voie de régulation ppGpp-HpaR1-gum module la production d’exopolysaccharides chez Xanthomonas campestris pv. campestris
Pourquoi des bactéries « collantes » comptent pour les cultures
De nombreuses bactéries pathogènes survivent et se propagent en s’enveloppant d’un manteau visqueux de sucres appelé biofilm. Dans les cultures légumières comme le chou et le brocoli, ces films peuvent obstruer les conduits d’eau des plantes, provoquant la fameuse maladie de la « pourriture noire » et d’importantes pertes de rendement. Cette étude examine l’une de ces bactéries, Xanthomonas campestris, pour révéler comment un système d’alerte chimique interne contrôle la production de son bouclier sucré. Comprendre ce circuit de contrôle caché pourrait aider les chercheurs à concevoir de meilleures stratégies de protection des cultures ou même à exploiter ces sucres pour des matériaux utiles.
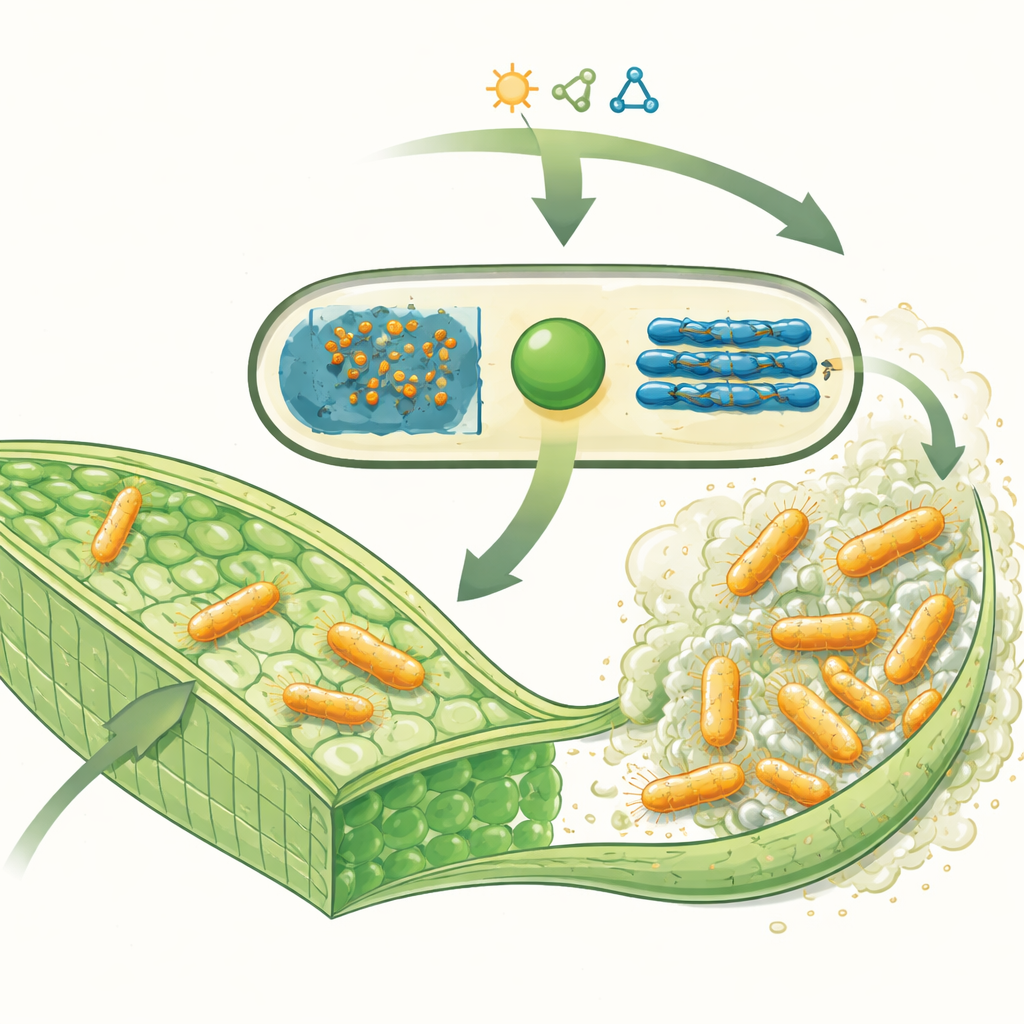
Le microbe infectant les plantes et son armure sucrée
Xanthomonas campestris pénètre dans les nervures des crucifères — plantes telles que le chou, le chou-fleur et la moutarde — et produit d’importantes quantités d’une substance visqueuse appelée gomme xanthane. Ce matériau est constitué de longues chaînes d’unités de sucre et constitue une part majeure du biofilm qui aide les bactéries à s’attacher aux tissus végétaux, à résister aux défenses de la plante et à survivre en conditions difficiles. Dans la plante, ces couches épaisses de sucres peuvent bloquer le flux d’eau, entraînant la nécrose des tissus et les lésions foliaires en forme de V caractéristiques de la pourriture noire. Fait intéressant, la même gomme xanthane est largement utilisée comme épaississant dans les aliments et d’autres produits, faisant de ce sucre bactérien à la fois un fléau agricole et un atout industriel.
Une alarme interne qui façonne le comportement bactérien
Au cœur de nombreuses bactéries, une petite molécule de signalisation appelée ppGpp agit comme une alarme d’urgence. Lorsque les nutriments se raréfient ou que d’autres stress apparaissent, les niveaux de ppGpp augmentent et déclenchent une vaste « réponse stricte » qui reconfigure la croissance, le métabolisme et les stratégies de survie. Des travaux antérieurs ont montré que le ppGpp peut favoriser la formation de biofilms chez plusieurs espèces et que son absence chez Xanthomonas affaiblit la capacité de la bactérie à former des biofilms et à provoquer la maladie. Ce qui restait peu clair, c’était comment cette petite molécule se reliait concrètement aux machines qui synthétisent la couche épaisse d’exopolysaccharide (EPS) chez ce pathogène végétal.
Suivre le trajet du signal vers le sucre
Les chercheurs ont comparé des bactéries normales avec des mutants incapables de produire du ppGpp. Sur milieux riches en sucres, les mutants dépourvus de ppGpp formaient des colonies plus petites et moins muqueuses, et des mesures directes ont montré qu’ils produisaient significativement moins d’EPS. Cependant, le profil chimique obtenu par spectroscopie infrarouge et l’imagerie en microscopie électronique ont révélé que la composition de base et la conformation d’ordre supérieur de l’EPS restaient identiques : les mutants en produisaient simplement moins. L’attention s’est tournée vers le cluster génique « gum », un ensemble de gènes codant pour les enzymes assemblant la gomme xanthane. Grâce à des mesures d’expression génique et au séquençage de l’ARN, l’équipe a constaté que presque tous les gènes gum étaient réprimés dans les cellules dépourvues de ppGpp, plaçant ppGpp en amont de ce cluster dans la hiérarchie de régulation.
Un intermédiaire clé : l’interrupteur HpaR1
Entre l’alarme ppGpp et les gènes gum se trouve une protéine régulatrice appelée HpaR1, un facteur de transcription qui se lie à l’ADN et stimule l’activité des gènes gum. L’étude a montré que le ppGpp agit sur deux fronts. D’une part, les cellules dépourvues de ppGpp présentaient une activité réduite du gène hpaR1, ce qui signifiait moins de protéine HpaR1 disponible. D’autre part, dans des tests en laboratoire avec des protéines purifiées, l’ajout de ppGpp renforçait directement l’affinité de HpaR1 pour les régions d’ADN contrôlant les gènes gum et même pour sa propre région de contrôle. À des niveaux modérés de ppGpp, cette liaison était nettement renforcée, bien que des niveaux extrêmement élevés en affaiblissaient partiellement l’effet, suggérant un équilibre finement réglé. Lorsque les scientifiques ont augmenté artificiellement les niveaux de HpaR1, la production d’EPS a de nouveau augmenté — même chez des bactéries dépourvues de ppGpp — confirmant que HpaR1 est l’intermédiaire crucial entre le signal d’alarme et la machinerie de fabrication du sucre.
Ce que ce circuit de contrôle signifie pour les cultures et au-delà
En termes simples, ce travail met au jour une cascade en trois étapes au sein d’un pathogène végétal : une molécule d’alarme interne (ppGpp) augmente et renforce un interrupteur lié à l’ADN (HpaR1), qui à son tour active une usine de production de sucres (les gènes gum), conduisant à un manteau protecteur plus épais autour des bactéries. En cartographiant en détail la voie ppGpp–HpaR1–gum, l’étude explique comment des signaux de stress environnemental peuvent se traduire par des modifications de la production de matrice de biofilm. Pour les agriculteurs et les phytopathologistes, ces informations suggèrent de nouvelles cibles pour perturber l’armure bactérienne et réduire les dégâts liés à la pourriture noire. Pour les microbiologistes en général, les résultats apportent une pièce importante au puzzle de la manière dont des signaux de stress universels contrôlent la formation de communautés microbiennes complexes.
Citation: Bai, K., Xu, X., Yu, C. et al. The ppGpp-HpaR1-gum regulatory pathway modulates exopolysaccharides production in Xanthomonas campestris pv. campestris. npj Biofilms Microbiomes 12, 60 (2026). https://doi.org/10.1038/s41522-026-00926-8
Mots-clés: biofilms bactériens, agents pathogènes des plantes, gomme xanthane, signalisation de stress, exopolysaccharides