Clear Sky Science · fr
Caractérisation métabolique en temps réel et haute résolution de bactéries vivantes par imagerie métabolique optique sans marquage
Observer les germes réagir en temps réel
Les bactéries sont partout sur nous et en nous, et façonnent discrètement notre santé. Elles aident à digérer les aliments, protègent notre peau et provoquent parfois des infections tenaces qui résistent aux antibiotiques. Cette étude présente une méthode pour observer des bactéries vivantes réagir au stress et aux médicaments en temps réel, au niveau de cellules individuelles, sans ajouter de colorants ni d’étiquettes. Cette capacité pourrait, à terme, aider les médecins à choisir plus rapidement le bon traitement et permettre aux chercheurs de comprendre pourquoi certaines infections sont si difficiles à soigner.
La lumière comme fenêtre sur la vie bactérienne
Plutôt que d’ajouter des colorants ou des balises génétiques, les chercheurs exploitent le fait que les bactéries émettent naturellement une très faible fluorescence lorsque certaines molécules internes sont excitées par un laser. Deux de ces molécules, connues sous les noms de NAD(P)H et FAD, jouent un rôle central dans la conversion des aliments en énergie par la cellule. En utilisant une microscopie laser rapide et à haute résolution, l’équipe peut mesurer à la fois l’intensité et le très court délai temporel de cette fluorescence, ce qui révèle l’activité métabolique d’une cellule. Comme la méthode est sans marquage et non destructive, les mêmes bactéries vivantes peuvent être suivies sur des secondes et des minutes pendant que leur environnement change. 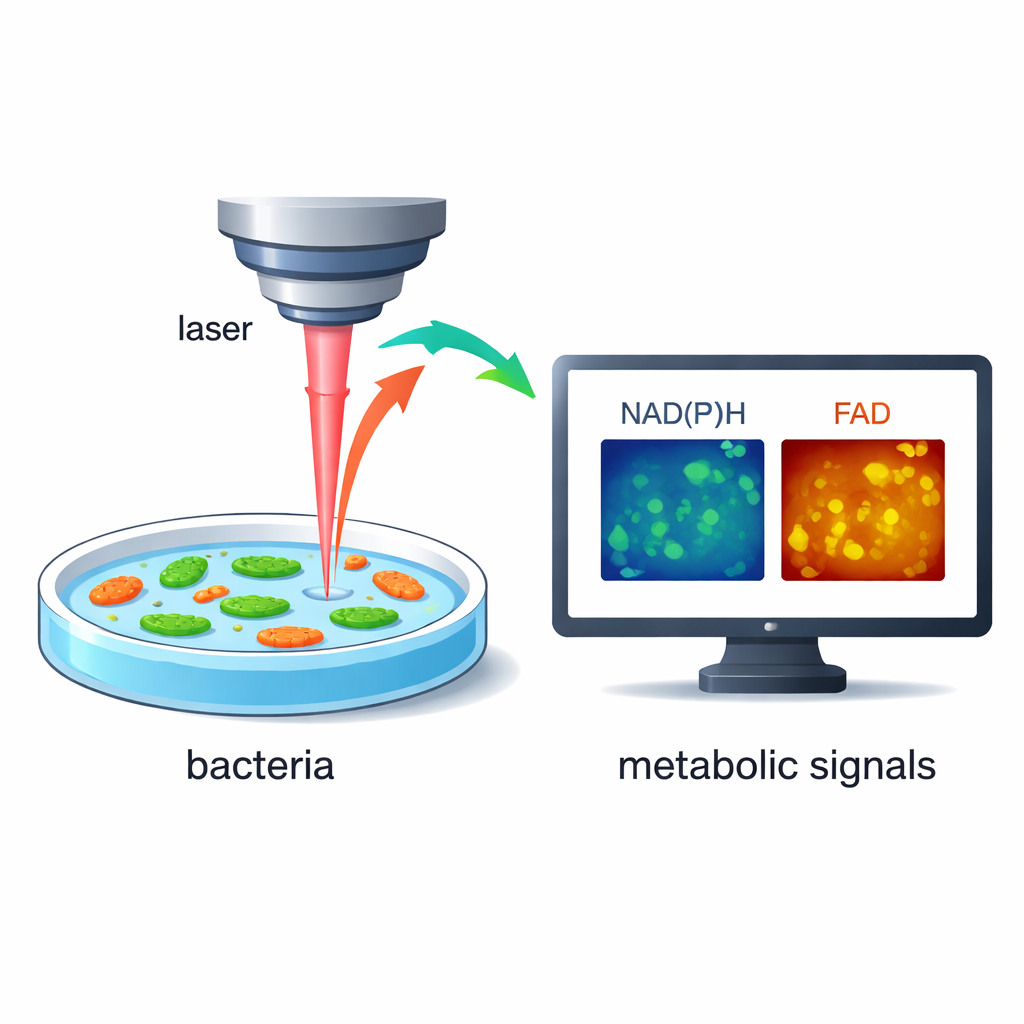
Voir les différences entre bactéries individuelles
La plupart des tests de laboratoire standard regroupent des millions de bactéries et ne fournissent qu’une réponse moyenne. Ici, les auteurs montrent que leur méthode d’imagerie peut isoler des cellules individuelles de Staphylococcus aureus en culture liquide et analyser chacune séparément, même à haute densité cellulaire. En comparant deux colonies de S. aureus cultivées dans les mêmes conditions, un signal clé (provenant du FAD) différait entre les colonies, et il existait aussi une dispersion de valeurs au sein de chaque colonie. Cela signifie que des bactéries génétiquement similaires dans le même flacon peuvent se trouver dans des états métaboliques très différents, une diversité cachée que les tests en vrac classiques pourraient manquer mais qui peut influencer la réponse des infections au traitement.
Observer l’action des antibiotiques en quelques secondes
L’équipe a ensuite suivi des cellules individuelles de S. aureus exposées à plusieurs traitements antibactériens, y compris des antibiotiques courants et de l’eau de Javel domestique. Grâce à leur dispositif d’imagerie rapide, ils ont capturé les changements dès le contact de la solution médicamenteuse avec les cellules et pendant les 30 minutes suivantes. Les traitements puissants entraînaient une baisse des signaux NAD(P)H et une hausse des signaux FAD, souvent en quelques secondes, traduisant un arrêt de la production d’énergie et un passage à un état intracellulaire plus oxydé. Le calendrier et le profil exacts de ces changements dépendaient du type et de la dose du médicament : par exemple, les antibiotiques bloquant la synthèse protéique ou ciblant la paroi cellulaire provoquaient une brève chute suivie d’une récupération partielle, tandis que l’eau de Javel induisait un changement net et soutenu. Ces « signatures lumineuses » distinctes suggèrent que la technique peut détecter non seulement si les cellules sont stressées ou meurent, mais aussi la manière dont elles sont endommagées. 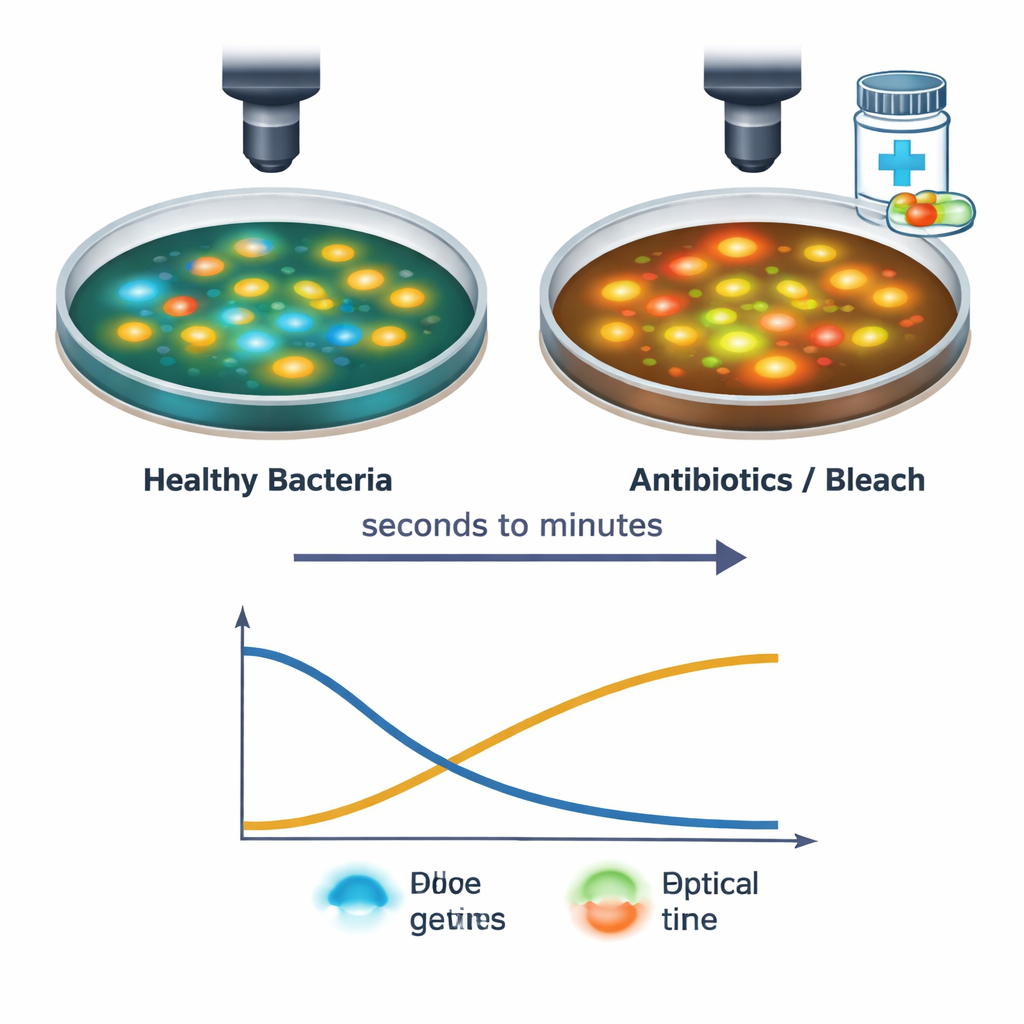
Plonger dans le monde caché des biofilms
Les bactéries vivent rarement isolées dans la nature ; elles forment plutôt des communautés visqueuses et protectrices appelées biofilms, sur des surfaces allant des implants médicaux aux dents. Dans ces couches denses, certaines cellules peuvent être très actives tandis que d’autres restent dormantes, un mélange qui aide la communauté à survivre aux antibiotiques. En utilisant de grandes images assemblées, les chercheurs ont cartographié le paysage métabolique au sein de biofilms de S. aureus et l’ont comparé aux cellules libres. Ils ont trouvé des poches lumineuses et métaboliquement actives entourées de régions moins actives et ont montré que, chez plusieurs espèces, les bactéries en biofilm avaient tendance à présenter un profil métabolique plus oxydé que leurs homologues libres. Des signaux optiques supplémentaires indiquaient une présence accrue de lipides et de protéines, cohérente avec la matière visqueuse qui maintient les biofilms.
Pourquoi cela compte pour la médecine de demain
Ensemble, ces résultats montrent que l’imagerie métabolique optique sans marquage peut fournir des instantanés rapides, détaillés et non invasifs de la façon dont les bactéries vivent, s’adaptent et meurent. Pour un lecteur non spécialiste, le message clé est que les scientifiques peuvent désormais « écouter » l’utilisation d’énergie par les bactéries en temps réel, sans perturber les cellules, en utilisant seulement de la lumière finement calibrée. À long terme, ce type de technologie pourrait aider à identifier des bactéries difficiles à cultiver, repérer des poches de cellules tolérantes aux médicaments au sein des biofilms ou tester rapidement la réponse d’une infection d’un patient à différents antibiotiques. Cela pourrait permettre des traitements plus rapides et mieux adaptés et approfondir notre compréhension des mondes microbiaux invisibles qui influencent notre santé au quotidien.
Citation: Sorrells, J.E., Yang, L., Iyer, R.R. et al. Real-time, high-resolution metabolic characterization of live bacteria using label-free optical metabolic imaging. npj Biofilms Microbiomes 12, 55 (2026). https://doi.org/10.1038/s41522-026-00920-0
Mots-clés: métabolisme bactérien, imagerie optique, biofilms, réponse aux antibiotiques, microbiome