Clear Sky Science · fr
La carence en fibres alimentaires aggrave l’inflammation intestinale via des vésicules extracellulaires intestinales enrichies en miR-6240
Pourquoi les fibres de votre alimentation comptent plus que vous ne le pensez
Un nombre croissant de personnes consomment des aliments fortement transformés dépourvus de fibres naturelles. Cette étude chez la souris explore ce que l’absence de ces fibres fait réellement au niveau intestinal. Elle montre qu’un régime pauvre en fibres n’affame pas seulement les microbes bienfaisants ; il déclenche aussi la libération de minuscules particules issues de la muqueuse intestinale qui reprogramment les cellules immunitaires et aggravent l’inflammation. Comprendre cette chaîne cachée d’événements aide à expliquer pourquoi les régimes modernes sont associés aux maladies intestinales et pourrait indiquer de nouvelles pistes thérapeutiques.
Des assiettes vides à un intestin en colère
Les chercheurs ont commencé par nourrir des souris soit avec un régime normal, soit avec un régime sans fibres pendant quatre semaines. Les souris privées de fibres ont rapidement montré des signes de dysfonctionnement intestinal : leurs côlons se sont raccourcis et détériorés, et la couche de mucus qui protège la surface intestinale s’est amincie. Au microscope, les tissus présentaient plus de lésions et moins de cellules productrices de mucus. Les analyses de sang et de côlon ont révélé des taux plus élevés de molécules pro-inflammatoires et des niveaux réduits de facteurs protecteurs et apaisants. Les cellules immunitaires intestinales ont basculé vers un état plus agressif, prêtes à l’attaque, et les jonctions moléculaires qui maintiennent l’intégrité des cellules intestinales se sont affaiblies, suggérant une barrière intestinale plus perméable.
Les microbes intestinaux portent le premier message
Parce que les fibres constituent une source alimentaire majeure pour les bactéries intestinales, l’équipe a aussi examiné comment la communauté microbienne changeait. Les souris sous régime sans fibres présentaient un mélange microbien remanié : des groupes utiles comme Bifidobacterium et Prevotella diminuaient, tandis que plusieurs espèces opportunistes ou consommatrices de mucus se développaient. Pour déterminer si les microbes seuls pouvaient provoquer la maladie, les scientifiques ont transféré le microbiote de souris privées de fibres ou de souris normales à de nouveaux animaux dont le microbiote avait été éliminé. Bien que ces nouveaux animaux aient tous reçu la même alimentation standard, ceux qui ont reçu les bactéries provenant des donneurs sans fibres ont développé des lésions coliques, une inflammation et des problèmes de barrière similaires aux animaux initialement privés de fibres. Cela a montré qu’un mode de vie pauvre en fibres peut « imprimer » un microbiote promoteur de maladie capable de transmettre des troubles intestinaux à d’autres.
De minuscules vésicules traduisent le signal alimentaire en perturbation immunitaire
L’étude s’est ensuite intéressée aux propres cellules de l’organisme. Les cellules de l’épithélium intestinal libèrent constamment des bulles de taille nanométrique appelées vésicules extracellulaires, qui véhiculent des messages moléculaires. Les auteurs ont isolé ces vésicules chez des souris normales et privées de fibres et les ont administrées à des animaux sains. Les vésicules issues d’intestins privés de fibres suffisaient à provoquer des lésions coliques, une perte de mucus, une augmentation des molécules inflammatoires et un affaiblissement des protéines de la barrière, sans changer le régime alimentaire des animaux. À l’intérieur de ces vésicules, l’équipe a identifié un profil distinct de petits ARN régulateurs, dont un en particulier — appelé miR-6240 — apparaissait fortement augmenté dans la condition pauvre en fibres. Lorsqu’on a introduit cet ARN unique dans des cellules immunitaires en culture, il les a poussées vers un profil plus inflammatoire et a indirectement endommagé les cellules intestinales voisines.
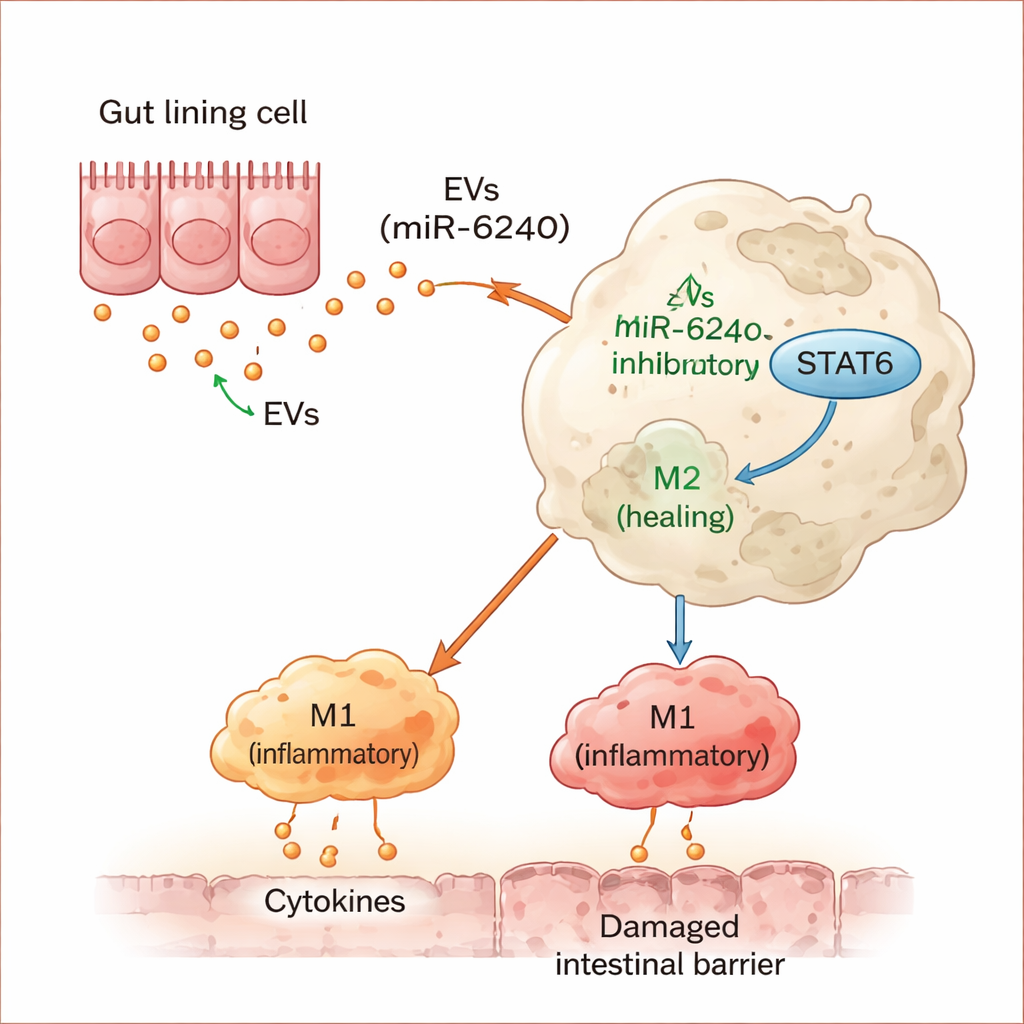
Un interrupteur moléculaire unique fait basculer l’équilibre immunitaire
En approfondissant, les chercheurs ont découvert que le miR-6240 cible directement une protéine appelée STAT6, qui aide normalement à orienter les macrophages — cellules immunitaires clés — vers un mode réparateur et de « nettoyage ». En atténuant STAT6, le miR-6240 bloque cette voie apaisante et oriente les macrophages vers une posture plus agressive et délétère pour les tissus. L’administration à des souris d’une forme synthétique de miR-6240 a reproduit de nombreuses caractéristiques de la carence en fibres dans leurs côlons, notamment l’inflammation, la perte de mucus et une barrière affaiblie. À l’inverse, bloquer le miR-6240 dans les cellules immunitaires a atténué les effets néfastes des vésicules provenant d’intestins sans fibres. Lorsque des macrophages préchargés en miR-6240 ont été transférés à des souris saines, ces réceptrices ont développé une inflammation intestinale, soulignant la puissance de ce signal unique.
Ce que cela signifie pour notre alimentation quotidienne
Pour le grand public, le message est clair : éviter les fibres ne change pas seulement les bactéries qui peuplent votre intestin ; cela modifie aussi la manière dont vos propres cellules intestinales communiquent avec le système immunitaire. Un régime pauvre en fibres reconfigure le microbiome et incite les cellules de la muqueuse intestinale à libérer des vésicules chargées en miR-6240, qui à leur tour inhibent un commutateur protecteur (STAT6) dans les cellules immunitaires et attisent l’inflammation. Si cet ARN particulier peut être spécifique à la souris, le principe général s’applique probablement plus largement : notre alimentation peut reprogrammer les messages moléculaires dans l’intestin qui déterminent s’il reste calme ou s’enflamme. Restaurer les fibres, ou cibler des voies moléculaires similaires, pourrait un jour aider à prévenir ou traiter les maladies intestinales liées à l’alimentation.
Citation: Song, M., Zhou, W., Fan, J. et al. Dietary fiber deficiency exacerbates intestinal inflammation via miR-6240-enriched gut extracellular vesicles. npj Biofilms Microbiomes 12, 53 (2026). https://doi.org/10.1038/s41522-026-00918-8
Mots-clés: fibres alimentaires, microbiote intestinal, inflammation intestinale, vésicules extracellulaires, microARN