Clear Sky Science · fr
Des nanocorps véhiculés par Lactobacillus améliorent la productivité des poulets de chair en présence d’entérite nécrosante subclinique avec modifications associées du microbiome et du transcriptome
Pourquoi la santé intestinale du poulet importe pour votre assiette
Les élevages de poulets modernes jouent les équilibristes : ils doivent produire des milliards d’oiseaux efficacement tout en réduisant les antibiotiques qui favorisent les infections résistantes aux médicaments chez l’humain. Une des menaces cachées les plus importantes pour les poulets de chair est une maladie intestinale appelée entérite nécrosante subclinique. Les oiseaux atteints paraissent souvent normaux mais croissent plus lentement et consomment plus d’aliment pour atteindre le même poids, augmentant silencieusement le coût et l’empreinte environnementale de la viande de poulet. Cette étude explore une nouvelle approche probiotique très ciblée qui arme des bactéries amies de petits fragments d’anticorps pour neutraliser les toxines pathogènes directement dans l’intestin.
Une maladie intestinale coûteuse et en grande partie invisible
L’entérite nécrosante est causée par la bactérie intestinale commune Clostridium perfringens lorsque celle-ci prolifère et libère de puissantes toxines. Dans sa forme sévère, la maladie tue des oiseaux et provoque des lésions intestinales évidentes. Mais la forme subclinique est beaucoup plus courante : des toxines comme NetB et la toxine alpha endommagent subtilement la muqueuse intestinale. Les oiseaux digèrent moins bien les aliments, prennent moins de poids, et montrent pourtant peu de signes externes de maladie. À l’échelle mondiale, cette perte silencieuse de productivité coûterait aux producteurs avicoles plus de 2 milliards de dollars par an. Historiquement, les élevages contrôlaient le problème avec des antibiotiques incorporés aux aliments, mais les inquiétudes croissantes concernant la résistance antimicrobienne et la demande des consommateurs pour du poulet « élevé sans antibiotiques » rendent ces médicaments moins acceptables, créant un besoin urgent d’alternatives précises et sans médicaments.
Transformer des probiotiques en bloqueurs de toxines ciblés
Les chercheurs se sont appuyés sur des travaux antérieurs où ils avaient modifié deux souches de la bactérie probiotique Limosilactobacillus reuteri pour sécréter des « nanocorps » — de très petits fragments d’anticorps — qui se lient à NetB ou à la toxine alpha et les neutralisent. Dans la nouvelle étude, ils ont testé si ces probiotiques conçus pouvaient améliorer les performances de poulets de chair confrontés à une forme légère et commercialement réaliste de la maladie. Sur un essai de 43 jours, plus de 2 000 oiseaux ont été répartis en quatre groupes : un groupe témoin soumis au défi ; un groupe recevant un antibiotique prophylactique courant (bacitracine méthylène disalicylate, BMD) ; un groupe recevant les souches productrices de nanocorps modifiées (appelées NE01 et NE06) ; et un groupe recevant les souches probiotiques parentales non modifiées. Tous les oiseaux ont été vaccinés contre la coccidiose puis exposés à C. perfringens pour déclencher une maladie subclinique.
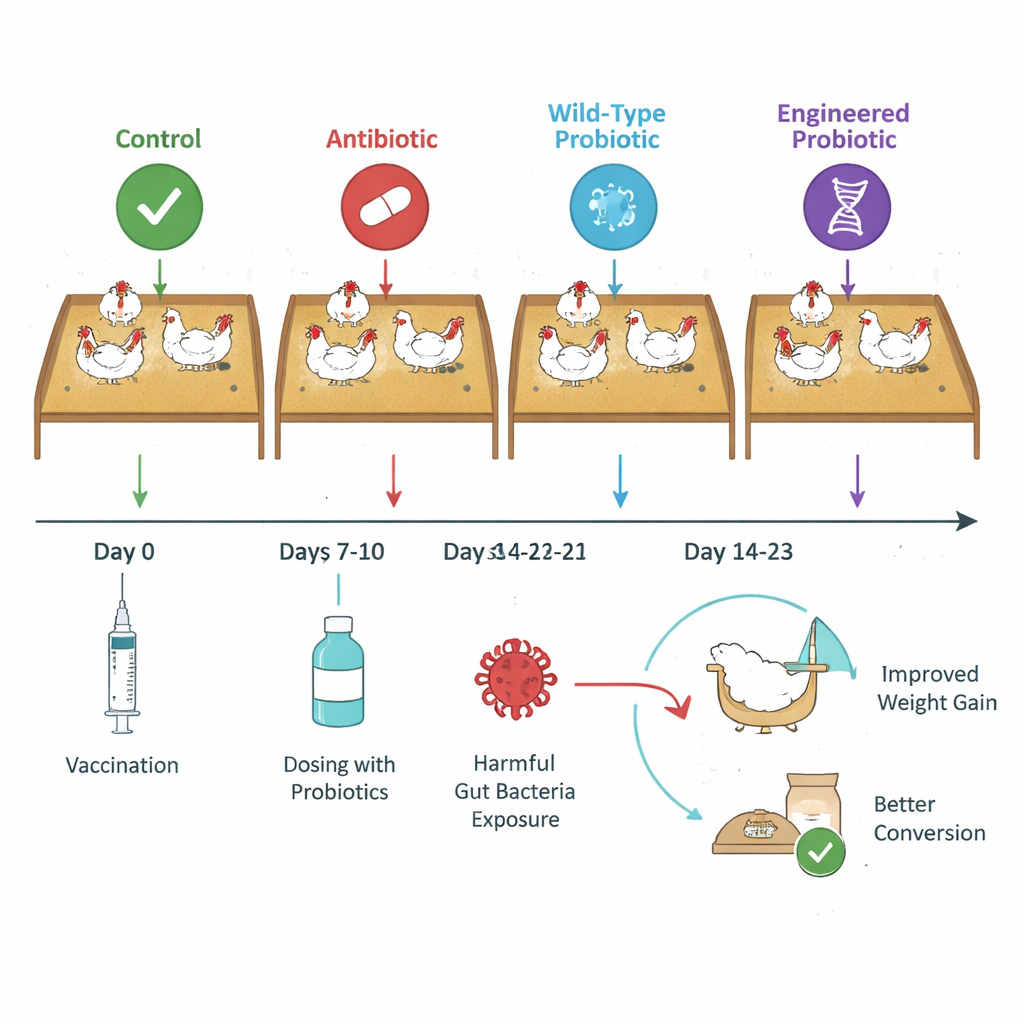
Meilleure croissance avec moins de coûts cachés
Les oiseaux ayant reçu les souches productrices de nanocorps ont converti l’aliment en poids corporel de manière systématiquement plus efficace que les autres groupes. Leur ratio de conversion alimentaire ajusté à la mortalité s’est amélioré de 4 à 7 « points » (0,04–0,07 unités) par rapport aux oiseaux non traités à différents moments, et ils étaient de 34 à 81 grammes plus lourds à la fin de l’étude comparés au groupe témoin, au groupe antibiotique ou aux oiseaux ayant reçu des probiotiques classiques. Fait intéressant, les mesures classiques de la maladie — telles que les lésions intestinales visibles et les dénombrements de C. perfringens dans les fèces et le contenu cæcal — montraient seulement de légères différences entre les traitements. Cela signifie que tous les oiseaux subissaient un niveau similaire de défi de faible intensité, mais que le groupe nanocorps y faisait face beaucoup plus efficacement, transformant la même quantité d’aliment en plus de viande.
Microbiomes plus calmes et systèmes immunitaires moins sollicités
Pour comprendre pourquoi les performances s’amélioraient, l’équipe a regardé au-delà de la pathologie macroscopique et examiné le microbiome et l’activité génique dans l’intestin et le foie. L’analyse métatranscriptomique du contenu jéjunal (intestin grêle) a montré que les oiseaux recevant les souches modifiées avaient plus de transcrits de L. reuteri et une expression détectable des gènes des nanocorps, confirmant que les probiotiques survivaient dans l’intestin et produisaient leurs molécules bloquant les toxines. La composition microbienne globale évoluait principalement avec l’âge des oiseaux plutôt qu’avec le traitement, mais le groupe nanocorps présentait moins de variabilité d’un échantillon à l’autre, suggérant une communauté intestinale plus stable et résiliente. Sur le plan fonctionnel, les microbes intestinaux de ce groupe exprimaient davantage de gènes liés à la fermentation et à la synthèse protéique et moins de gènes associés à la respiration et à l’utilisation du nitrate — des profils liés à un environnement moins enflammé. Les chercheurs ont également observé une augmentation de l’expression des enzymes produisant un composé appelé 2,3-butanediol, qui présente des effets anti-inflammatoires dans des modèles animaux.
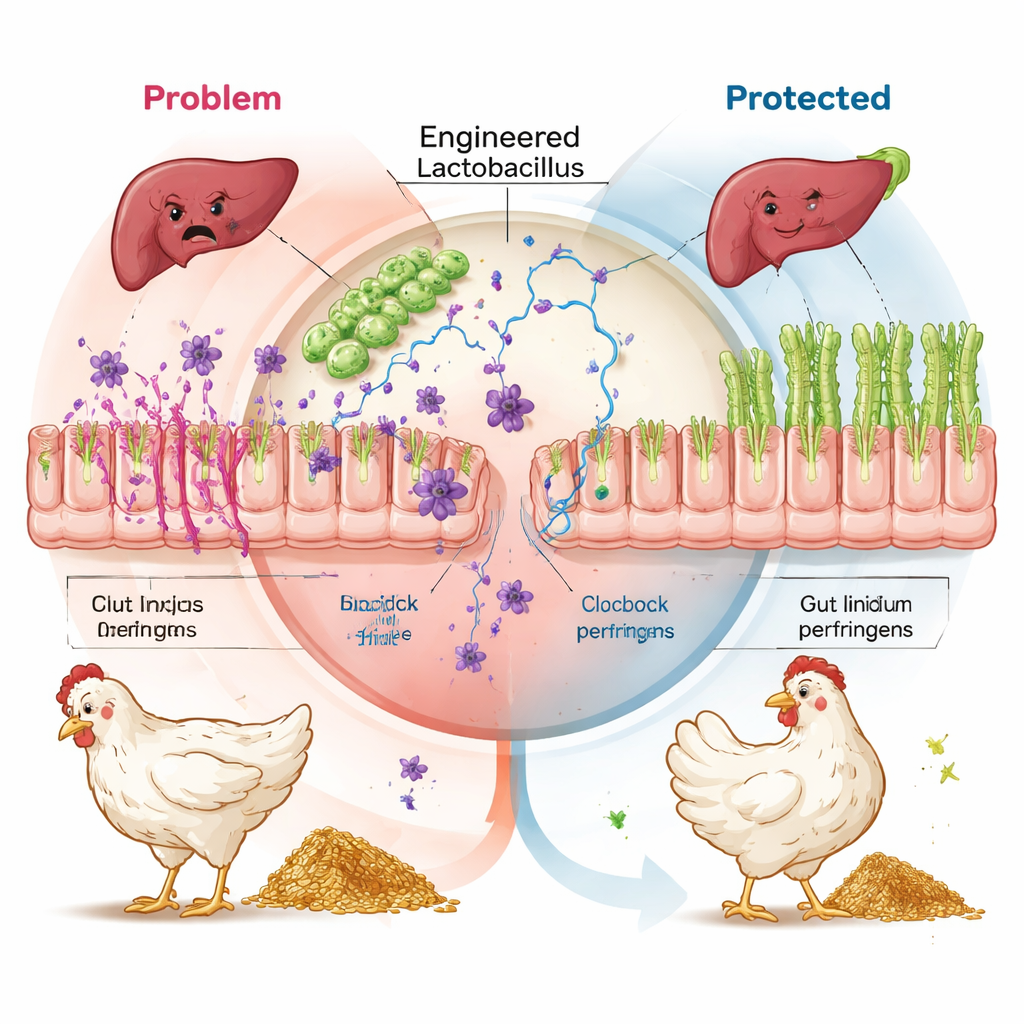
Protection des organes distants et amélioration de l’efficacité
L’histoire s’étendait au-delà de l’intestin. L’expression génique dans le jéjunum et le foie a révélé que les oiseaux ayant reçu les probiotiques modifiés présentaient une activation nettement plus faible des voies immunitaires et de stress oxydatif comparé aux témoins soumis au défi, et dans de nombreux cas comparé aux groupes antibiotique et probiotiques classiques. Dans le foie — un organe qui subit des dommages collatéraux dus aux toxines bactériennes — le groupe nanocorps montrait une réduction de la signalisation via les voies de l’insuline et de mTOR connues pour s’activer lors de blessures induites par les toxines, tout en renforçant les voies antioxydantes et génératrices d’énergie. Pris ensemble, ces résultats suggèrent que la neutralisation de NetB et de la toxine alpha à la surface intestinale prévient une cascade d’inflammation et de lésions tissulaires, épargnant à l’oiseau les lourds coûts métaboliques d’une lutte permanente contre des infections cachées.
Ce que cela signifie pour la santé future des poulets et des humains
Pour un lecteur général, le message clé est que tous les « probiotiques » ne se valent pas. En équipant des bactéries utiles de nanocorps précisément ciblés, les chercheurs ont créé une thérapie vivante qui protège les poulets contre une maladie intestinale commune et largement invisible sans recourir aux antibiotiques traditionnels — et qui a surpassé à la fois un régime antibiotique et des probiotiques standards. Les oiseaux ont consommé moins d’aliment pour atteindre le poids commercial, avec moins de signes de stress interne. Si des stratégies similaires peuvent être étendues à d’autres animaux d’élevage, et éventuellement à l’humain, les probiotiques modifiés pourraient offrir un moyen puissant de désarmer les toxines intestinales nocives tout en préservant les microbes bénéfiques et en ralentissant la propagation de la résistance aux antibiotiques.
Citation: Hall, A.N., Manuja, S., Payling, L.M. et al. Lactobacillus-vectored nanobodies improve broiler productivity under sub-clinical necrotic enteritis with associated microbiome and transcriptome changes. npj Biofilms Microbiomes 12, 52 (2026). https://doi.org/10.1038/s41522-026-00916-w
Mots-clés: probiotiques génétiquement modifiés, entérite nécrosante, santé intestinale de la volaille, nanocorps, alternatives aux antibiotiques