Clear Sky Science · fr
Modulation immunitaire dirigée par le microbiote buccal le long de l’axe bouche–intestin : des signaux locaux à l’inflammation systémique
Pourquoi votre bouche compte pour tout votre corps
Les bactéries qui vivent dans la bouche font bien plus que provoquer des caries ou mauvaise haleine. Cet article de synthèse explique comment les microbes buccaux peuvent descendre jusqu’à l’intestin, perturber ses défenses délicates et contribuer à déclencher une inflammation qui atteint des organes comme le foie et le cerveau. Comprendre cet « axe bouche–intestin » caché apporte de nouvelles pistes sur des problèmes courants allant de la stéatose hépatique à la maladie d’Alzheimer, et souligne des mesures étonnamment simples — comme une meilleure hygiène dentaire et une alimentation adaptée — qui peuvent protéger la santé globale.
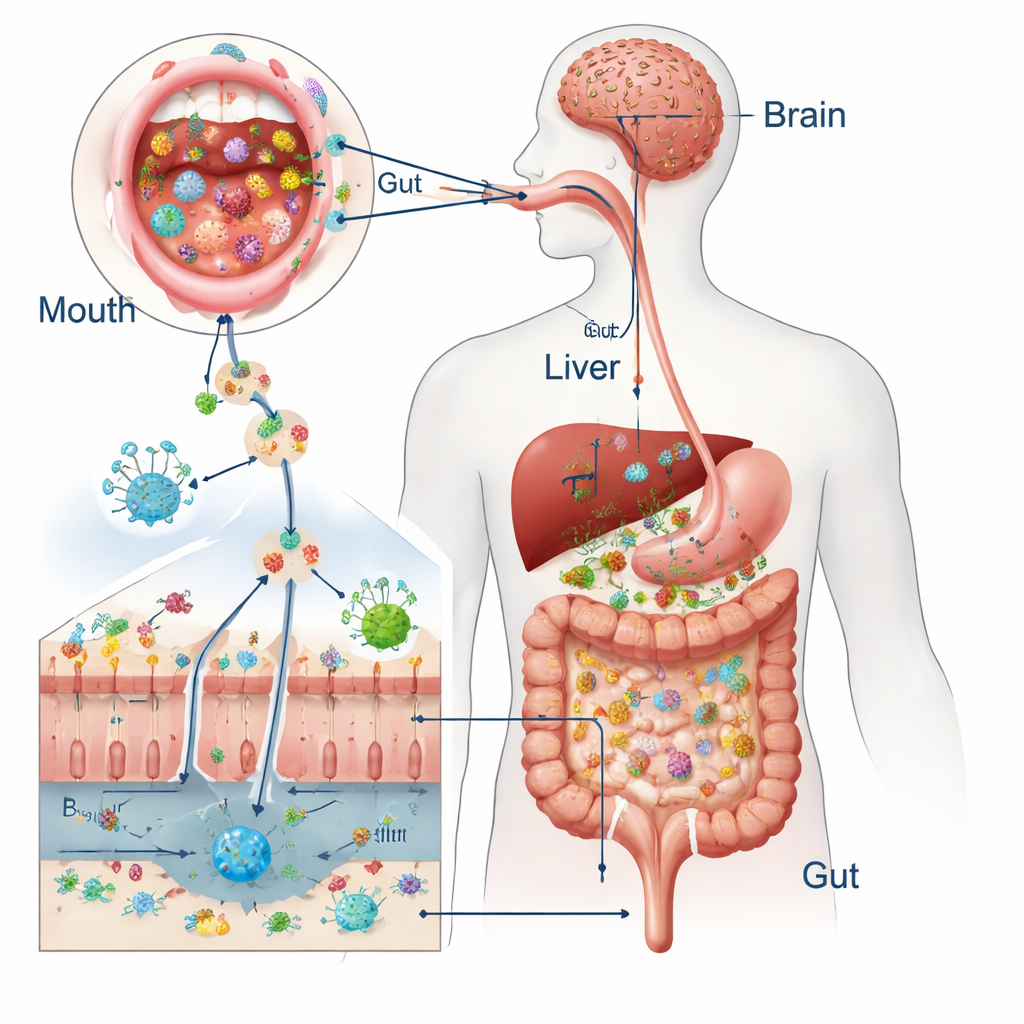
Du déglutissement aux effets systémiques
Chaque jour, nous avalons environ un litre et demi de salive remplie de milliards de microbes buccaux. Chez les personnes en bonne santé, des défenses robustes — les agents antimicrobiens naturels de la salive, l’acidité gastrique, la bile, le mucus visqueux et des jonctions serrées entre les cellules intestinales — empêchent la plupart de ces visiteurs de s’installer. Les études comparant les germes de la bouche et des selles montrent que seule une infime fraction des microbes intestinaux provient directement de la bouche lorsque tout fonctionne bien. Mais les deux écosystèmes se recoupent suffisamment pour que des espèces orales comme Streptococcus et Veillonella soient parfois détectées dans l’intestin, ce qui pose la question de savoir quand elles deviennent plus que de simples passagères inoffensives.
Quand les barrières se détériorent
La situation change sous l’effet du stress. Le vieillissement, la sécheresse buccale, une mauvaise hygiène dentaire et les maladies parodontales chroniques peuvent surcharger la bouche de bactéries nocives. Des médicaments tels que les antibiotiques et les antiacides affaiblissent les défenses intestinales en amincissant le mucus, en desserrant les jonctions entre cellules et en permettant à davantage de microbes de survivre au passage par l’estomac. Les infections buccales et les interventions dentaires peuvent même propulser des bactéries dans le sang. La revue met également en avant les vésicules extracellulaires bactériennes — de « paquets » nanosize émis par les microbes — qui peuvent traverser les tissus et porter des signaux inflammatoires loin de leur point d’origine. Certaines bactéries orales, comme Porphyromonas gingivalis et Fusobacterium nucleatum, s’abritent même à l’intérieur de cellules immunitaires et se déplacent dans l’organisme comme un « cheval de Troie » microbien.
Comment les bactéries buccales apprennent à vivre dans l’intestin
Toutes les bactéries buccales qui atteignent l’intestin ne peuvent pas s’y maintenir. Celles qui y parviennent possèdent souvent des astuces de survie particulières. Certains souches remodèlent leur membrane cellulaire pour résister à l’acidité ou à la bile ; d’autres exploitent les sucres du mucus qui tapisse la paroi intestinale ou s’associent aux bactéries résidentes pour former des biofilms adhésifs. En parallèle, elles apprennent à passer sous le radar du système immunitaire. Certaines bloquent la capacité létale des cellules NK et des lymphocytes T ; d’autres interfèrent avec des capteurs d’alerte précoces qui détectent normalement des composants microbiens et déclenchent des réponses protectrices. En poussant l’équilibre des cellules immunitaires vers des phénotypes plus inflammatoires et en réduisant les « freins » régulateurs, elles créent un créneau où une colonisation durable et de faible intensité devient possible.
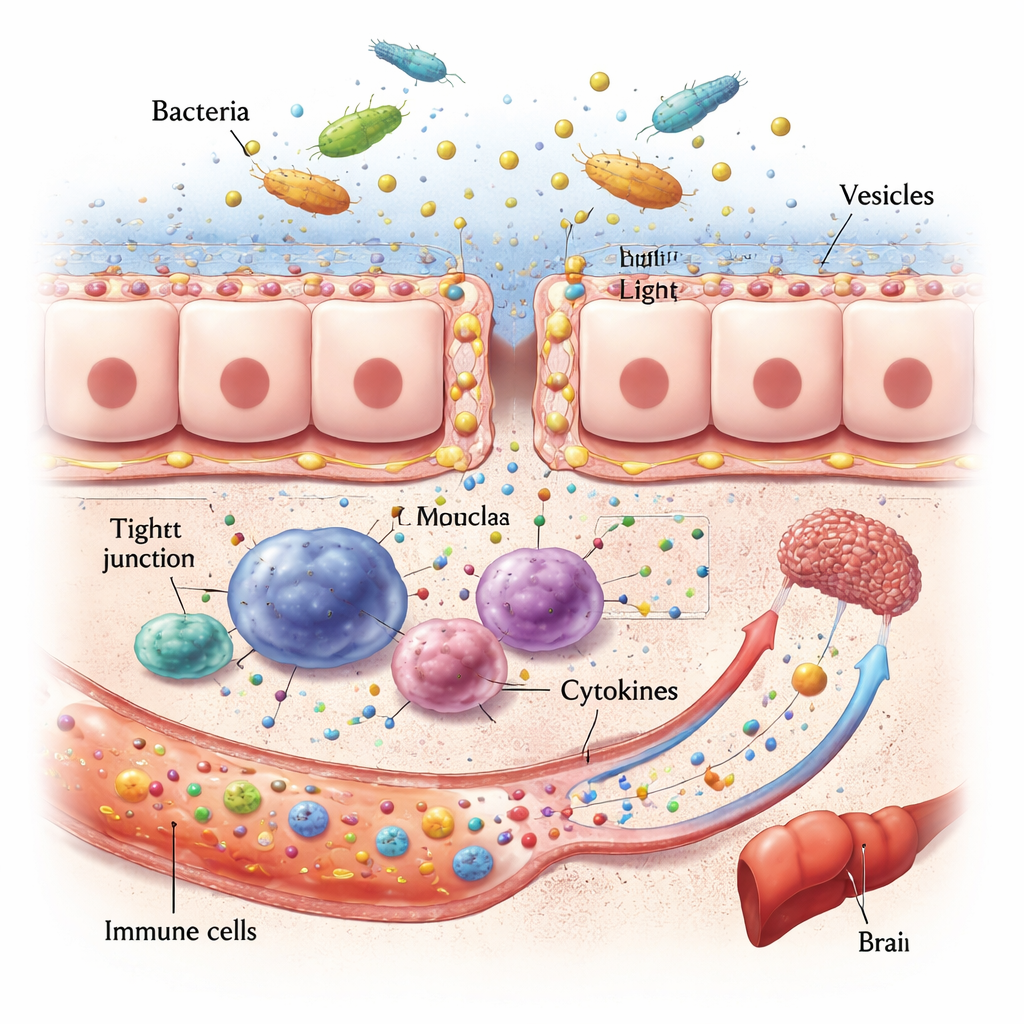
Du syndrome de l’intestin perméable aux organes malades
Une fois installées, les microbes oraux envahissants et leurs vésicules peuvent endommager la première ligne de défense intestinale. Ils dégradent les protéines qui scellent les cellules voisines, amincissent la couche de mucus et peuvent même tuer directement les cellules intestinales. Cela rend la paroi intestinale plus perméable, permettant à des fragments bactériens et à des toxines de s’infiltrer dans la circulation sanguine. Là, ils activent des cellules immunitaires et déclenchent des salves de molécules de signalisation appelées cytokines. Parce que le sang intestinal rejoint directement le foie, cet organe est particulièrement exposé : des données animales et humaines relient les agents pathogènes buccaux à la stéatose hépatique, à la fibrose et à une aggravation de l’inflammation. Des voies similaires relient la dysbiose buccale et la perturbation intestinale au cerveau, où une inflammation chronique et des métabolites microbiaux altérés semblent favoriser l’accumulation de protéines associées à Alzheimer et perturber l’humeur et la cognition.
Nouvelles voies d’intervention
Reconnaître l’axe bouche–intestin ouvre des stratégies multiniveaux de prévention et de traitement. Au niveau buccal, les soins parodontaux de routine, les thérapies photodynamiques et des peptides antimicrobiens naturels peuvent réduire les bactéries nuisibles et diminuer le nombre de microbes qui atteignent l’intestin. Dans l’intestin, les probiotiques, les régimes riches en fibres et les compléments qui restaurent les acides gras à chaîne courte aident à reconstruire la barrière intestinale et à apaiser une immunité hyperactive. À l’avenir, des dispositifs sophistiqués « organe-sur-puce » reliant de mini tissus de la bouche, de l’intestin, du foie et du cerveau, associés à des cartographies massives des microbes et des réactions immunitaires qu’ils provoquent, pourraient permettre des approches personnalisées pour prévenir les maladies inflammatoires chroniques.
Ce que cela signifie pour vous
Pour un lecteur non spécialiste, le message central est que la bouche n’est pas un compartiment isolé : ses microbes peuvent façonner la santé intestinale et, via l’intestin, influencer l’ensemble du corps. Lorsque les bactéries buccales contournent ou érodent les barrières naturelles, elles peuvent contribuer à une inflammation durable dans des organes aussi éloignés que le foie et le cerveau. L’article conclut que protéger la santé buccale, préserver la barrière intestinale et orienter en douceur nos communautés microbiennes avec des traitements ciblés pourraient devenir des outils importants pour combattre les maladies chroniques modernes.
Citation: Li, C., Fan, Y. & Chen, X. Oral microbiota–driven immune modulation along the oral–gut axis: from local signals to systemic inflammation. npj Biofilms Microbiomes 12, 46 (2026). https://doi.org/10.1038/s41522-026-00912-0
Mots-clés: microbiome buccal, barrière intestinale, inflammation systémique, maladie du foie, santé du cerveau