Clear Sky Science · fr
Une thérapie antibiotique améliorée par des enzymes réduit les biofilms à des niveaux indétectables dans un modèle d’infection associée à un implant
Pourquoi les infections d’implants tenaces comptent
Les remplacements de hanche et de genou transforment des vies, mais lorsque des bactéries colonisent ces implants métalliques, elles peuvent former des communautés visqueuses appelées biofilms. Ces biofilms fonctionnent comme des cités blindées qui protègent les germes à la fois du système immunitaire et des antibiotiques, entraînant des infections douloureuses et durables, très difficiles à éradiquer. Cette étude explore un nouveau traitement à deux volets qui aide d’abord à démanteler les défenses du biofilm, puis inonde la zone de fortes doses d’antibiotiques — une approche qui pourrait un jour permettre de sauver davantage d’implants plutôt que de les remplacer.
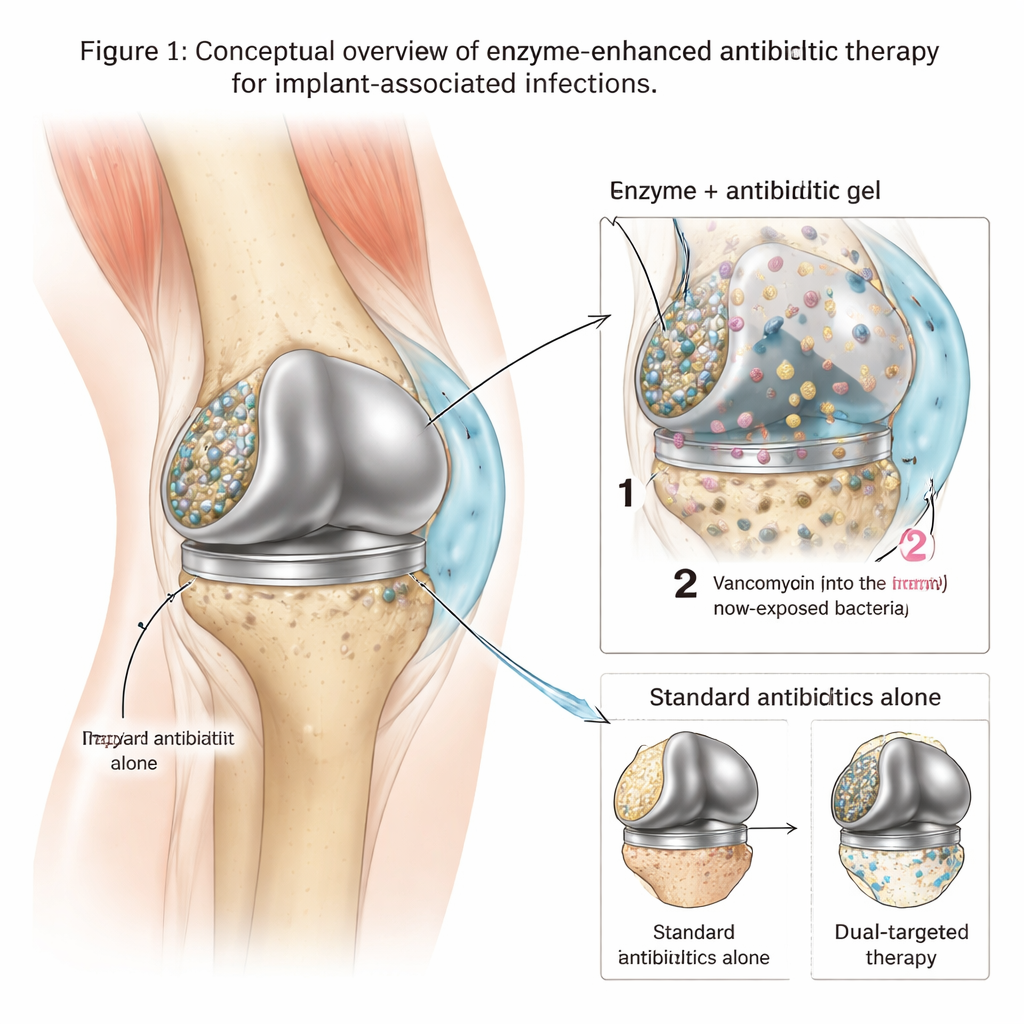
Les bastions cachés sur les implants métalliques
Quand des bactéries comme le Staphylococcus aureus résistant à la méticilline (SARM) adhèrent à une articulation artificielle, elles construisent rapidement une matrice adhésive composée d’ADN, de sucres et d’autres molécules sur la surface métallique. À l’intérieur de ce biofilm protecteur, les bactéries se développent lentement, modifient leur comportement et peuvent tolérer des niveaux d’antibiotiques des centaines voire des milliers de fois supérieurs à ceux qui tuent des germes en suspension. Par conséquent, les traitements standard — même des antibiotiques puissants comme la vancomycine — échouent souvent à éliminer complètement l’infection, contraignant les patients à subir des chirurgies répétées ou le remplacement total de l’implant. Les médecins ont besoin d’outils qui non seulement tuent les bactéries, mais brisent aussi leur forteresse protectrice pour que les médicaments puissent atteindre leur cible.
Un gel intelligent qui délivre enzymes et antibiotiques
Les chercheurs ont conçu un traitement local reposant sur un hydrogel thermosensible à base d’un composé appelé poloxamère 407. Ce gel est liquide quand il est froid, ce qui le rend facile à injecter autour d’un implant, puis devient rapidement un solide mou à la température corporelle, ce qui l’aide à rester en place. Dans ce gel, l’équipe a incorporé deux ingrédients clés : un antibiotique puissant (la vancomycine) et un cocktail de trois enzymes qui dégradent les composants majeurs de la matrice du biofilm. En laboratoire, ils ont ajusté le gel de sorte que les enzymes soient libérées en premier — assouplissant et amincissant le biofilm — tandis que la vancomycine est diffusée plus lentement sur plusieurs jours, maintenant des concentrations locales très élevées exactement là où résident les bactéries.
Des boîtes de Pétri aux cobayes
Pour vérifier l’efficacité de la stratégie, l’équipe l’a d’abord testée sur des biofilms cultivés sur des pièces de titane en laboratoire, puis dans un modèle de cobaye mimant des implants infectés. In vitro, deux applications du gel enzyme‑antibiotique, espacées de 48 heures, ont réduit le nombre de bactéries vivantes sur les surfaces métalliques de plus de 100 000 fois et ont presque anéanti la masse du biofilm. Chez les animaux, les chercheurs ont placé chirurgicalement sous la peau des cages perforées contenant des billes de titane, les ont infectées par SARM, puis les ont traitées avec différentes combinaisons d’antibiotiques systémiques et de gels locaux. Le schéma le plus efficace associait : (1) le gel local contenant à la fois les enzymes et la vancomycine, administré deux fois, et (2) un traitement systémique par vancomycine associé à un second antibiotique, la rifampicine, particulièrement efficace pour pénétrer les biofilms.
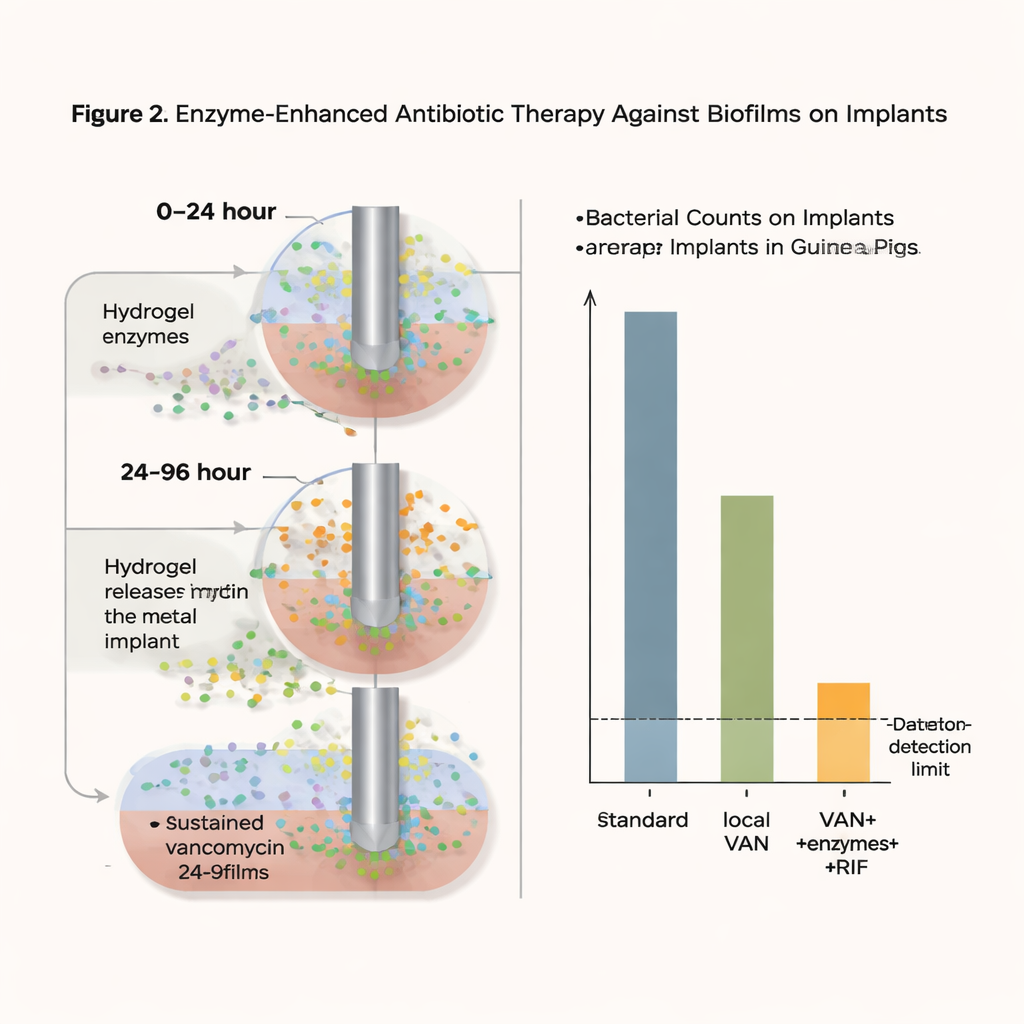
Ce que la nouvelle approche a accompli
Avec cette stratégie intensive mais localisée, le nombre de bactéries sur le matériau d’implant est tombé jusqu’à la limite de détection — effectivement « aucune bactérie récupérable » dans ce modèle — dans 75 % des cages traitées un jour après la fin de la thérapie, et dans 37,5 % des cas même cinq jours plus tard. Fait important, aucune augmentation de la résistance à la vancomycine n’a été observée, et des niveaux locaux élevés de vancomycine semblent avoir empêché l’émergence de souches résistantes à la rifampicine. Des tests de sécurité sur des cellules cultivées et un modèle de peau humaine reconstituée n’ont montré aucun signe de toxicité ou d’irritation dû aux formulations de gel. Bien qu’une légère repousse bactérienne soit survenue dans certains cas et que la période de traitement ait été plus courte que celle généralement administrée aux patients, les résultats montrent que la combinaison d’enzymes perturbant le biofilm et d’une délivrance locale soutenue d’antibiotique peut réduire considérablement des infections par ailleurs tenaces.
Ce que cela pourrait signifier pour les patients
Pour les personnes confrontées à des infections liées à un implant, ce travail ouvre la voie à un avenir où les chirurgiens pourraient injecter un gel intelligent autour d’une articulation infectée, plutôt que d’enlever ou remplacer immédiatement l’implant. En affaiblissant d’abord le bouclier du biofilm puis en inondant la zone de doses élevées et soutenues d’antibiotiques — soutenues par un traitement systémique — cette stratégie à double ciblage vise à faire tomber le nombre de bactéries à des niveaux indétectables et à réduire le risque de résistance. Bien que des études supplémentaires, des traitements plus longs et des essais cliniques restent nécessaires, l’approche offre une feuille de route prometteuse pour transformer certaines des infections orthopédiques les plus persistantes en problèmes plus gérables, et potentiellement curables.
Citation: Buzisa Mbuku, R., Poilvache, H., Maigret, L. et al. Enzymes-enhanced antibiotic therapy reduces biofilms to undetectable levels in an implant-associated infection model. npj Biofilms Microbiomes 12, 44 (2026). https://doi.org/10.1038/s41522-026-00910-2
Mots-clés: infection par biofilm, implants orthopédiques, vancomycine, thérapie enzymatique, rifampicine