Clear Sky Science · fr
Exploration théorique de protocoles pour traiter les infections des articulations prothétiques par des combinaisons d’antibiotiques et de bactériophages
Pourquoi les infections d’implants articulaires sont importantes
Les remplacements de la hanche et du genou ont transformé la vie de millions de personnes en leur permettant de marcher sans douleur. Mais lorsque des bactéries colonisent ces articulations artificielles, elles peuvent former des communautés visqueuses appelées biofilms qui adhèrent solidement aux surfaces métalliques et plastiques. Une fois qu’un biofilm est établi, les doses habituelles d’antibiotiques et les défenses immunitaires peinent souvent à l’éliminer, entraînant parfois la nécessité d’interventions chirurgicales supplémentaires. Cette étude se demande si l’ajout de virus ciblant spécifiquement les bactéries — appelés bactériophages, ou phages — aux antibiotiques standard peut offrir une approche plus efficace pour traiter ces infections tenaces.
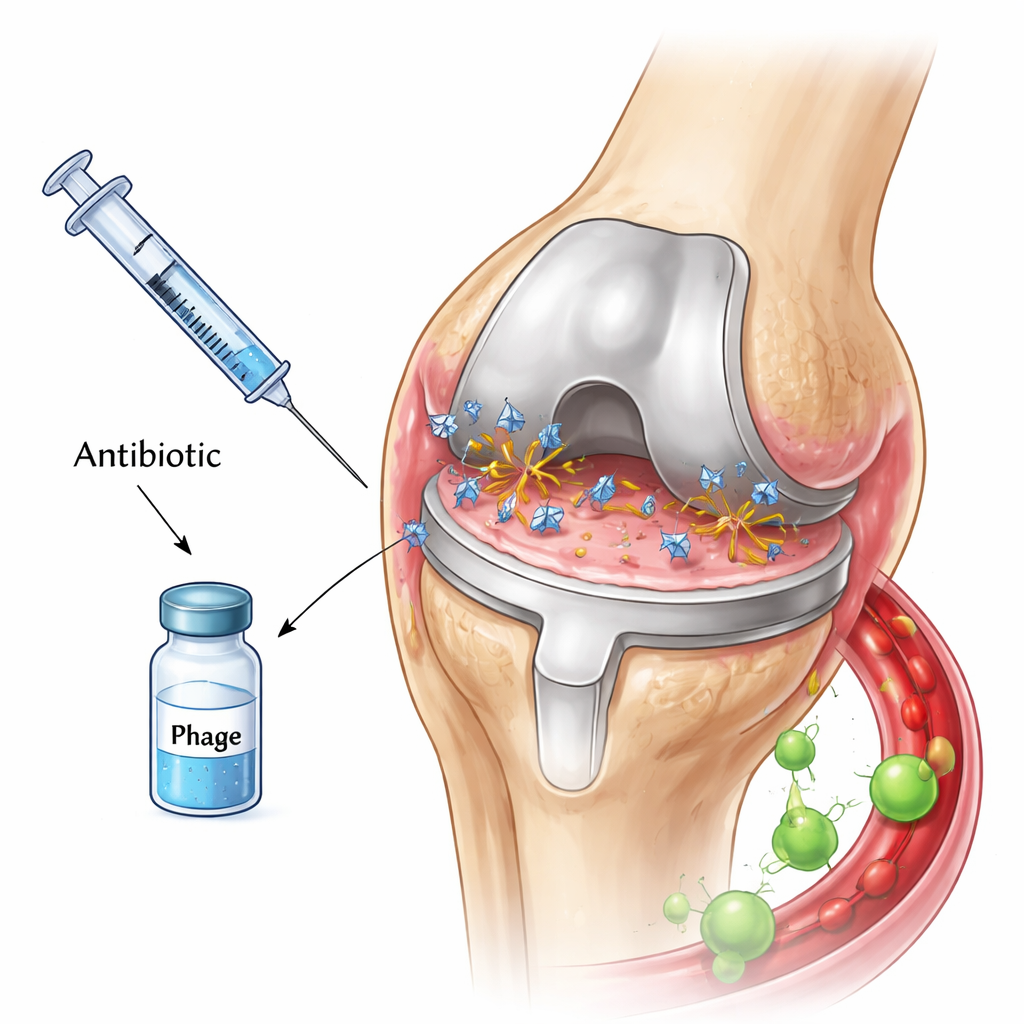
De petits virus qui traquent les bactéries
Les phages sont des prédateurs naturels des bactéries. Ils s’attachent à une cellule bactérienne, injectent leur matériel génétique, transforment la cellule en usine à virus, puis la font éclater, libérant une cohorte de nouveaux phages. Certains phages transportent aussi des enzymes capables de dégrader la matrice visqueuse entourant les biofilms, ouvrant potentiellement des couches protectrices qui protègent les bactéries des médicaments. À cause de ces propriétés, de nombreux chercheurs ont émis l’hypothèse que la combinaison de phages et d’antibiotiques pourrait constituer un double coup puissant contre les infections de prothèse articulaire, en particulier lorsque les bactéries deviennent résistantes aux médicaments.
Construire des infections à l’intérieur d’un ordinateur
Plutôt que de passer directement aux expériences animales ou aux essais cliniques, les auteurs ont d’abord construit un modèle mathématique et informatique détaillé d’une infection de prothèse articulaire. Leur système virtuel comportait deux zones principales : des bactéries en suspension dans les fluides corporels et des bactéries intégrées dans un biofilm à la surface de l’implant. Le modèle suivait également les cellules immunitaires, les nutriments favorisant la croissance bactérienne, les antibiotiques et les phages, tous entrant et sortant de l’articulation. En modifiant des conditions telles que la dose de médicament, le timing et la présence de bactéries résistantes aux antibiotiques, ils ont pu explorer de nombreuses stratégies de traitement difficiles, longues ou coûteuses à tester chez de vrais patients.
Quand les médicaments agissent seuls et ensemble
Les simulations ont montré que ni le système immunitaire ni les antibiotiques seuls n’éliminaient facilement les infections de biofilm. Les antibiotiques réduisaient fortement les bactéries en suspension mais n’affectaient guère la population du biofilm. Les phages pouvaient initialement mieux contrôler l’infection, mais ils introduisaient des cycles d’explosion et d’effondrement : lorsque les phages tuaient les bactéries, leurs proies devenaient trop rares, entraînant la baisse du nombre de phages et la reprise de la croissance bactérienne. Lorsque les antibiotiques et les phages étaient administrés simultanément, l’antibiotique tendait à dominer l’issue, et l’ajout de phages n’apportait souvent pas beaucoup plus que ce que l’antibiotique pouvait accomplir seul.
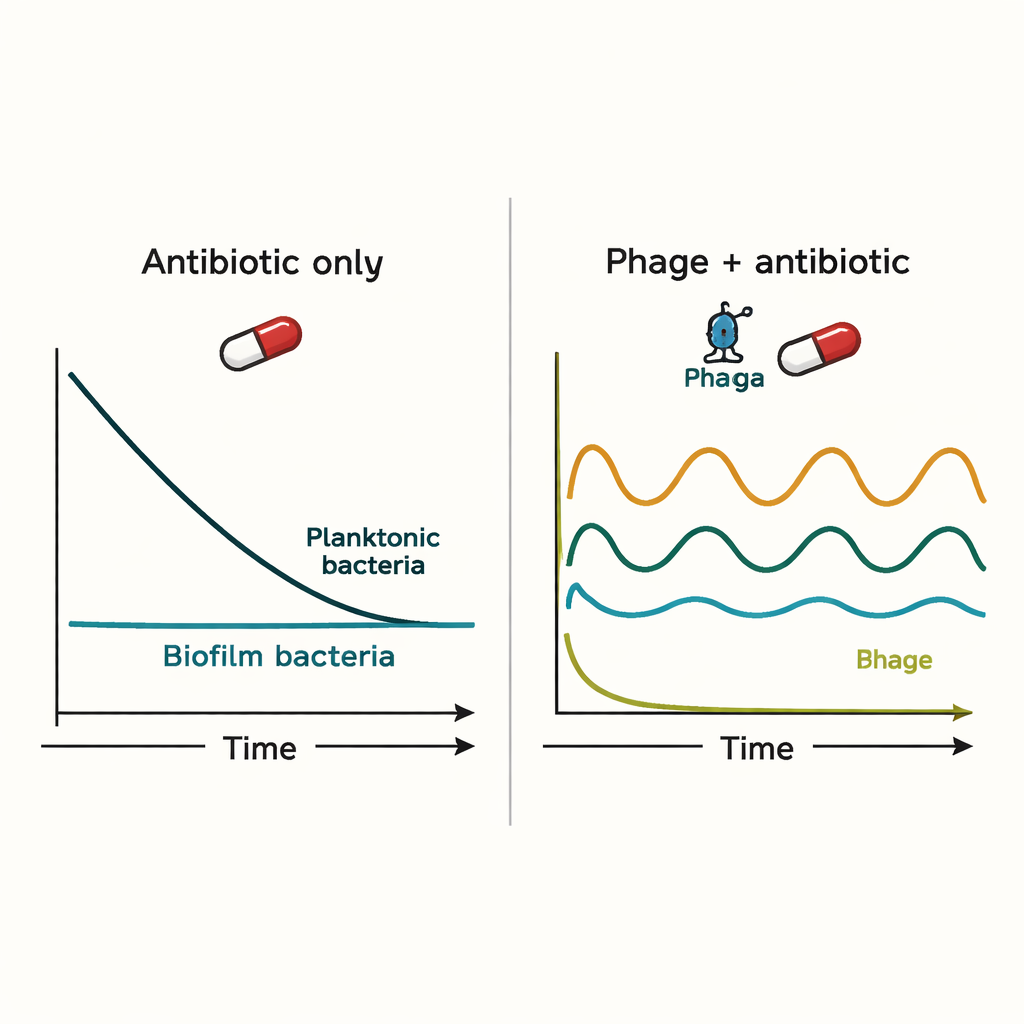
Le rôle particulier du timing et de la résistance
Le modèle devint plus optimiste lorsque des bactéries résistantes aux antibiotiques furent incluses. Les phages pouvaient attaquer ces cellules résistantes, parfois les éliminant complètement. Si le traitement par phages était commencé en premier et que les antibiotiques étaient ajoutés quelques heures plus tard, la stratégie combinée réduisait les bactéries en suspension de plusieurs ordres de grandeur et éliminait les sous-populations résistantes dans les simulations. Pourtant, les bactéries associées au biofilm n’étaient pas complètement éradiquées ; leurs effectifs restaient à des niveaux plus faibles, susceptibles d’être mieux gérés par le système immunitaire. Cela suggère que les phages sont peut-être plus utiles non pas comme des solutions miraculeuses, mais comme des aides qui préviennent la résistance et maintiennent les infections sous contrôle.
Ce que cela signifie pour les patients et les médecins
Pour les personnes confrontées à une prothèse articulaire infectée, ce travail apporte à la fois prudence et espoir. Le modèle suggère que l’ajout simple de phages aux antibiotiques standard est peu susceptible de guérir à lui seul des infections profondes de biofilm. Cependant, les phages peuvent rester des outils précieux : ils peuvent aider à éliminer les bactéries résistantes aux antibiotiques et à réduire le nombre total d’agents infectieux suffisamment pour que l’organisme puisse les contrôler, en particulier s’ils sont utilisés avant ou en synchronisation réfléchie avec les antibiotiques. Les auteurs insistent sur le fait qu’il s’agit de prédictions théoriques, non de preuves cliniques. Leur message principal est que des expériences ciblées — guidées par des modèles comme celui-ci — sont nécessaires pour déterminer quand la thérapie par phages peut réellement améliorer les résultats pour les patients atteints d’infections de prothèse articulaire.
Citation: Levin, B.R., Gil-Gil, T., Berryhill, B.A. et al. A theoretical exploration of protocols for treating prosthetic joint infections with combinations of antibiotics and bacteriophage. npj Biofilms Microbiomes 12, 51 (2026). https://doi.org/10.1038/s41522-025-00908-2
Mots-clés: infection de prothèse articulaire, biofilm, thérapie par bactériophages, résistance aux antibiotiques, modélisation mathématique