Clear Sky Science · fr
Étapes de formation des condensats biomoléculaires dans l’assemblage du pro‑β‑carboxysome
Pourquoi ces petites usines à carbone comptent
Les réseaux alimentaires terrestres dépendent de la photosynthèse, et pourtant l’enzyme clé qui capture le dioxyde de carbone (CO2) de l’air, la Rubisco, est lente et facilement perturbée par l’oxygène. Les cyanobactéries — microbes microscopiques et photosynthétiques — ont résolu ce problème il y a longtemps en construisant des « micro‑usines » protéiques appelées carboxysomes qui concentrent le CO2 autour de la Rubisco. Cette étude dévoile comment un complexe adaptateur crucial, composé de protéines nommées ApN et CM, s’auto‑assemble par étapes pour aider à construire un carboxysome fonctionnel. Comprendre cette chorégraphie pourrait guider les efforts visant à installer des systèmes similaires de concentration du CO2 dans les plantes cultivées afin d’augmenter les rendements.
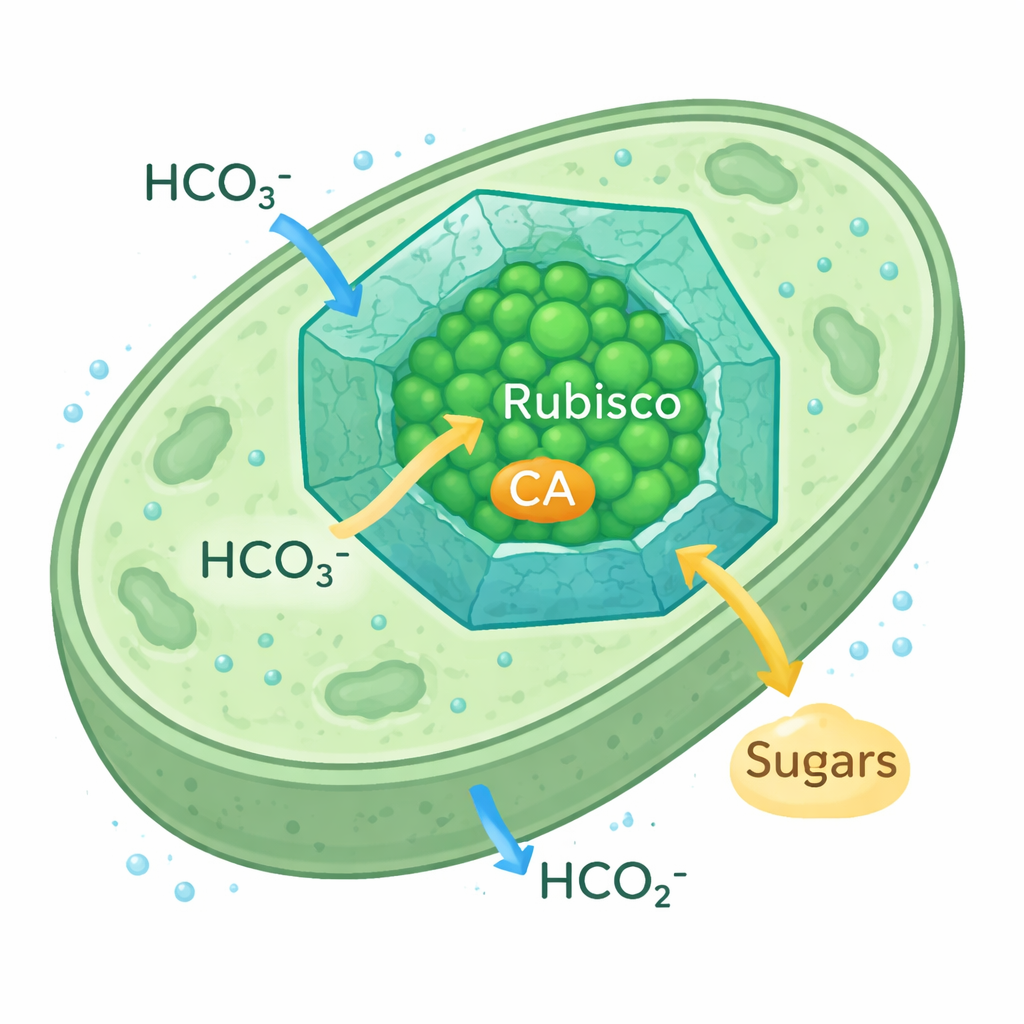
Comment les microbes améliorent la capture du carbone
Les carboxysomes cyanobactériens sont de petits compartiments protéiques icosaédriques présents à l’intérieur de la cellule. Leur coque protéique laisse entrer les ions bicarbonate tout en ralentissant la fuite du CO2, créant une bulle riche en CO2 autour de la Rubisco et de son enzyme partenaire, l’anhydrase carbonique (CA), qui convertit le bicarbonate en CO2. Ce mécanisme de concentration du CO2 permet aux cyanobactéries de prospérer même lorsque le CO2 environnemental est rare. Comme la forme de Rubisco utilisée dans ces carboxysomes ressemble à celle des plantes, les chercheurs les considèrent comme un modèle réaliste pour ré‑ingénier l’appareil des chloroplastes végétaux afin d’améliorer la capture du carbone.
La pièce du puzzle qui communique avec la coque
Avant la formation de la coque protéique rigide, les cyanobactéries construisent d’abord un condensat mou en forme de goutte appelé « pro‑carboxysome ». Des travaux antérieurs ont montré qu’une protéine échafaudage nommée CM rassemble la Rubisco et la CA dans cette goutte. Il manquait le lien expliquant comment la protéine adaptatrice de la coque ApN rejoint cette structure puis s’y connecte pour lier la coque. Les auteurs ont constaté que lorsque ApN est produite seule, elle forme un tétramère qui n’interagit pas avec les autres composants du carboxysome. À l’état isolé, ApN ne peut pas être entraînée dans les gouttes avec la Rubisco, la CM et la CA, ce qui suggère qu’une autre forme d’ApN est utilisée lors de l’assemblage réel du carboxysome.
Adaptateurs co‑construits et un commutateur redox
En examinant l’organisation génétique chez les cyanobactéries, l’équipe a remarqué que apn se trouve directement après cm dans le même opéron, de sorte que les deux protéines sont généralement synthétisées ensemble. En reproduisant cela dans des bactéries modèles, ils ont co‑exprimé ApN et CM à partir d’un même fragment d’ADN. Dans ces conditions, ApN n’a plus formé de tétramère autonome. À la place, trois sous‑unités d’ApN et une sous‑unité de CM s’assemblèrent en un complexe adaptateur spécifique en quatre parties, noté (ApN)3:CM. Cet hétéro‑complexe se lia facilement à la Rubisco, à la CA et à la CM et pouvait rejoindre les condensats. La modélisation structurale et la cryo‑microscopie électronique montrèrent que ApN et CM se rencontrent via une interface « langue‑et‑rainure » finement ajustée ; lorsque des résidus clés d’ApN dans cette interface furent mutés, l’adaptateur ne se formait plus et les cellules étaient incapables de construire des carboxysomes corrects.
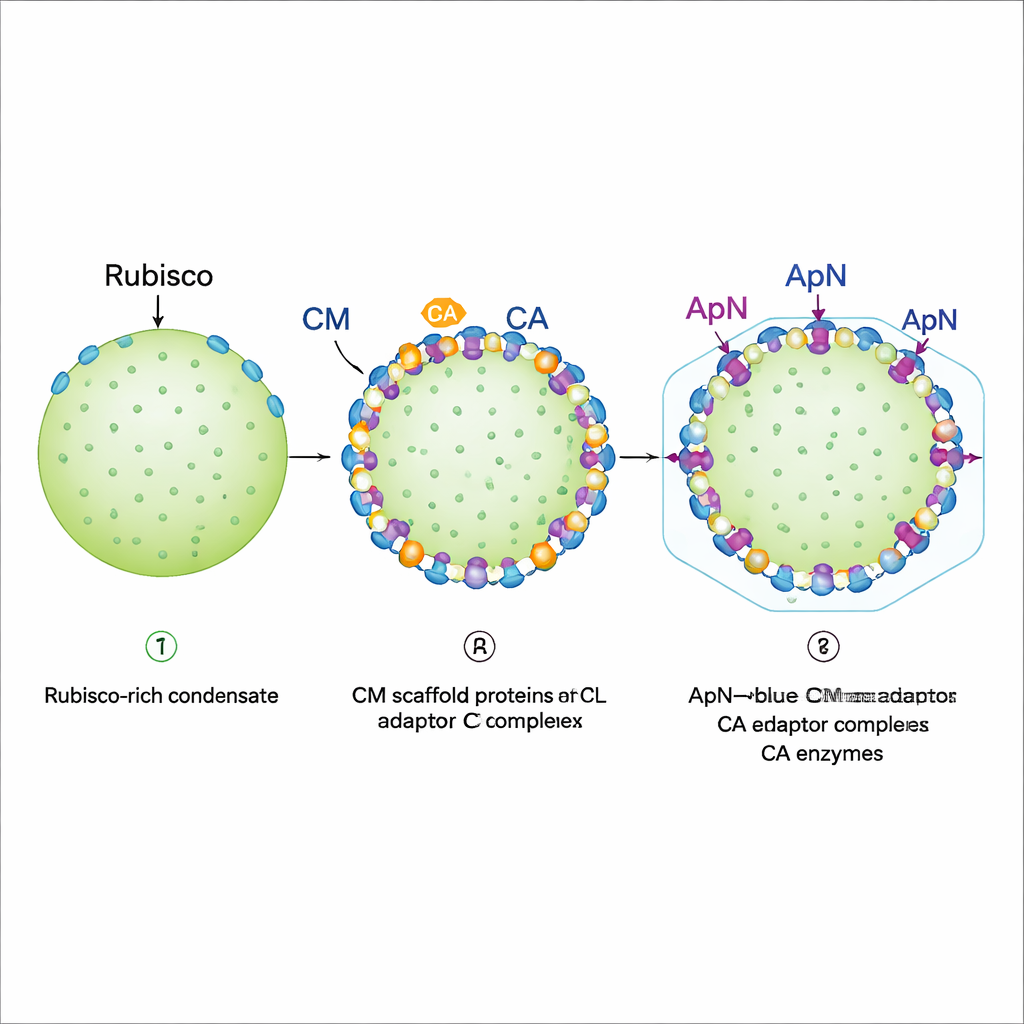
Se positionner en bordure et se préparer pour la coque
L’imagerie par fluorescence de gouttes reconstituées révéla un programme d’assemblage par étapes. D’abord, la Rubisco, la CM en pleine longueur et une variante plus courte de la CM forment un condensat dense qui se comporte comme un gel : la Rubisco y est essentiellement immobilisée. Ensuite, la CA et le complexe (ApN)3:CM sont ajoutés. Les deux se déposent préférentiellement sur le bord externe de la goutte existante, à condition que la CA arrive avant ou en même temps que (ApN)3:CM. Cette localisation en périphérie est cruciale car la queue d’ApN porte un « peptide d’encapsulation » qui se lie aux protéines de la coque. Les auteurs ont également découvert un commutateur redox intégré : à mesure que l’intérieur du carboxysome en maturation devient plus oxydant, deux résidus cystéine conservés dans ApN peuvent s’oxyder, incitant l’adaptateur à passer d’un tétramère (ApN)3:CM vers un trimère (ApN)2:CM. Dans des cellules cyanobactériennes vivantes, modifier ces cystéines ralentit la croissance et produit des carboxysomes surdimensionnés mais encore fonctionnels, soulignant leur rôle dans l’ajustement fin de la maturation.
Enseignements pour concevoir de meilleures cultures
Pour un non‑spécialiste, ces détails moléculaires peuvent sembler arides, mais ils convergent vers un message simple : la synchronisation et les partenariats comptent. Le travail montre qu’ApN doit être co‑produite avec CM pour éviter de former un auto‑amas inutile et devenir à la place un adaptateur qui se positionne à la surface du pro‑carboxysome, prêt à recruter la coque. Une étape sensible au redox aide ensuite à remodeler cet adaptateur à mesure que le compartiment se referme et que sa chimie interne change. Pour les ingénieurs végétaux qui espèrent transplanter la machinerie cyanobactérienne de concentration du CO2 dans les cultures, l’étude souligne qu’il ne suffit pas de transférer des parties isolées ; il faut aussi respecter l’ordre, les proportions et les déclencheurs chimiques qui dirigent l’assemblage des carboxysomes dans la nature.
Citation: Zang, K., Hong, X., Nguyen, N.D. et al. Stages of biomolecular condensate formation in pro-β-carboxysome assembly. Nat. Plants 12, 447–464 (2026). https://doi.org/10.1038/s41477-026-02227-6
Mots-clés: assemblage du carboxysome, mécanisme de concentration du CO2 chez les cyanobactéries, condensats de Rubisco, condensats biomoléculaires, photosynthèse synthétique