Clear Sky Science · fr
Le profilage moléculaire multicouche éclaire le diagnostic et la thérapie ciblée de la tumeur des petits ronds desmoplastique
Un cancer rare qui réclame de meilleures réponses
La tumeur des petits ronds desmoplastique (DSRCT) est un cancer extrêmement rare et agressif qui touche principalement les enfants, les adolescents et les jeunes adultes. En raison de son caractère inhabituel et de sa ressemblance microscopique avec d’autres tumeurs, les médecins ont souvent du mal à la diagnostiquer correctement et à choisir des traitements efficaces. Cette étude pose une question simple mais puissante : si l’on analyse en profondeur les tumeurs DSRCT à plusieurs niveaux moléculaires — pas seulement l’ADN, mais aussi l’ARN, les profils protéiques et les marques chimiques sur l’ADN — peut-on à la fois affiner le diagnostic et découvrir de nouvelles options thérapeutiques plus précises pour des patients à qui les traitements standards ont déjà été refusés ou ont échoué ?
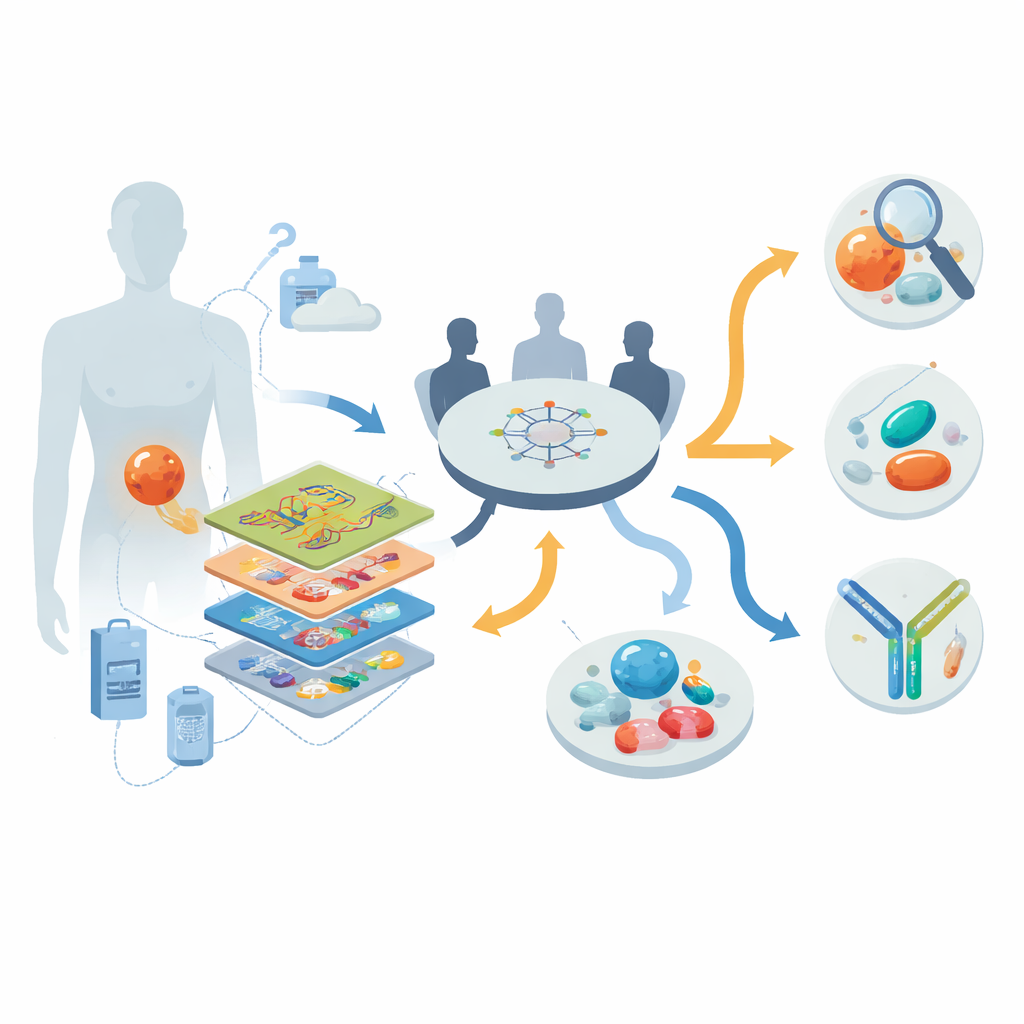
Examiner les tumeurs couche par couche
Les chercheurs ont travaillé dans le cadre d’un programme national d’oncologie de précision en Allemagne, incluant 30 personnes atteintes de DSRCT avancée, majoritairement résistante aux traitements, entre 2013 et 2022. Pour chaque patient, ils ont appliqué une boîte à outils « multi-omique » : séquençage du génome complet ou de l’exome pour étudier l’ADN ; séquençage de l’ARN pour voir quels gènes sont activement exprimés ; profilage de la méthylation de l’ADN pour capturer des empreintes épigénétiques ; et, chez neuf patients, mesures détaillées des protéines et phosphoprotéines révélant quelles voies de signalisation sont réellement actives. Un comité multidisciplinaire des tumeurs a ensuite examiné ces données avec l’histoire clinique de chaque patient pour formuler des recommandations individualisées de clarification diagnostique, de médicaments ciblés et d’essais cliniques.
Corriger des diagnostics erronés et révéler des cibles cachées
Un résultat marquant a été la fréquence à laquelle le profilage approfondi a corrigé le diagnostic initial. Chez huit des 30 patients, des tumeurs initialement classées comme d’autres entités — telles que des cancers d’origine inconnue ou des sarcomes vaguement définis — ont été reclassées en DSRCT après l’identification d’une fusion génique caractéristique (EWSR1::WT1) et d’un profil de méthylation distinctif. Parallèlement, l’ADN de ces tumeurs s’est avéré relativement calme : peu de mutations et seulement des altérations occasionnelles du nombre de copies, de sorte que l’approche classique « gène muté = cible thérapeutique » a apporté peu de résultats. Ce sont plutôt les couches ARN et protéique qui ont fourni les indices les plus riches. En comparant l’activité génique de la DSRCT à celle de centaines d’autres sarcomes, l’équipe a constaté une surexpression répétée de plusieurs molécules de surface et d’enzymes de signalisation susceptibles, en principe, d’être ciblées par des médicaments existants ou émergents.
Des signaux moléculaires à des traitements sur mesure
Sur la base de ces profils, le comité tumoral a émis 107 recommandations de prise en charge informées par la biologie moléculaire pour 28 des 30 patients. La plupart des recommandations portaient sur des médicaments bloquant les tyrosine kinases — des enzymes clés qui pilotent la croissance cellulaire et la formation de vaisseaux — ou sur des stratégies plus récentes s’attachant à des protéines de surface fortement exprimées. Parmi les exemples figurent des inhibiteurs kinasiques de petite taille comme le pazopanib ; des approches ciblées par peptides radioactifs visant les récepteurs de la somatostatine ; des CAR-T expérimentaux ciblant la molécule d’adhésion CLDN6 ; et des conjugués anticorps–médicament qui délivrent des toxines aux cellules exprimant le récepteur ERBB2 (HER2). Dix-sept patients ont été jugés éligibles à des essais cliniques appariés à des biomarqueurs, ce qui souligne comment des données moléculaires détaillées peuvent ouvrir l’accès à des études autrement difficiles d’accès pour des personnes atteintes d’une maladie ultra-rare.
Impact concret chez des patients lourdement prétraités
Parmi toutes les thérapies personnalisées recommandées, 16 ont été effectivement administrées à 13 patients, toutes guidées par des signaux au niveau de l’ARN et parfois affinées par des données de phosphoprotéines. Même si ces personnes avaient déjà reçu plusieurs cycles de chimiothérapie et de traitements locaux, huit des 13 ont obtenu un contrôle de la maladie : cinq avec une réduction partielle des tumeurs et trois avec une maladie stable. Les inhibiteurs tyrosine kinases multi-cibles, le plus souvent le pazopanib, ont apporté des bénéfices significatifs et parfois durables chez plusieurs patients, en particulier lorsque les cibles connues du médicament étaient clairement hyperactives dans la tumeur. Peut-être plus notable, deux patients présentant une forte expression d’ERBB2 ont reçu le conjugué anticorps–médicament trastuzumab deruxtecan (T-DXd). Les deux ont connu des réponses prolongées durant jusqu’à deux ans ou plus, malgré l’épuisement de nombreuses lignes thérapeutiques précédentes et malgré l’absence d’un profil d’activation élevé du récepteur ERBB2 tel qu’exigé habituellement pour les médicaments classiques bloquant ERBB2.
Ce que cela signifie pour les patients et les soins futurs
Pour les personnes atteintes de DSRCT, l’étude délivre un message prudemment optimiste. Bien que ce cancer présente peu de mutations ADN évidentes exploitables, l’analyse à travers plusieurs couches moléculaires permet à la fois de corriger des erreurs diagnostiques et de révéler des faiblesses actionnables invisibles aux tests standards. Ce travail montre que, même dans une maladie rare et agressive, une approche guidée par la biologie peut produire un bénéfice clinique tangible, y compris des réponses durables à des médicaments comme le pazopanib et le trastuzumab deruxtecan. Plus largement, il plaide pour que les patients atteints de DSRCT — et par extension d’autres cancers ultra-rares — bénéficient d’un accès systématique à un profilage moléculaire complet et à un examen expert, ouvrant la voie à des essais futurs où les traitements sont choisis non pas seulement en fonction du type tumoral, mais selon les empreintes moléculaires uniques de chaque cancer.
Citation: Renner, M., Oleś, M., Paramasivam, N. et al. Multi-layered molecular profiling informs the diagnosis and targeted therapy of desmoplastic small round cell tumor. Nat Commun 17, 3397 (2026). https://doi.org/10.1038/s41467-026-71636-0
Mots-clés: tumeur des petits ronds desmoplastique, oncologie de précision, profilage multi-omique, thérapie ciblée, conjugués anticorps-médicament