Clear Sky Science · fr
Interplay of SLC33A1-dependent and -independent Golgi sialic acid O-acetylation in CASD1 catalysis
Comment de minuscules modifications de sucres peuvent influencer la santé et la maladie
Nos cellules sont recouvertes de chaînes de sucres complexes qui font office de cartes d’identité moléculaires, guidant l’immunité, le développement et même la façon dont les virus s’attachent. Cette étude explore une modification subtile mais puissante de ces sucres — l’ajout de petites « caps » chimiques appelées groupes acétyle sur un sucre terminal nommé acide sialique — et révèle une machinerie moléculaire en deux parties, étonnamment coordonnée, qui contrôle ce processus dans l’appareil de Golgi. Comprendre ce système caché aide à expliquer certains troubles neurologiques sévères et donne des indications sur la manière dont les cellules ajustent finement leur surface en santé et en maladie. 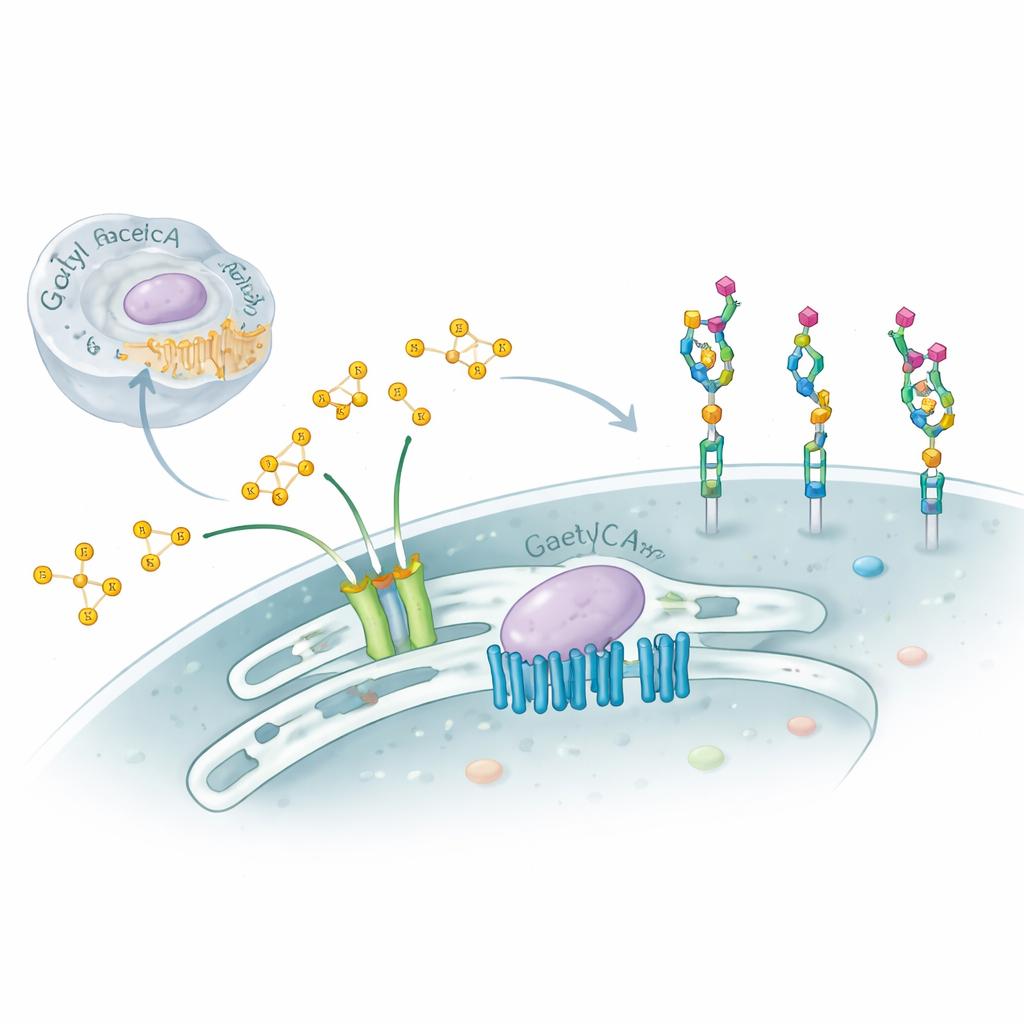
Les sucres particuliers à la surface cellulaire
Les acides sialiques se situent aux extrémités externes de nombreux sucres de surface des protéines et des lipides, en particulier sur des molécules appelées gangliosides dans le cerveau. En modifiant légèrement les acides sialiques — par exemple en ajoutant un ou deux groupes acétyle à des positions spécifiques — les cellules peuvent masquer des sites de reconnaissance existants ou en créer de nouveaux. Des virus comme l’influenza C et certains coronavirus ciblent spécifiquement ces sucres modifiés, et les gangliosides acétylés peuvent influencer la survie ou la mort des neurones ainsi que la croissance des cancers. Pourtant, malgré leur importance, le fonctionnement interne de la machinerie cellulaire qui pose ces groupes acétyle dans le Golgi est resté peu compris.
Un transporteur et une enzyme agissent de concert
Les chercheurs se sont concentrés sur deux protéines résidant dans ou autour du Golgi : SLC33A1, un transporteur qui fait traverser l’acétyl‑CoA (le principal donneur d’acétyle de la cellule) à travers les membranes, et CASD1, une enzyme connue pour transférer des groupes acétyle sur les acides sialiques. En utilisant l’édition génomique dans des lignées cellulaires humaines et de hamster, ils ont supprimé SLC33A1 et observé ce qui arrivait à des gangliosides spécifiques. Les cellules dépourvues de SLC33A1 pouvaient encore fabriquer les gangliosides de base GD3 et GD2, mais perdaient complètement leurs formes 9‑O‑acétylées, une modification emblématique liée au cancer et à la fonction neuronale. La réintroduction de SLC33A1 humain a restauré ces gangliosides acétylés, montrant que SLC33A1 est un fournisseur crucial d’acétyl‑CoA pour cette voie. 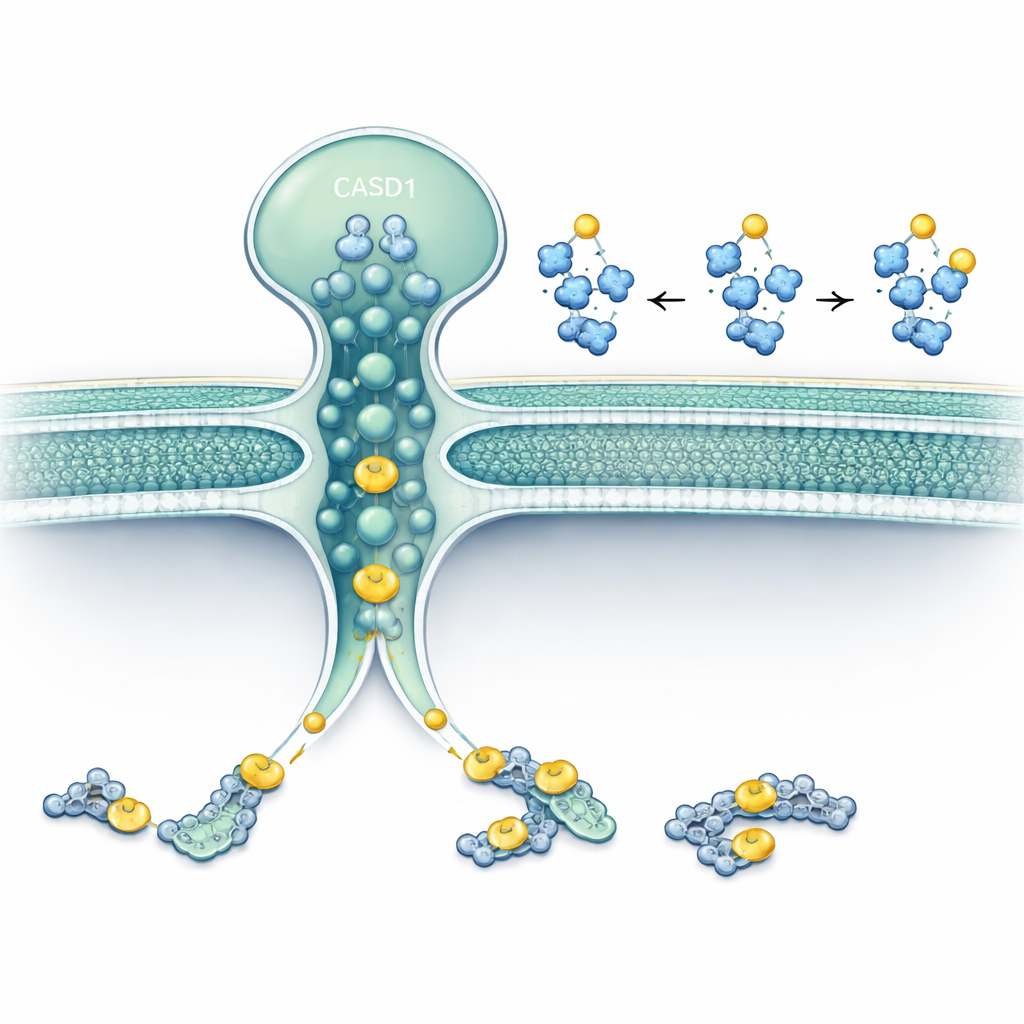
Des mutations de patients révèlent une pertinence clinique
SLC33A1 a été impliqué dans plusieurs affections neurologiques rares, y compris un trouble infantile sévère (syndrome de Huppke–Brendel), une forme de paraplégie spastique héréditaire et une ataxie cérébelleuse à début tardif. L’équipe a recréé quatre variants de SLC33A1 dérivés de patients dans des cellules dépourvues du transporteur normal et a testé si ces protéines altérées pouvaient restaurer l’acétylation des gangliosides. Les quatre présentaient une fonction réduite, et les mutations les plus sévères d’apparition infantile ne restaient que très peu efficaces pour restaurer l’acétylation. Guidés par une structure tridimensionnelle récemment résolue de SLC33A1, les auteurs ont cartographié ces mutations sur la protéine et montré comment elles perturbent probablement son architecture ou sa capacité à lier l’acétyl‑CoA. Cela suggère fortement qu’une altération de l’acétylation des gangliosides contribue aux symptômes neurologiques observés chez les patients.
Un second site actif caché dans CASD1
Le travail a aussi mis au jour une surprise inattendue : CASD1 semble être une enzyme à double fonction. Sa portion connue dans le lumen du Golgi utilise l’acétyl‑CoA fourni par SLC33A1. Mais lorsque SLC33A1 était inactivé, les cellules parvenaient encore, dans certaines conditions, à placer un seul groupe acétyle sur certains acides sialiques, bien qu’elles ne pouvaient plus ajouter le second groupe nécessaire à des motifs plus complexes. Grâce à des prédictions de structure avancées et des simulations moléculaires, les auteurs ont montré que la partie transmembranaire de CASD1 ressemble fortement à une acétyltransférase transmembranaire connue des lysosomes. Ils ont identifié des acides aminés clés dans cette région qui lient l’acétyl‑CoA côté cytosolique et transmettent directement son groupe acétyle à l’acide sialique à travers la membrane. Lorsque ces résidus ont été mutés, CASD1 a perdu cette seconde activité tant dans des essais in vitro que dans des cellules vivantes.
Deux voies, un code sucré finement réglé
Dans l’ensemble, les données soutiennent un modèle à « deux sites catalytiques ». Une voie dépend de l’entrée d’acétyl‑CoA par SLC33A1 dans le lumen du Golgi, où le domaine luminal de CASD1 ajoute un groupe acétyle à l’acide sialique, permettant des schémas d’acétylation simples ou doubles. L’autre voie est intégrée au cœur transmembranaire de CASD1, qui puise directement dans l’acétyl‑CoA cytosolique et peut encore réaliser un niveau d’acétylation de base même en l’absence de SLC33A1. Pour un non‑spécialiste, cela signifie qu’une seule enzyme, alimentée par deux sources d’acétyle différentes, écrit de subtiles « ponctuations » sur les sucres de surface cellulaire. Quand le transporteur ou l’une ou l’autre partie de l’enzyme est défectueux, ces marques sont déplacées ou absentes, ce qui peut aider à expliquer certains troubles neurodéveloppementaux et neurodégénératifs et met en lumière un nouveau niveau de régulation de la façon dont nos cellules façonnent leur identité externe.
Citation: Albers, M., Bosse, L., Schröter, L. et al. Interplay of SLC33A1-dependent and -independent Golgi sialic acid O-acetylation in CASD1 catalysis. Nat Commun 17, 3156 (2026). https://doi.org/10.1038/s41467-026-71333-y
Mots-clés: acide sialique, acétylation du Golgi, gangliosides, SLC33A1, CASD1