Clear Sky Science · fr
Dynamique structurelle du midnolin–protéasome lors du renouvellement des substrats indépendant de l’ubiquitine
Comment les cellules éliminent rapidement leurs déchets
À l’intérieur de chaque cellule, des protéines sont continuellement synthétisées et détruites. Beaucoup sont marquées par de petites molécules appelées ubiquitine avant d’être envoyées dans la principale machine de recyclage cellulaire, le protéasome. Mais certaines protéines nucléaires doivent être éliminées si rapidement qu’il n’y a pas le temps pour ce marquage. Cette étude révèle comment une protéine auxiliaire peu connue, le midnolin, s’insère directement dans le protéasome pour éliminer ces cibles urgentes, fournissant des indices sur la manière dont la cellule contrôle de façon stricte et rapide l’activité des gènes.
Un raccourci vers le broyeur cellulaire
Le protéasome 26S est un complexe en forme de tonneau qui découpe les protéines en petits fragments. Classiquement, il reconnaît ses cibles en lisant des chaînes d’ubiquitine qui y sont attachées. Des travaux récents ont mis au jour une voie alternative : un « raccourci » dans lequel le midnolin escorte certaines protéines nucléaires — en particulier les produits des gènes immédiats qui activent et désactivent rapidement l’expression — directement vers le protéasome sans aucun marquage par ubiquitine. Ces protéines, comme des facteurs de transcription impliqués dans les réponses au stress et l’inflammation, doivent apparaître et disparaître en quelques minutes. L’article combine la cryo‑microscopie électronique à haute résolution et des expériences biochimiques pour cartographier, presque image par image, comment le midnolin s’accroche au protéasome et positionne sa cargaison pour la destruction.
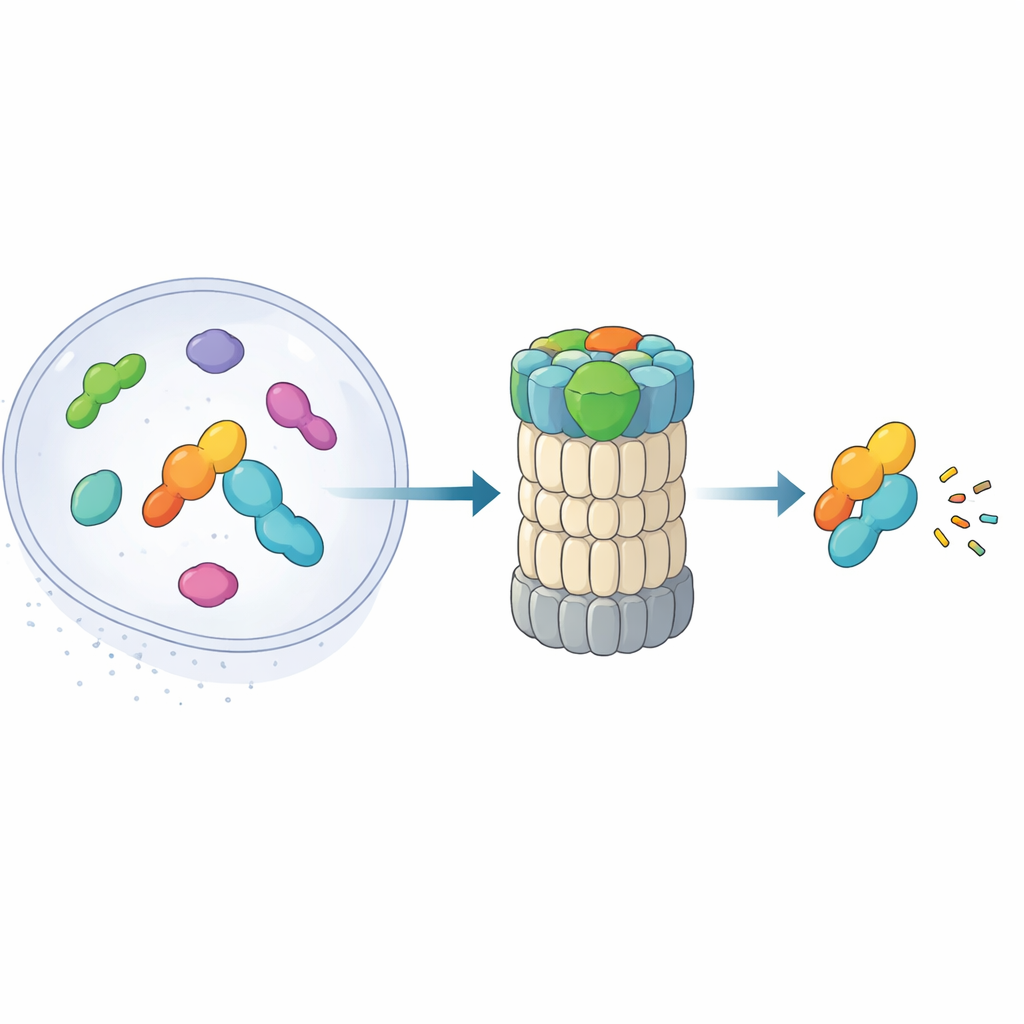
Un assistant en trois parties qui saisit et oriente les cibles
Le midnolin fonctionne comme un outil multifonction à trois modules clés. Une extrémité, une hélice C‑terminale, se branche sur un site d’ancrage d’un composant du protéasome appelé RPN1, fixant ainsi le midnolin à la machine de recyclage. Une région centrale, le « Catch », reconnaît et saisit une caractéristique filamenteuse spécifique (un dégron) présente dans les protéines cibles. À l’autre extrémité se trouve un domaine de type ubiquitine. De manière surprenante, ce domaine ne sert pas principalement à lier le protéasome, comme c’est le cas pour des domaines analogues dans d’autres protéines navette. Les auteurs montrent plutôt qu’il se loge contre RPN11, une enzyme qui coupe normalement l’ubiquitine des substrats. Ici, RPN11 joue davantage le rôle d’un échafaudage : en embrassant le segment de type ubiquitine du midnolin, il contribue à maintenir le domaine Catch et sa cargaison directement au‑dessus de la pore d’entrée étroite du protéasome.
Guider la protéine vers le noyau broyeur
Une fois le midnolin amarré, le moteur énergivore du protéasome — un anneau AAA+ ATPase — prend le relais. Cet anneau est situé juste sous la pore d’entrée et tire les chaînes protéiques dépliées vers le cœur, étape par étape. Les clichés cryo‑EM révèlent une série de positions « en escalier en spirale » adoptées par les six sous‑unités du moteur lorsqu’elles saisissent et transmettent le substrat à travers le canal central. Les auteurs ont capturé quatre étapes consécutives de ce cycle, toutes avec du matériel lié au midnolin passé à travers la pore, et ont même observé comment la libération d’un ion magnésium dans une sous‑unité coïncide avec un déplacement vers le bas de l’ensemble de l’anneau. Cela suggère qu’un usage coordonné de l’ATP et la libération du magnésium contribuent à faire avancer la protéine plus profondément dans la chambre où se trouvent les sites de coupe.
Pourquoi le positionnement et la co‑expression sont importants
L’équipe a testé comment chaque module du midnolin contribue à l’efficacité. L’hélice d’ancrage seule peut se lier à RPN1 mais ne suffit pas à augmenter significativement l’activité du protéasome. La suppression du domaine Catch laisse de nombreux protéasomes bloqués dans un état inactif, sans substrat, même si le midnolin peut toujours s’attacher ; remplacer le Catch par un substrat fusionné de façon permanente ne restaure pas non plus l’activité complète. Ces observations indiquent que le Catch ne se contente pas de saisir la cible : il doit aussi orienter la protéine précisément à l’entrée de la pore. Des données biochimiques et des transcriptomes tumoraux montrent en outre que le midnolin a tendance à être produit en même temps que ses substrats. Lorsqu’ils sont co‑exprimés, le midnolin se replie mieux et forme des complexes stables, créant un paquet « dégrade‑moi » prêt à être rapidement livré au protéasome lorsque la cellule doit réinitialiser l’expression génique.
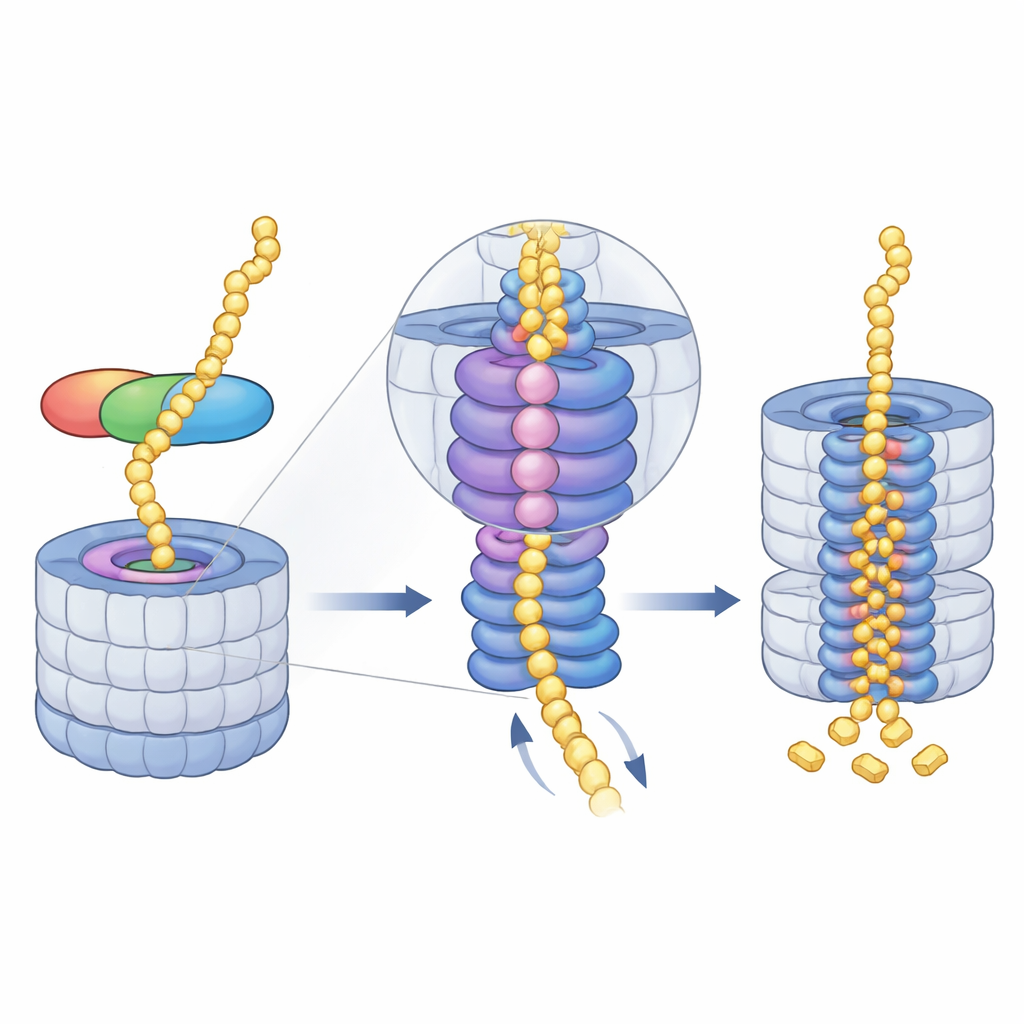
Auto‑nettoyage et perspectives médicales
Après que la protéine cible a été tirée et découpée, le midnolin lui‑même n’est pas épargné. Ses propres régions non structurées peuvent être engagées par le moteur et alimentées dans la même chambre de destruction, garantissant que l’auxiliaire ne s’accumule pas inutilement. En éclairant cette voie vers le protéasome dépourvue d’ubiquitine, l’étude étend notre compréhension de la gestion des durées de vie des protéines sur des calendriers très serrés. Elle suggère aussi de nouvelles stratégies thérapeutiques : en concevant des molécules inspirées du midnolin qui rattachent directement des protéines nucléaires pathogènes au protéasome, les chercheurs pourraient un jour éliminer plus rapidement et de manière plus sélective des cibles « intraitables », y compris certains inducteurs de cancer.
Citation: Zhu, C., Qin, L., Dai, Z. et al. Structural dynamics of the midnolin-proteasome during ubiquitin-independent substrate turnover. Nat Commun 17, 2800 (2026). https://doi.org/10.1038/s41467-026-71002-0
Mots-clés: protéasome, midnolin, dégradation des protéines, voie indépendante de l’ubiquitine, gènes immédiats