Clear Sky Science · fr
La compétence transcriptionnelle définit le potentiel nucléateur d’hétérochromatine des unités MSR isolées
Interrupteurs cachés dans notre ADN
Nos génomes sont repliés à l’intérieur du noyau cellulaire sous deux états principaux : des régions actives hébergeant des gènes, et des étendues fortement compactées longtemps considérées comme la « matière noire » génétique. Cette étude pose une question apparemment simple : qu’est‑ce qui ordonne à une portion d’ADN de devenir ce matériau fortement compacté et répressif — l’hétérochromatine — en premier lieu ? En disséquant une classe spécifique d’ADN répétitif chez la souris, les auteurs montrent que toutes les répétitions ne se valent pas : seules celles capables de soutenir une forme particulière de transcription peuvent actionner l’interrupteur qui construit et maintient ces voisinages silencieux de l’ADN.
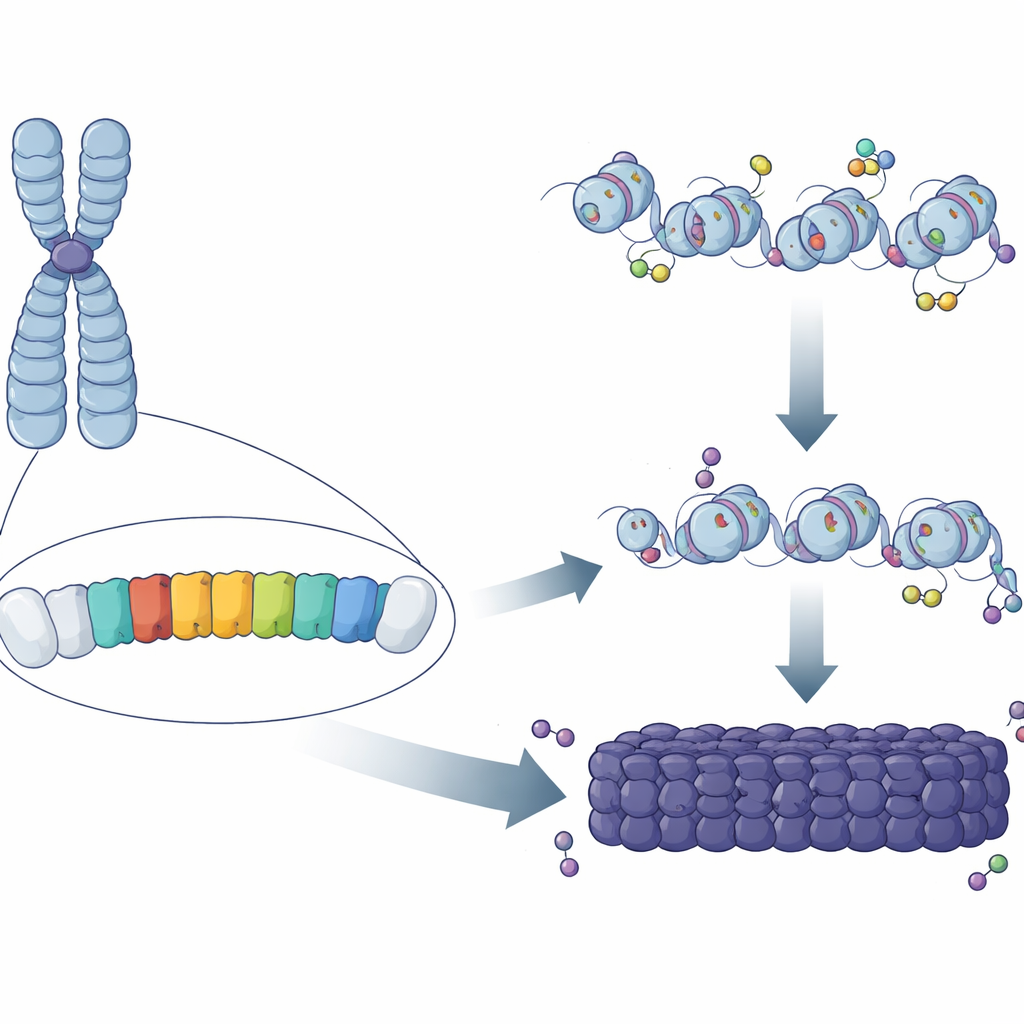
Motifs répétés dans le génome
Près de la moitié de l’ADN des mammifères est composée de séquences répétées, dont beaucoup s’accumulent autour de la région centromérique des chromosomes. Chez la souris, un composant majeur de ces régions est le « repeat satellite majeur » (MSR), une courte séquence riche en A/T copiée des centaines de milliers de fois. Des travaux classiques ont montré que ces régions sont tapissées de marques chimiques et de protéines qui verrouillent l’ADN dans un état compact et protecteur. Mais il restait mystérieux pourquoi certaines copies de MSR devenaient pleinement hétérochromatiques alors que d’autres, disséminées ailleurs dans le génome, ne l’étaient pas. Les auteurs ont supposé que de petites différences de séquence ou de comportement des unités MSR individuelles pourraient déterminer si elles peuvent amorcer, ou « nucléer », une tache d’hétérochromatine.
Construction d’un site test dans le génome
Pour tester cette idée de façon nette, l’équipe a conçu des cellules souches embryonnaires de souris contenant un site d’atterrissage artificiel dans un tronçon silencieux du chromosome 2 — une région sans gènes ni répétitions à proximité et sans activité détectable. Dans ce site neutre, ils ont inséré différents fragments d’ADN : des unités MSR intactes, des variantes MSR fortement brouillées, et des éléments de contrôle comme des promoteurs viraux ou des segments d’éléments mobiles. Cela leur a permis d’évaluer, unité par unité, quelles séquences sont capables d’attirer les caractéristiques emblématiques de l’hétérochromatine : une marque chimique spécifique sur les histones (H3K9me3), la liaison des protéines HP1, et l’incorporation de l’histone de liaison H1, qui ensemble épaississent et stabilisent la chromatine locale.
Seules les répétitions prêtes à transcrire amorcent la chromatine silencieuse
Les résultats ont été remarquablement sélectifs. Une seule unité MSR intacte insérée au site test n’a pas suffi à modifier la chromatine. En revanche, trois copies tandem ou plus de la séquence MSR intacte ont converti la région environnante en une « île » d’hétérochromatine, avec des niveaux élevés de H3K9me3, HP1 et histone H1. À l’inverse, des tronçons de longueur équivalente de séquence MSR brouillée, ou d’un autre type de répétition (la région 5' non traduite des LINE‑1), n’y sont pas parvenus, même s’ils pouvaient provoquer une transcription forte. La différence clé était que les unités MSR intactes multi‑copies soutenaient une transcription modeste et bidirectionnelle produisant de courts ARN non standard étroitement associés à la chromatine. Ce modèle, plutôt qu’une transcription élevée de type génique, corrélait avec la capacité à nucléer l’hétérochromatine.
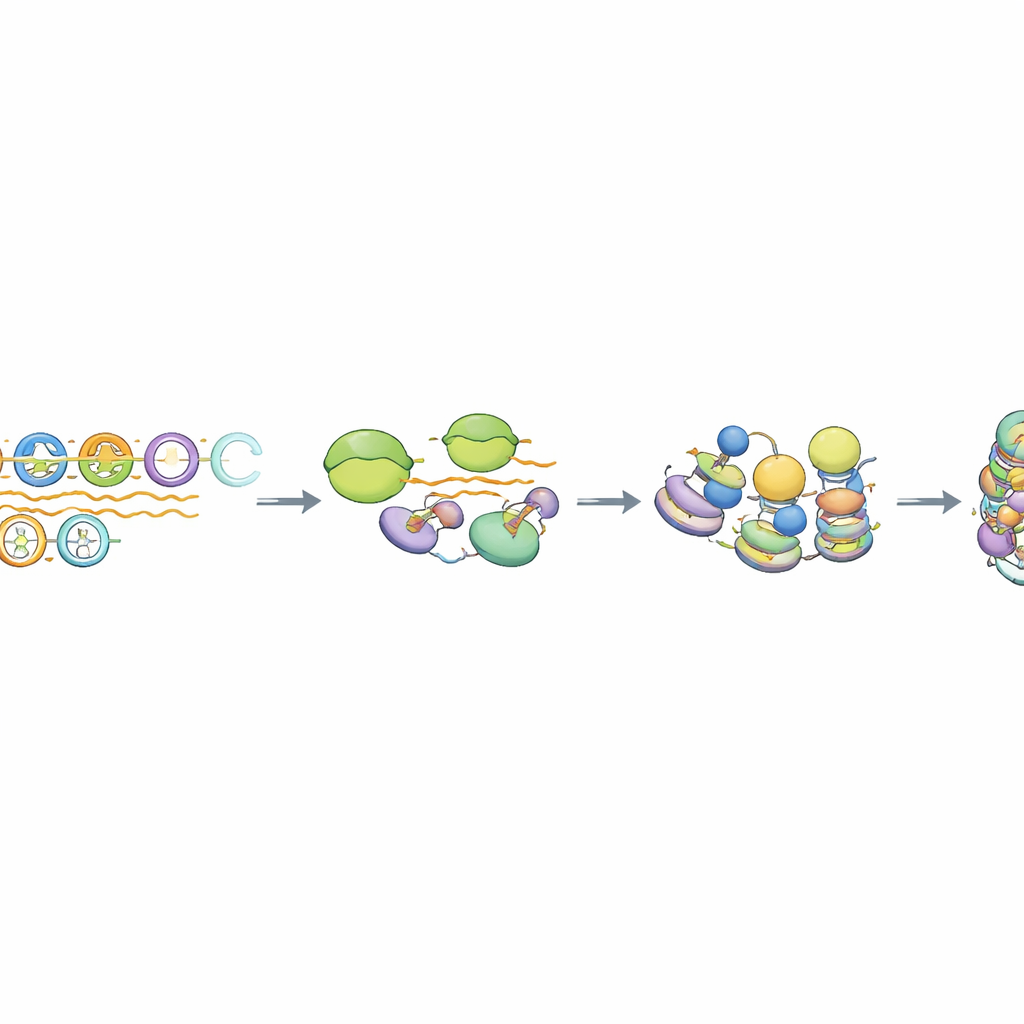
Une forme particulière de transcription et de traitement des ARN
En creusant davantage, les auteurs ont constaté que l’ARN polymérase II, l’enzyme qui produit normalement l’ARN messager, s’engage brièvement sur les matrices MSR mais n’avance pas efficacement en longs transcrits. Les ARN résultants sont dépourvus des caractéristiques typiques des ARNm, telles qu’une coiffe 5' protectrice et de longues queues poly‑A, et ils restent proches de l’ADN qui les a produits. Un complexe protéique appelé Integrator, connu pour tronçonner et terminer certains ARN non codants, était spécifiquement enrichi sur les unités MSR intactes. Lorsque l’activité de coupure d’Integrator était réduite, les niveaux d’ARN dérivés des MSR augmentaient sensiblement, mais la marque histone répressive clé persistait tandis que la liaison d’HP1 évoluait subtilement. Une analyse à l’échelle du génome a montré que seuls les ~10–15 % de copies MSR les plus intactes se comportent ainsi, mettant en évidence un sous‑ensemble de répétitions « compétentes » câblées pour cette voie de silençage couplée à la transcription.
ADN déroulé comme imitation de promoteur
L’équipe a également exploré comment l’ADN MSR lui‑même favorise cette transcription inhabituelle. Les réseaux MSR multi‑copies, mais pas les copies simples ou doubles, présentaient des signes clairs d’ADN localement déroulé et d’hybrides ARN:ADN, des caractéristiques structurales souvent observées près de promoteurs actifs et aux sites de pause. Ces configurations étaient renforcées lorsque les enzymes topoisomérases étaient inhibées, et coïncidaient avec une plus grande transcription des MSR et des caractéristiques d’hétérochromatine plus marquées. Les auteurs proposent que trois unités MSR en tandem ou plus créent une topologie physique de l’ADN qui mime un promoteur, invitant la polymérase et les facteurs de transcription à s’engager juste assez pour générer de courts ARN qui, avec des protéines spécifiques, renforcent une architecture de chromatine compacte.
Pourquoi cela compte pour la santé du génome
Pour un observateur non spécialiste, ce travail révèle que des portions de notre ADN « poubelle » fonctionnent comme des interrupteurs finement réglés, utilisant un mélange de conformation de l’ADN, de transcription de faible niveau et de traitement des ARN pour construire la coque protectrice du génome. Seules les unités MSR capables de soutenir cette transcription contrôlée et non messagère peuvent déclencher la formation d’hétérochromatine, tandis que les éléments brouillés ou excessivement actifs ne le peuvent pas. Cette logique fondée sur l’ADN et l’ARN aide à expliquer comment les cellules distinguent les régions à garder silencieuses de celles autorisées à porter des gènes, et pourquoi des ARN satellites mal régulés sont associés au cancer et à des troubles du développement. En substance, l’étude montre que le « fond » répétitif du génome n’est pas un remplissage passif mais un ingénieur actif de l’architecture nucléaire et de la stabilité.
Citation: Lo, YH., Shukeir, N., Erikson, G. et al. Transcriptional competence defines the heterochromatin nucleating potential of isolated MSR units. Nat Commun 17, 2653 (2026). https://doi.org/10.1038/s41467-026-70991-2
Mots-clés: hétérochromatine, ADN satellite, ARN non codant, structure de la chromatine, stabilité du génome