Clear Sky Science · fr
Hétérogénéité spatiale des MDSC médiée par le signalement ANXA1-FPRs favorisant l’immunosuppression dans la progression du COSC
Pourquoi les défenses de l’organisme peinent contre certains cancers de la bouche
Le carcinome épidermoïde buccal, une forme fréquente de cancer de la bouche, résiste souvent aux traitements immunothérapeutiques actuels qui mobilisent les défenses de l’organisme. Cette étude pose une question simple mais cruciale : pourquoi des cellules immunitaires puissantes, qui devraient reconnaître et détruire la tumeur, échouent-elles si souvent ? En cartographiant la position des différents types cellulaires dans la tumeur et leurs interactions, les chercheurs mettent au jour un jeu changeant du « chat et de la souris » entre cellules cancéreuses, cellules suppressives et lymphocytes T cytotoxiques, qui aide à expliquer les échecs thérapeutiques — et suggère une manière de les surmonter. 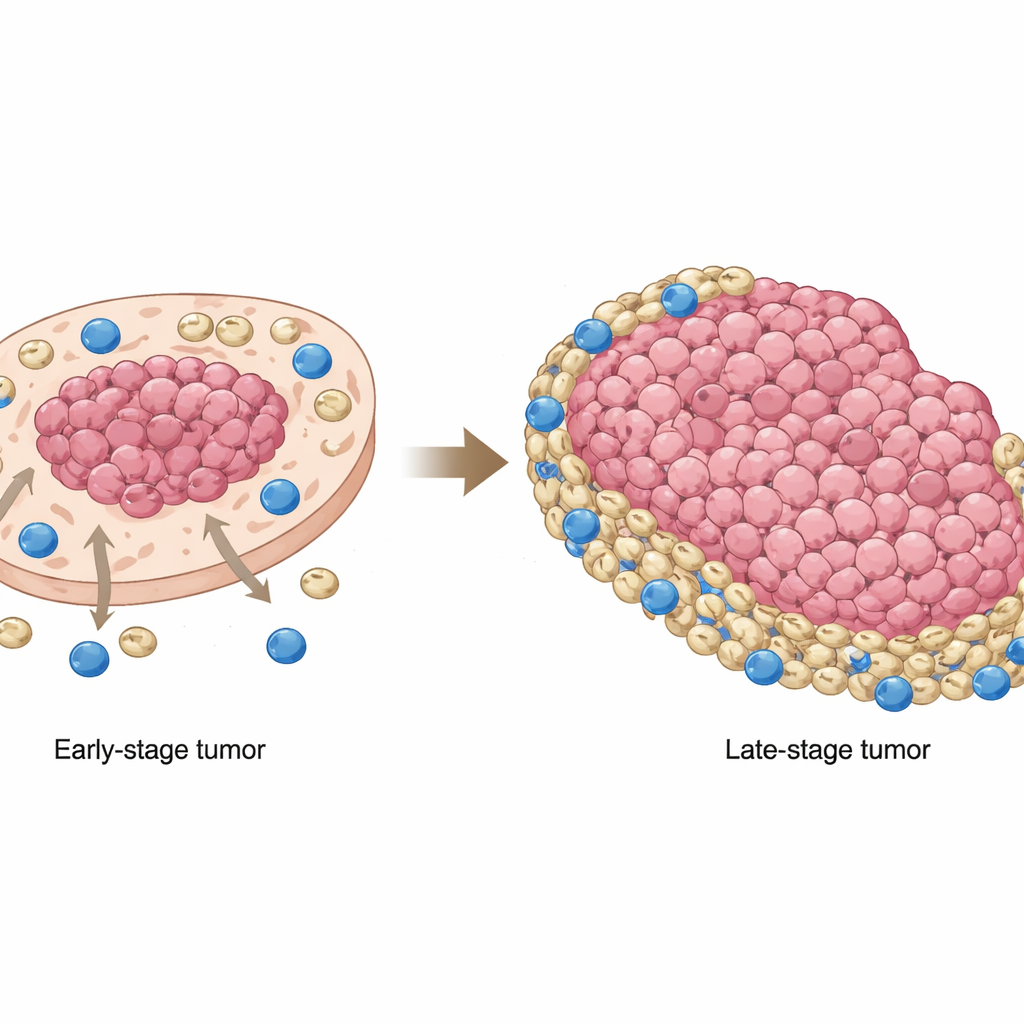
Le paysage caché à l’intérieur d’une tumeur
Les auteurs ont combiné deux approches de pointe : le séquençage ARN unicellulaire, qui lit l’activité des cellules individuelles, et la transcriptomique spatiale, qui indique où ces cellules se situent dans des coupes de tissu tumoral. En analysant des tumeurs de patients aux stades précoces et avancés du cancer buccal, ils ont identifié les principaux acteurs cellulaires : les cellules épithéliales tumorales, les lymphocytes T CD8 « tueurs », d’autres cellules T et B, des fibroblastes formant le support structurel, et des cellules immunitaires spécialisées appelées cellules suppressives dérivées de la lignée myéloïde (MDSC). Alors que les tumeurs précoces contenaient davantage de lymphocytes T CD8 actifs, les tumeurs avancées présentaient une signalisation T amoindrie et des signaux immunosuppresseurs plus forts émanant des cellules myéloïdes, indiquant un environnement progressivement plus hostile à l’immunité antitumorale.
Les cellules suppressives en mouvement
Une des observations marquantes est le changement de position des MDSC au fur et à mesure de la progression tumorale. Dans les cancers au stade précoce, ces cellules suppressives avaient tendance à se regrouper dans les régions riches en cellules tumorales, près du noyau tumoral. Aux stades avancés, elles se déplaçaient vers l’extérieur, s’accumulant dans des zones pauvres en cellules tumorales et en périphérie, où les lymphocytes T CD8 étaient plus fréquents. Cela signifie que, dans les tumeurs avancées, les lymphocytes tueurs sont en grande partie repoussés vers les bords et rencontrent alors une ceinture de MDSC qui atténue leur capacité à attaquer les cellules cancéreuses. Des prélèvements de patients et des modèles murins ont confirmé que cette redistribution n’était pas anecdotique : lorsque le recouvrement entre MDSC et cellules tumorales diminuait et que les MDSC s’établissaient plutôt dans des régions non tumorales, la survie globale des patients était plus mauvaise. 
Un switch de signalisation entre cellules cancéreuses et suppressives
L’étude a examiné de près une « conversation » moléculaire entre cellules tumorales et MDSC impliquant la protéine annexine A1 (ANXA1) à la surface des cellules tumorales et une famille de récepteurs nommée FPR sur les cellules myéloïdes. Dans les stades précoces, l’ANXA1 des cellules tumorales interagissait fortement avec FPR1 et FPR3, en particulier sur les MDSC et les macrophages associés à la tumeur, contribuant au recrutement et au maintien de ces cellules suppressives au cœur tumoral. Au fur et à mesure de la progression, le niveau d’ANXA1 sur les cellules tumorales diminuait, affaiblissant ces connexions initiales. Parallèlement, de plus en plus de MDSC exprimaient un autre récepteur, FPR2, et la signalisation ANXA1–FPR2 est apparue comme une voie compensatoire permettant de maintenir l’engagement des MDSC. Un sous-ensemble spécifique de cellules tumorales présentant une forte expression d’ANXA1, avec des caractéristiques de type souche, semblait agir comme un « appât », attirant les MDSC au début ; lorsque l’ANXA1 chutait, les MDSC n’étaient plus ancrées au centre et migraient vers des régions riches en lymphocytes T CD8.
Désactiver le bouclier pour améliorer l’immunothérapie
Pour tester si interrompre cette communication pouvait améliorer le traitement, les chercheurs ont utilisé un modèle murin de cancer buccal et bloqué FPR2 avec un inhibiteur de petite molécule appelé WRW4. Seul, l’inhibition de FPR2 réduisait la présence des MDSC et augmentait les lymphocytes T CD8 dans le microenvironnement tumoral, mais n’a pas suffisamment ralenti la croissance tumorale. De même, un traitement seul par un anticorps anti–PD-1 produisait des bénéfices modestes, car les MDSC formaient toujours une barrière suppressive. Lorsque les deux traitements étaient combinés, toutefois, la croissance tumorale était fortement freinée et la survie des souris améliorée. Chez ces animaux, l’infiltration en MDSC chutait nettement tandis que les lymphocytes T CD8 pénétraient plus profondément dans les régions riches en cellules tumorales, suggérant que le blocage de FPR2 supprime un bouclier clé qui protège normalement les cellules cancéreuses de l’attaque immunitaire.
Ce que cela signifie pour les soins anticancéreux futurs
Dans l’ensemble, ce travail montre que non seulement les types cellulaires mais aussi leur organisation spatiale et leurs partenariats de signalisation déterminent si l’immunothérapie peut réussir dans le cancer buccal. À mesure que la tumeur progresse, les MDSC migrent du centre vers les bords, où elles interceptent les lymphocytes T tueurs, et la signalisation ANXA1–FPR2 contribue à maintenir cette disposition suppressive. En perturbant cette voie — en particulier en association avec les inhibiteurs de points de contrôle immunitaires existants — les cliniciens pourraient reprogrammer le microenvironnement tumoral pour que les cellules immunitaires de l’organisme reconnaissent et détruisent à nouveau la tumeur. Cela suggère une stratégie concrète : associer des bloqueurs de FPR2 à l’immunothérapie pourrait améliorer les résultats chez les patients dont les cancers buccaux résistent actuellement aux meilleurs traitements disponibles.
Citation: Li, F., Han, Y., Ou, F. et al. Spatial heterogeneity of MDSCs mediated by ANXA1-FPRs signaling drives immune suppression in OSCC progression. Nat Commun 17, 2535 (2026). https://doi.org/10.1038/s41467-026-70861-x
Mots-clés: carcinome épidermoïde buccal, microenvironnement tumoral, cellules suppressives dérivées de la lignée myéloïde, transcriptomique spatiale, immunothérapie contre le cancer