Clear Sky Science · fr
La signalisation FGFR établit des gradients spatiaux d’identités de cellules sécrétoires le long de l’axe proximal-distal des voies aériennes
Comment nos voies aériennes trient discrètement et protègent l’air que nous respirons
Chaque respiration balaie l’air sur des millions de cellules qui tapissent notre trachée et nos poumons. Ces cellules font bien plus que fournir une simple surface passive : elles détoxifient les polluants, combattent les germes et aident à empêcher l’affaissement des petits sacs aériens. Cette étude révèle que les cellules sécrétoires de l’arbre respiratoire de la souris ne sont pas toutes identiques. Elles sont organisées en gradients lisses allant de la région proche de la gorge (proximale) jusqu’aux régions profondes du poumon (distales), et une voie de signalisation clé, appelée FGFR2b, contribue à établir et maintenir ces changements progressifs d’identité et de fonction. Comprendre cet ordre caché éclaire la manière dont les poumons restent en bonne santé et ce qui peut mal tourner dans les maladies pulmonaires chroniques.
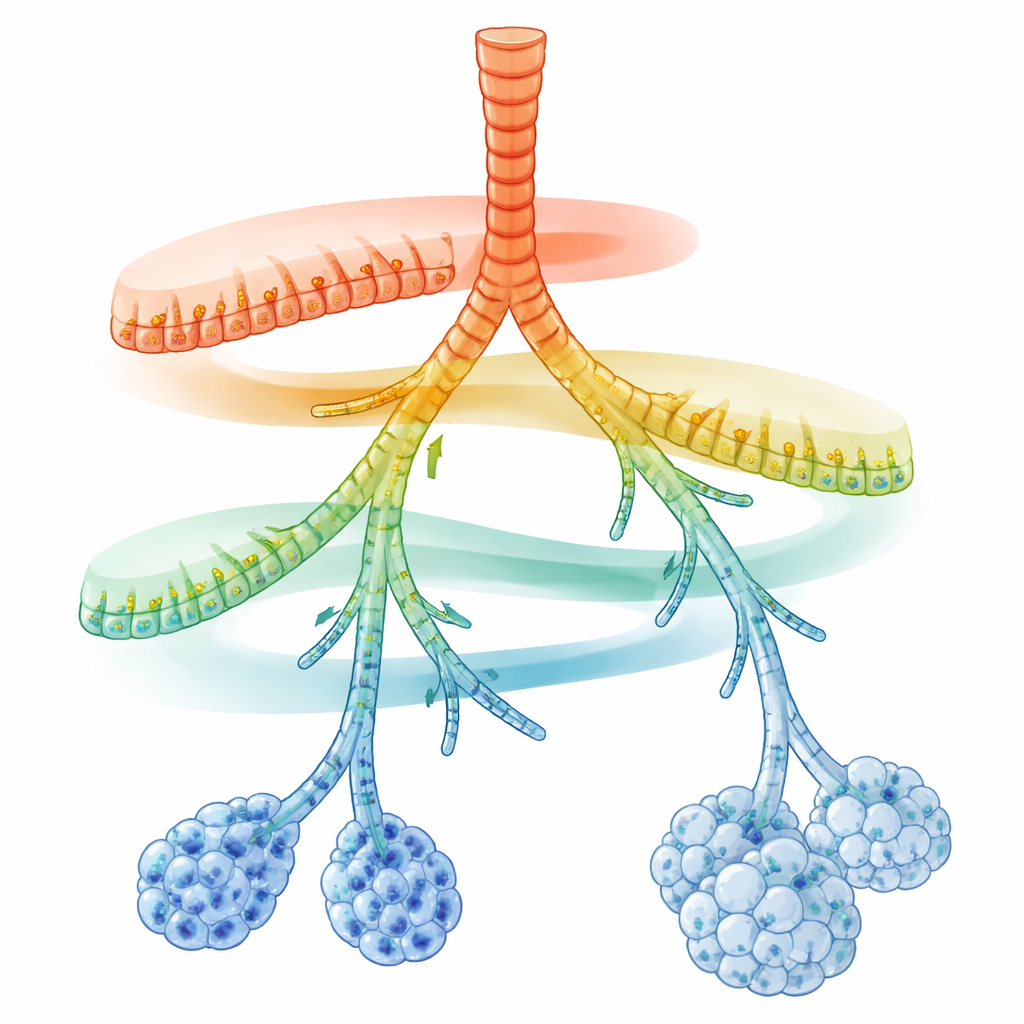
Une carte cachée le long des conduits respiratoires
Les chercheurs se sont concentrés sur les cellules sécrétoires, qui tapissent les conduits aériens et sécrètent du mucus, des peptides antimicrobiens et du surfactant. En utilisant le séquençage ARN monocellulaire, ils ont lu les gènes actifs dans des milliers de cellules individuelles provenant de poumons de souris adultes. Lorsqu’ils ont projeté ces cellules sur une carte de similarité moléculaire, les cellules sécrétoires ne se sont pas regroupées en quelques types rigides. Elles formaient plutôt une chaîne continue d’états reliant les grandes voies aériennes aux minuscules alvéoles. En plus d’un programme central partagé pour la détoxification des inhalants, deux gradients opposés d’activité génique sont apparus : près des grandes voies aériennes, les gènes impliqués dans une défense innée rapide étaient les plus élevés ; vers les branches les plus éloignées et les alvéoles, les gènes liés au métabolisme lipidique, à la production de surfactant et à la présentation d’antigènes dominaient.
D’un point de départ unique vers de nombreux états cellulaires spécialisés
Pour comprendre comment ce schéma émerge, l’équipe a marqué les précurseurs sécrétoires à la fin de la vie fœtale et a suivi leurs descendants au cours de la vie précoce grâce au traçage de lignage et à l’analyse monocellulaire. Ces cellules marquées formaient initialement un réservoir immature doté d’une forte machinerie de synthèse protéique et de gènes associés à la construction tissulaire. Après la naissance, quand la respiration et l’exposition au monde extérieur ont commencé, ces cellules se sont progressivement diversifiées en plusieurs groupes matures : des cellules sécrétoires proximales riches en gènes de défense innée, des cellules plus centrales avec des signatures développementales et régulatrices, des cellules doublement positives faisant le lien entre identités airway et alvéolaire, et des cellules de type 2 alvéolaires spécialisées pour le surfactant. Le programme de détoxification s’est activé tôt et de manière étendue, tandis que les programmes d’immunité innée et de présentation d’antigènes se sont mis en place plus tard et dans des régions distinctes, indiquant que les caractéristiques des cellules sécrétoires sont acquises selon une séquence temporelle définie.
Comment un signal de croissance façonne l’identité des voies aériennes distales
Un indice majeur sur ce qui pilote ces gradients est venu d’un récepteur appelé FGFR2b, partie d’une voie de signalisation des facteurs de croissance déjà connue pour être essentielle aux cellules alvéolaires de type 2. FGFR2b et ses gènes cibles étaient plus actifs dans les cellules des voies aériennes distales et alvéolaires que dans les cellules proximales. Lorsque les chercheurs ont éteint FGFR2b spécifiquement dans les cellules sécrétoires juste après la naissance, le programme distal normal a faibli. Les gènes nécessaires à la production de surfactant et au trafic vésiculaire ont diminué, tandis que les gènes typiques des cellules alvéolaires plates de type 1, des composants mitochondriaux, des canaux ioniques et des facteurs de survie au stress ont augmenté. Certaines cellules intermédiaires des voies aériennes exprimaient désormais conjointement des niveaux modérés de marqueurs proximaux de défense innée et des marqueurs distaux, brouillant en pratique le profil spatial normal. Dans des cultures d’organoïdes dérivées de cellules des voies aériennes, l’ajout de ligands FGFR a réprimé les marqueurs proximaux de défense innée et renforcé les gènes liés au surfactant d’une manière conforme aux observations in vivo, confirmant que l’activation de FGFR2b suffit à pousser les cellules vers une identité sécrétoire distale.
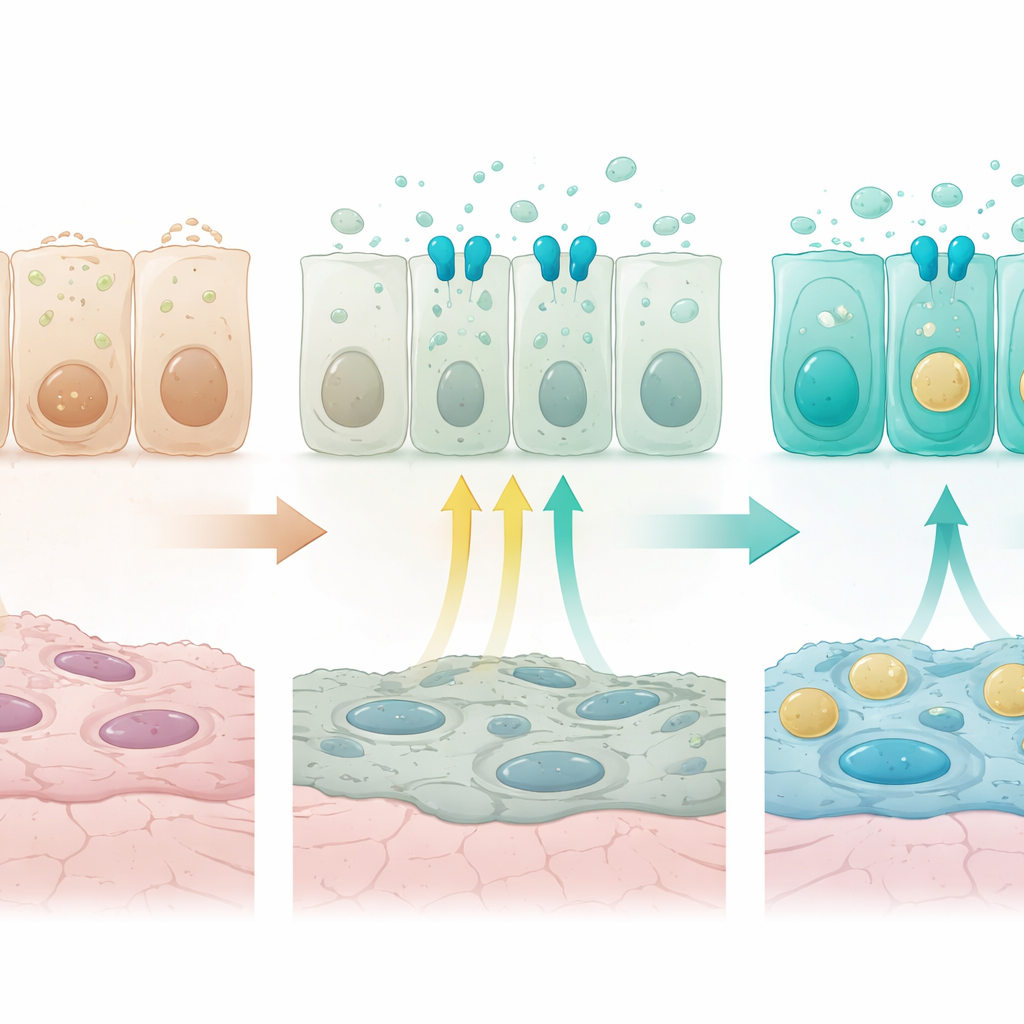
Ajustements fins par interaction avec d’autres signaux
L’équipe a également exploré comment la signalisation FGFR2b interagit avec une autre voie portée par VEGFA, mieux connue pour façonner les vaisseaux sanguins. Dans les organoïdes, le VEGFA seul pouvait atténuer certains gènes de défense innée, et le blocage de son récepteur modifiait certains marqueurs distaux, mais il ne pouvait pas pleinement remplacer FGFR2b. En fait, la perte de FGFR2b in vivo réduisait l’expression de Vegfa, et la stimulation conjointe des deux voies rétroagissait pour abaisser les niveaux de FGFR2b, soulignant un dialogue complexe entre ces systèmes de signalisation. Chez la souris adulte, l’extinction de FGFR2b ne remodelait plus de manière spectaculaire les gradients d’immunité innée, mais elle restait nécessaire pour maintenir l’expression de marqueurs distaux clés, tels que le gène du surfactant Sftpb et le marqueur sécrétoire classique des voies aériennes Scgb1a1, et pour préserver les cellules hybrides airway–alvéolaires.
Pourquoi ces gradients sont importants pour la santé pulmonaire
Le tableau qui émerge présente le revêtement des voies aériennes comme un paysage finement gradué plutôt qu’un patchwork de zones isolées. Les régions proximales sont calibrées pour une défense rapide à base de mucus, tandis que les régions distales combinent production de surfactant et communication immunitaire plus spécialisée. La signalisation FGFR2b aide à établir et à soutenir cette organisation, en particulier dans les compartiments distaux, en promouvant les programmes liés aux lipides et au trafic vésiculaire et en restreignant des caractéristiques inappropriées de type proximal. La perturbation de ces gradients, qu’elle soit d’origine génétique, environnementale ou liée à la maladie, pourrait déséquilibrer la défense, la détoxification et le soutien de l’échange gazeux, contribuant à des états où les voies aériennes distales adoptent des traits plus proximaux. Ce cadre offre une nouvelle manière d’envisager les maladies pulmonaires qui « reconfigurent » l’arbre bronchique et peut orienter de futures stratégies pour restaurer une organisation cellulaire appropriée.
Citation: Sountoulidis, A., Theelke, J., Liontos, A. et al. FGFR signaling establishes spatial gradients of secretory cell identities along the airway proximal-distal axis. Nat Commun 17, 2651 (2026). https://doi.org/10.1038/s41467-026-70842-0
Mots-clés: épithélium des voies aériennes, cellules sécrétoires, signalisation FGFR2b, développement pulmonaire, gradients spatiaux