Clear Sky Science · fr
Les canaux à protons régulent la chimie carbonatée vésiculaire dans les cellules minéralisantes d’un calcificateur marin
Comment de minuscules bâtisseurs façonnent notre planète
Une grande partie des falaises calcaires et des récifs coralliens de la Terre est fabriquée par des bâtisseurs microscopiques qui prélèvent des ingrédients dissous dans l’eau de mer et les transforment en roche solide. Cette étude examine l’intérieur d’un de ces bâtisseurs — le stade larvaire d’un oursin — pour poser une question étonnamment fondamentale : comment ses cellules contrôlent‑elles l’acidité pendant qu’elles construisent un squelette en carbonate de calcium ? La réponse révèle un astucieux mécanisme électrique qui peut aussi expliquer pourquoi les organismes marins formant des coquilles sont si vulnérables à un océan plus acide.
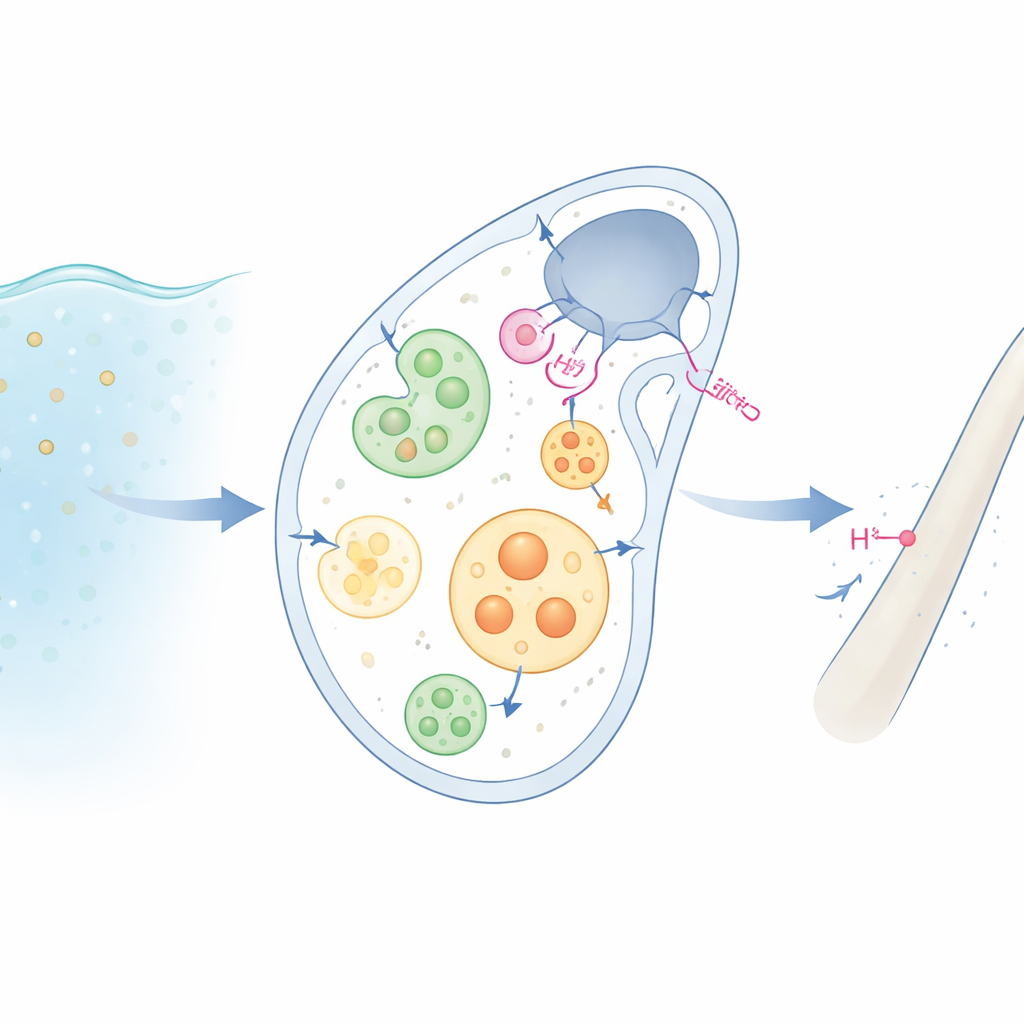
De l’eau de mer au squelette
Les larves d’oursin durcissent leur corps avec de minuscules bâtonnets de calcite composés de carbonate de calcium. Pour ce faire, des cellules spécialisées « minéralisantes » aspirent d’abord l’eau de mer, la conditionnent en petites gouttes internes, ou vésicules. À l’intérieur de ces vésicules, les ingrédients du minéral — calcium, carbonate et autres ions — sont concentrés en un précurseur amorphe, vitreux, qui se cristallise ensuite. Mais chaque fois que du carbonate de calcium se forme, de l’acide supplémentaire (protons) est produit. Si cet acide s’accumulait, il dissoudrait le minéral que les cellules cherchent à fabriquer. La manière dont les cellules empêchent cette auto‑destruction a longtemps été une énigme.
Mesurer l’acidité à l’intérieur de gouttes en mouvement
Les chercheurs ont utilisé l’imagerie en direct et des indicateurs fluorescents sensibles au pH pour observer la chimie à l’intérieur de ces vésicules en temps réel. Ils ont constaté qu’à peu près la moitié des vésicules étaient fortement alcalines — plus basiques que l’eau de mer normale — tandis que les autres étaient neutres ou légèrement acides. Lorsqu’ils ont brièvement modifié l’acidité de l’eau de mer environnante, l’intérieur des cellules et des vésicules a lui aussi bougé, montrant que les protons peuvent traverser relativement librement ces membranes. Cependant, les vésicules étaient partiellement protégées par rapport à l’intérieur cellulaire : elles réagissaient plus lentement et de façon moins marquée, ce qui suggère une « perméabilité » contrôlée aidant à maintenir des conditions favorables à la minéralisation.
Fuites électriques qui évacuent l’acide
Pour découvrir ce qui crée cette perméabilité, l’équipe s’est concentrée sur une protéine canal à protons nommée Otop2l, déjà associée à la croissance du squelette d’oursin. Grâce à des anticorps, ils ont vu qu’Otop2l se localise non seulement dans la membrane externe des cellules minéralisantes, mais aussi sur les membranes de grandes vésicules internes. Lorsqu’ils ont réduit les niveaux d’Otop2l avec un bloqueur génétique ciblé, les cellules et leurs vésicules sont devenues moins réactives aux changements de pH externe, indiquant que ce canal constitue une voie majeure pour la sortie des protons. Des enregistrements électriques dans des œufs de grenouille et des cellules humaines modifiées pour produire Otop2l ont montré que le canal s’ouvre largement en conditions alcalines et en présence de calcium et de magnésium — exactement la situation dans les vésicules calcifiantes. En substance, les cellules exploitent leur différence de potentiel naturelle à travers la membrane, conjointement avec Otop2l, pour expulser l’acide sans dépenser beaucoup d’énergie métabolique.
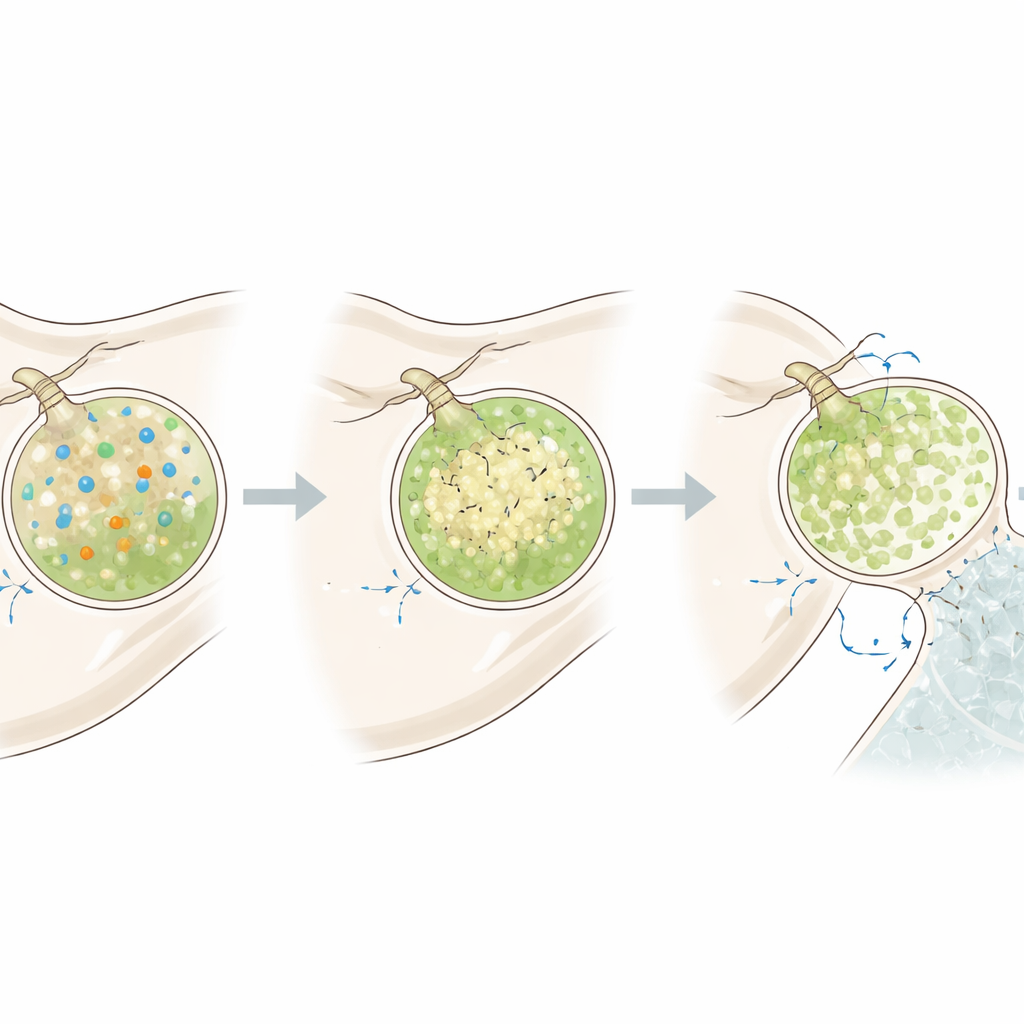
Des vésicules prêtes à intensifier la réparation
L’équipe a ensuite exploré ce qui se passe lorsque les larves doivent reconstruire leur squelette après une lésion. Ils ont dissous les squelettes larvaires en exposant brièvement les larves à de l’eau de mer à faible pH, puis les ont replacées en eau normale et ont suivi les vésicules pendant la repousse. Pendant cette phase de forte demande, les cellules minéralisantes ont produit davantage de vésicules au total, avec une nette augmentation des vésicules alcalines et riches en calcium. Ces vésicules récupéraient leur pH élevé plus rapidement après une impulsion acide, et l’intérieur des cellules devenait lui aussi plus alcalin. Pourtant, le potentiel électrique des cellules est resté similaire, ce qui implique qu’elles s’ajustent principalement en augmentant l’apport en carbonate et la conductance aux protons plutôt qu’en modifiant fondamentalement leur état électrique.
Pourquoi l’acidification des océans importe
Pris ensemble, les résultats soutiennent un modèle dans lequel les cellules minéralisantes d’oursin fonctionnent comme un système « ouvert » : elles endocytent en continu l’eau de mer, concentrent le carbone dans les vésicules et comptent sur les canaux à protons et la tension membranaire pour refouler l’excès d’acide vers l’océan environnant. Ce dispositif est efficace tant que le pH externe reste dans la plage étroite et stable qui caractérise une grande partie de l’histoire récente de la Terre. Mais si l’eau de mer devient plus acide — comme c’est le cas aujourd’hui avec l’augmentation du dioxyde de carbone — ce flux sortant de protons peut s’affaiblir voire s’inverser. Ce travail offre donc un éclairage mécanistique sur la raison pour laquelle de nombreux calcificateurs marins peinent sous l’acidification des océans : les mêmes canaux qui rendaient autrefois la biominéralisation peu coûteuse et robuste peuvent devenir des faiblesses dans un milieu qui change rapidement.
Citation: Jonusaite, S., Przibylla-Diop, C., Musinszki, M. et al. Proton channels govern vesicular carbonate chemistry in mineralizing cells of a marine calcifier. Nat Commun 17, 2578 (2026). https://doi.org/10.1038/s41467-026-70837-x
Mots-clés: biominéralisation, larves d’oursin, canaux à protons, acidification des océans, carbonate de calcium