Clear Sky Science · fr
Des mécanorécepteurs aptamères synthétiques permettent la détection de forces spécifiques aux cellules et le contrôle temporel via des circuits d’ADN
Écouter les cellules par de légères tractions
Nos organismes sont peuplés de cellules qui poussent et tirent en permanence sur leur environnement, utilisant de petites forces pour décider quand croître, se déplacer ou se différencier. Cette étude décrit une nouvelle manière d’intercepter ces forces à l’aide de dispositifs à base d’ADN pouvant être ajustés à des types cellulaires spécifiques et activés ou désactivés dans le temps. Une telle technologie pourrait un jour aider les ingénieurs à guider la croissance tissulaire, comprendre le comportement des tumeurs ou concevoir des matériaux intelligents réagissant en temps réel aux cellules vivantes.
Utiliser l’ADN comme un minuscule interrupteur mécanique
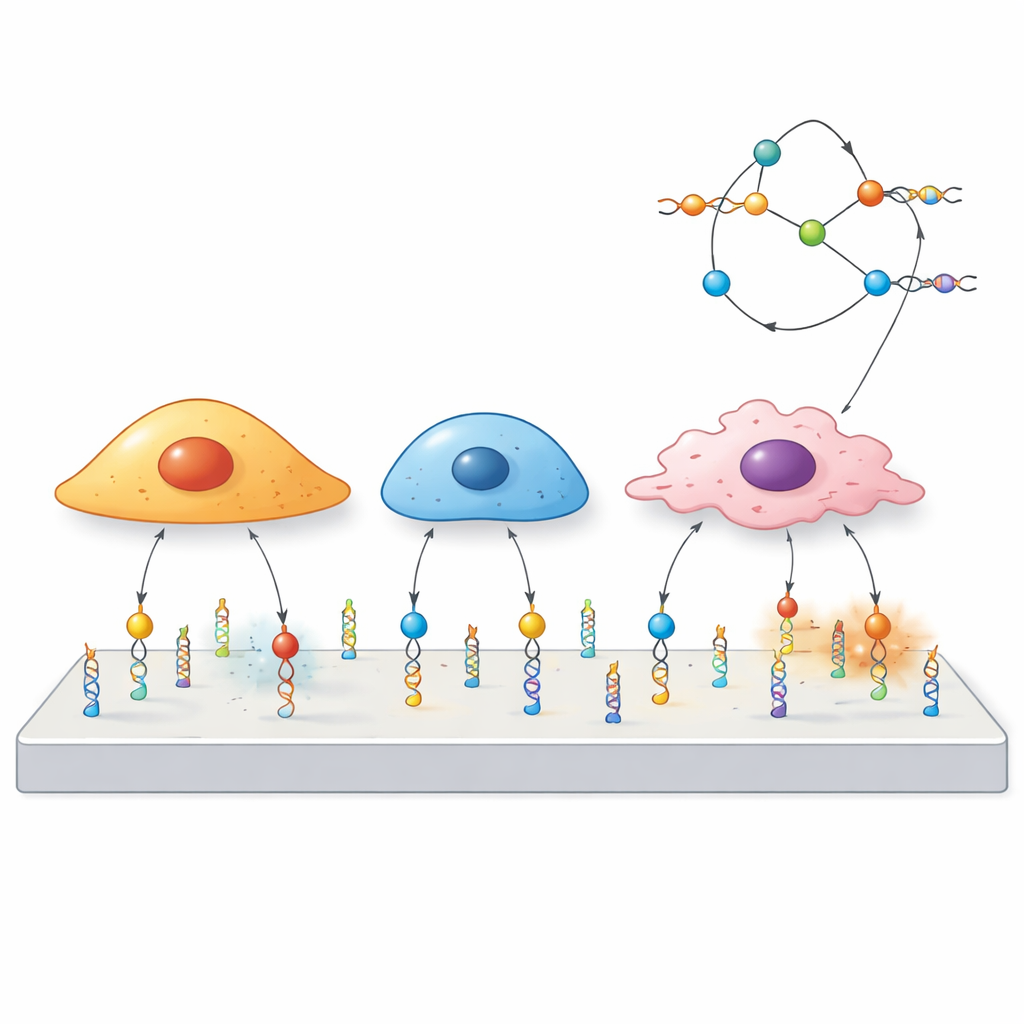
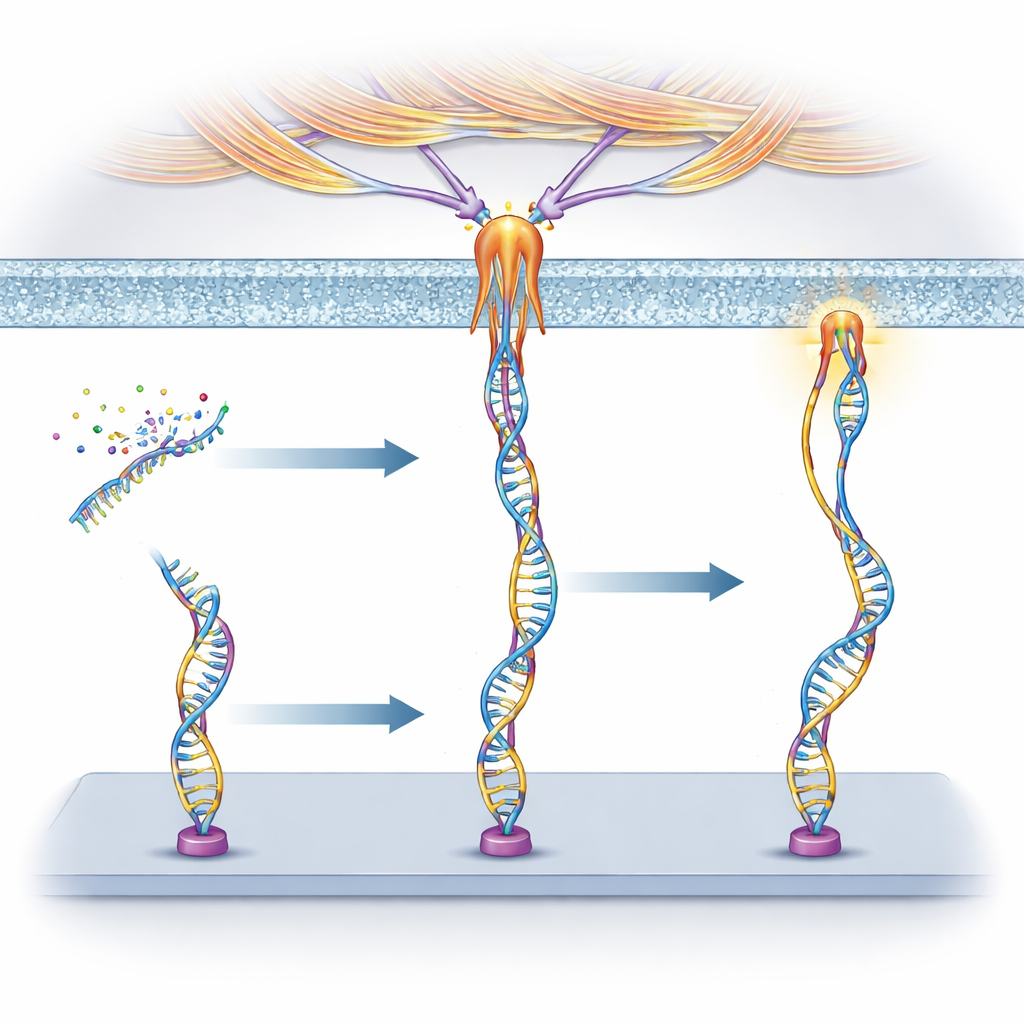
Les chercheurs ont construit des « mécanoprobles » en ADN, la même molécule qui porte l’information génétique. Chaque sonde comporte trois parties : une courte séquence d’ADN appelée aptamère qui se lie à une protéine choisie à la surface cellulaire, un segment d’ADN apparié qui agit comme un ressort calibré pour se rompre à une force donnée, et un colorant fluorescent qui s’allume lorsque ce ressort se dénoue. Lorsqu’une cellule tire suffisamment fort sur le récepteur auquel l’aptamère est fixé, le duplex d’ADN s’ouvre et le signal s’active. Comme différents aptamères ciblent différents récepteurs, l’équipe peut décider à l’avance quelles cellules ou quelles protéines pourront déclencher la sonde.
Mettre au jour des voies de force cachées à la surface des cellules
La plupart des capteurs de force existants se concentrent sur les intégrines, des protéines bien connues qui aident les cellules à s’accrocher à leur environnement mais sont présentes dans de nombreux types cellulaires, ce qui réduit la sélectivité. Ici, l’équipe a au contraire ciblé des récepteurs « non-canoniques » qui ne sont pas habituellement considérés comme mécaniques. Ils ont montré qu’un aptamère nommé AS1411, qui se lie à une protéine appelée nucléoline fréquente sur les cellules cancéreuses, ne produisait un signal que lorsqu’il reconnaissait spécifiquement sa cible. En concevant des sondes nécessitant des forces plus faibles ou plus fortes pour s’ouvrir, ils ont découvert que la nucléoline transmet des forces modestes comparées aux intégrines et n’aide pas, à elle seule, à l’étalement cellulaire sur une surface. En revanche, un autre aptamère, Sgc8, qui reconnaît le récepteur PTK7, a pu rapporter des forces même lorsque les cellules adhéraient à peine, formant des motifs annulaires suggérant une source de mouvement différente.
Tracer l’origine des forces
Pour comprendre ce qui tirait sur ces dispositifs en ADN, les chercheurs ont utilisé des médicaments bloquant sélectivement différents processus cellulaires. Pour la nucléoline, ils ont constaté que ses forces dépendaient fortement de la myosine, la même protéine motrice impliquée dans la contraction musculaire, et apparaissaient aux sites où la cellule forme des adhésions focales — des points de contact spécialisés pour s’accrocher et détecter la rigidité. Cela suggère que la nucléoline est liée indirectement à la machinerie actine–myosine interne de la cellule et peut partager ses forces contractiles. Pour PTK7, en revanche, bloquer un processus appelé macropinocytose — où la cellule fronce sa membrane et engloutit du fluide — réduisait fortement les signaux. Les forces provenaient principalement des premiers frémissements membranaires alimentés par la croissance de l’actine, et non des étapes ultérieures de scellement des vésicules, révélant une voie mécanique distincte.
Ajuster la sélectivité cellulaire avec une précision moléculaire
Parce que chaque aptamère reconnaît un récepteur de surface particulier, le même échafaudage d’ADN peut être reprogrammé simplement en remplaçant un aptamère par un autre. L’équipe l’a démontré avec des sondes pour trois cibles différentes — PTK7, mucine-1 et EpCAM — sur un panel de lignées cellulaires cancéreuses exprimant ces protéines en niveaux élevés ou faibles. Les cellules riches en un récepteur donné produisaient des signaux forts, tandis que celles ayant peu de récepteur répondaient à peine, même lorsqu’elles étaient mélangées dans le même milieu. De façon frappante, des cellules partageant le même récepteur pouvaient néanmoins montrer des motifs spatiaux de force différents, soulignant que le flux de force à travers un récepteur dépend non seulement de sa présence mais aussi du câblage interne propre à chaque type cellulaire.
Programmer quand les cellules peuvent tirer
Profitant du fait que les aptamères sont fabriqués en ADN, les chercheurs ont connecté leurs sondes à des réseaux de réactions d’ADN qui contrôlent si l’aptamère peut se lier ou non. Des brins complémentaires « bloqueurs » peuvent temporairement masquer l’aptamère, et des brins « activateurs » peuvent ensuite enlever les bloqueurs par une réaction d’échange de brins, restaurant la sensibilité aux forces. Ils ont également conçu un bloqueur à base d’ARN qui peut être coupé par une enzyme appelée RNase H, et ont ralenti cette coupure à l’aide de molécules leurres compétitionnant pour l’enzyme. De cette manière, ils ont transformé la mécanosurveillance en un programme temporel : les cellules ne pouvaient générer un signal qu’après un délai intégré ou dans des fenêtres temporelles choisies.
Pourquoi c’est important pour les matériaux vivants de demain
Concrètement, ce travail transforme l’ADN en une serrure mécanique intelligente qui ne s’ouvre que pour certaines cellules, seulement sous certaines forces et uniquement à des moments choisis. En révélant que des récepteurs moins évidents comme la nucléoline et PTK7 peuvent véhiculer de l’information mécanique via des voies très différentes au sein des cellules, il élargit notre vision de la façon dont les cellules « ressentent » leur environnement. Comme l’ensemble du système est construit à partir d’acides nucléiques, il peut s’intégrer directement à la boîte à outils en rapide expansion des circuits et nanodispositifs à base d’ADN. Cela crée une base pour des matériaux et des tissus conçus qui non seulement détectent quand les cellules poussent ou tirent, mais réagissent aussi par des actions biochimiques minutieusement programmées, pouvant guider la réparation, la croissance ou le traitement du cancer de manière hautement programmable.
Citation: Xu, T., Sethi, S., Drees, C. et al. Synthetic aptamer mechanoreceptors enable cell-specific force sensing and temporal control via DNA circuits. Nat Commun 17, 2492 (2026). https://doi.org/10.1038/s41467-026-70765-w
Mots-clés: mécanotransduction, aptamères d’ADN, mécanique cellulaire, biologie synthétique, réseaux de réactions d’ADN