Clear Sky Science · fr
Frazzled/DCC dirige l’intégration spatiale des progéniteurs pour assurer le renouvellement intestinal en état d’équilibre
Comment l’intestin se renouvelle discrètement
Chaque jour, les cellules qui tapissent nos intestins s’usent et doivent être remplacées, pourtant l’organe conserve sa forme et sa taille avec une précision remarquable. Cette étude, utilisant la mouche du vinaigre comme modèle, dévoile un système de guidage caché qui indique aux cellules intestinales nouvellement nées exactement où aller pour combler de minuscules brèches dans l’épithélium. Comprendre ce « contrôle du trafic cellulaire » clarifie non seulement la façon dont les organes saines se maintiennent, mais éclaire aussi comment des signaux de guidage semblables peuvent être détournés lors de la propagation du cancer.
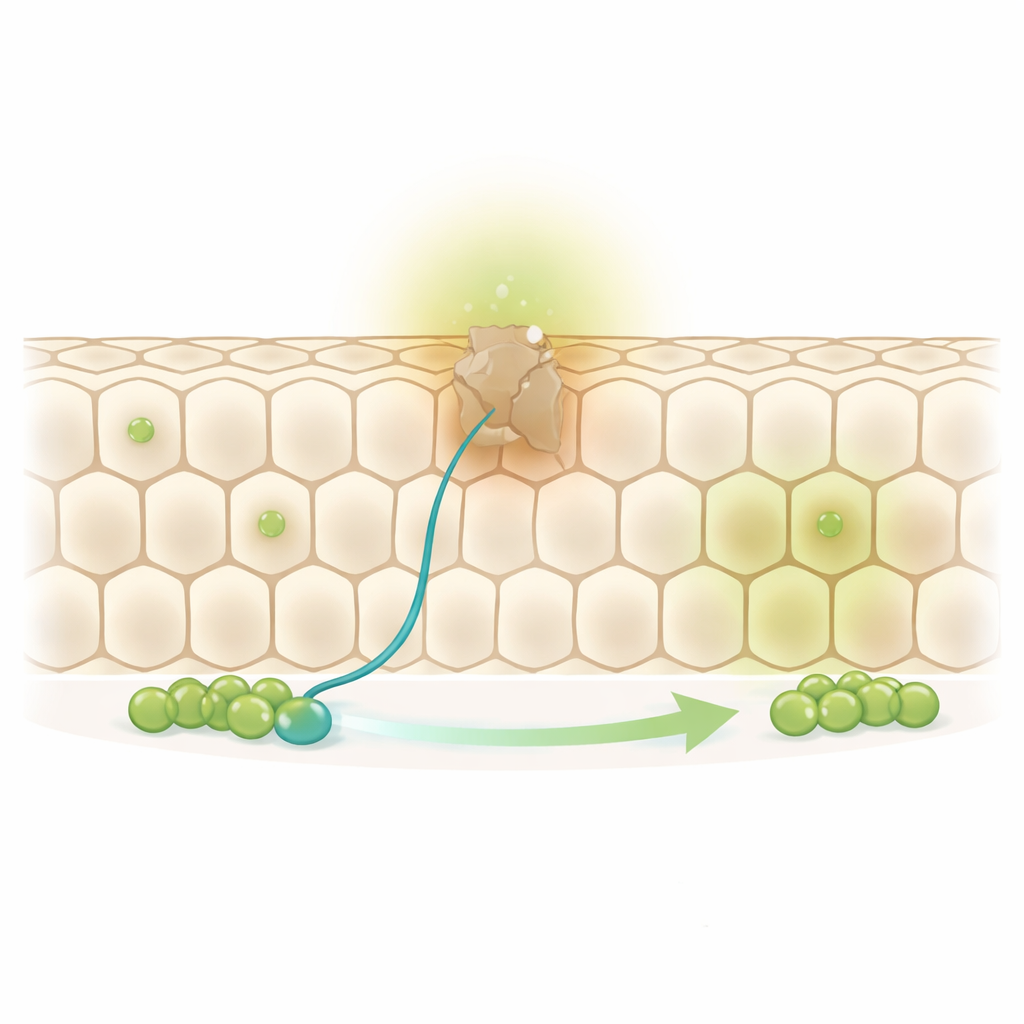
Un alvéole en mouvement constant
Le midgut de la mouche est recouvert d’une seule couche de grandes cellules absorbantes disposées comme un nid d’abeilles. À la base de cette couche se trouvent des cellules souches dispersées et leurs filles immédiates, appelées progéniteurs. Lorsqu’une cellule absorbante arrive en fin de vie, une cellule souche se divise et sa fille progénitrice finit par remplacer la voisine usée. Cependant, les auteurs ont remarqué qu’environ un tiers des cellules de ce réseau n’ont pas de cellule souche ou de progéniteur directement adjacent. Cela pose un casse-tête : comment ces cellules « hors de portée » sont-elles renouvelées sans laisser de trous dans la barrière ?
Des nouvelles cellules en mouvement
En suivant des événements de remplacement individuels pendant une semaine, les chercheurs ont constaté que ces cellules éloignées sont renouvelées aussi souvent que celles situées juste à côté d’une cellule souche. Cela implique que les progéniteurs doivent se déplacer. En effet, l’équipe a observé que les progéniteurs étendent de longues et fines protrusions — des « antennes » cellulaires — plus longues et plus fréquentes que celles des cellules souches elles-mêmes. Ces protrusions ne sont pas aléatoires : dans des conditions normales, elles sont principalement orientées vers des voisines plus âgées et non remplacées plutôt que vers des cellules fraîchement renouvelées, suggérant un comportement actif de recherche et de secours ciblant les cellules les plus en besoin de remplacement.
Un signal de guidage nerveux réutilisé pour l’intestin
Pour comprendre comment ces protrusions sont orientées, les auteurs se sont intéressés à une famille de molécules mieux connue pour le câblage cérébral : les Netrines et leurs récepteurs Frazzled/DCC et Unc-5. Dans le système nerveux, les Netrines agissent comme des balises à longue portée qui attirent ou repoussent les fibres nerveuses en croissance. Dans l’intestin de la mouche, l’équipe a montré que les récepteurs Frazzled/DCC et Unc-5 se trouvent spécifiquement sur les progéniteurs, concentrés dans leurs protrusions. Les cellules absorbantes usées, elles, commencent à produire et à libérer une Netrine appelée Netrin-B. Lorsque les chercheurs ont augmenté la quantité de Netrin-B dans des cellules sélectionnées, les progéniteurs voisins ont développé des protrusions plus longues orientées vers la source, puis ont migré pour occuper cet emplacement. Lorsqu’ils ont bloqué Netrin-B ou désactivé Frazzled, les protrusions se sont raccourcies, les cellules éloignées n’étaient plus remplacées efficacement, et les mouches mouraient plus tôt, soulignant combien ce guidage est vital pour la santé intestinale.
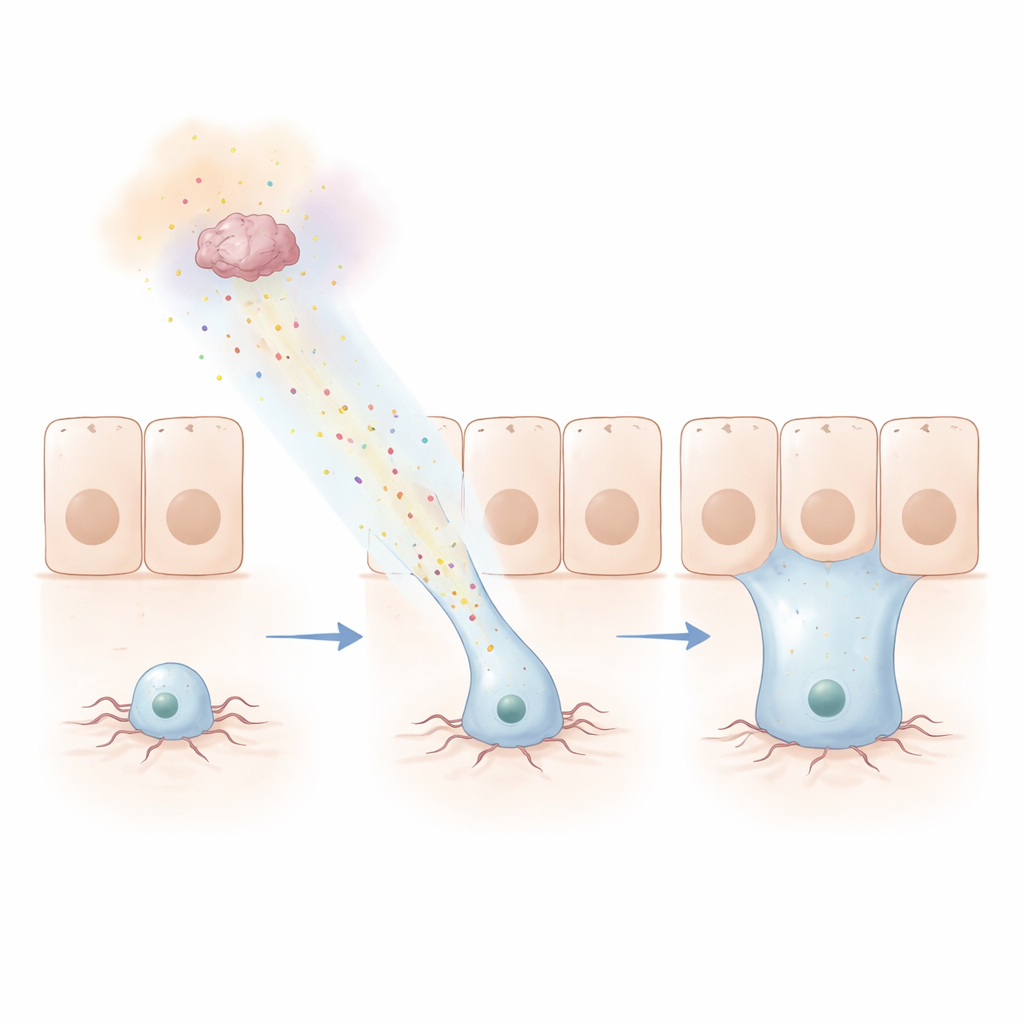
Suivre une piste chimique
Pour mesurer jusqu’où ce signal peut agir, l’équipe a conçu un astucieux test « Hamelin », nommé d’après le joueur de flûte. Ils ont fait sécréter des Netrines par un anneau de cellules à la jonction entre régions intestinales, tout en marquant fluorescentement des progéniteurs à distance. Sur plusieurs jours, des progéniteurs ont migré jusqu’à plusieurs dizaines de micromètres vers la source, franchissant même une frontière nette vers une couche tissulaire différente et s’y intégrant. Des versions humaines des Netrines et du récepteur DCC pouvaient remplacer leurs homologues de mouche et guider encore ces mouvements, montrant que le mécanisme est profondément conservé. La même machinerie d’actine qui propulse le mouvement cellulaire ailleurs dans l’organisme était requise : lorsque des composants clés étaient supprimés, les protrusions et le renouvellement à longue portée échouaient.
Pourquoi cela compte pour la santé et la maladie
En termes simples, ce travail révèle que l’intestin ne dépend pas uniquement de la pression locale de division cellulaire pour renouveler son épithélium. Au lieu de cela, les cellules mourantes envoient un signal chimique d’« aide », Netrin‑B, qui attire des progéniteurs spécifiques équipés de récepteurs Frazzled/DCC. Ces progéniteurs étendent des antennes le long du gradient, rampent vers la cellule vieillissante et se glissent en place pour maintenir l’intégrité de la barrière. Comme le même système Netrin–DCC est actif chez les mammifères et a été lié à l’invasion tumorale et aux métastases, les résultats obtenus chez la mouche apportent un soutien mécanistique concret à l’idée que ces molécules sont à double tranchant : essentielles à une réparation ordonnée des tissus sains, mais potentiellement dangereuses lorsqu’elles sont mal régulées dans des tumeurs qui apprennent à migrer et à coloniser de nouveaux organes.
Citation: Zipper, L., Ramon-Cañellas, P., Akkas-Gazzoni, F. et al. Frazzled/DCC directs spatial progenitor integration ensuring steady-state intestinal turnover. Nat Commun 17, 2491 (2026). https://doi.org/10.1038/s41467-026-70704-9
Mots-clés: cellules souches intestinales, migration cellulaire, signalisation netrine, homéostasie tissulaire, métastase cancéreuse