Clear Sky Science · fr
Dysfonctionnement du métabolisme microbien des fibres de l’intestin grêle dans la maladie cœliaque
Pourquoi l’usine à fibres de l’intestin compte dans la maladie cœliaque
La maladie cœliaque est généralement expliquée comme un problème lié au gluten, la protéine du blé, du seigle et de l’orge. Mais cette étude pose une question différente : que deviennent les micro-organismes vivant dans l’intestin grêle, et comment traitent-ils les fibres alimentaires, lorsqu’une personne est atteinte de la maladie cœliaque ? Les réponses suggèrent qu’une « usine » à fibres défaillante dans l’intestin supérieur pourrait ralentir la guérison, et que le bon type de fibres associé aux bons microbes pourrait un jour faire partie du traitement.
Problème lié au gluten et équipe de soutien manquante
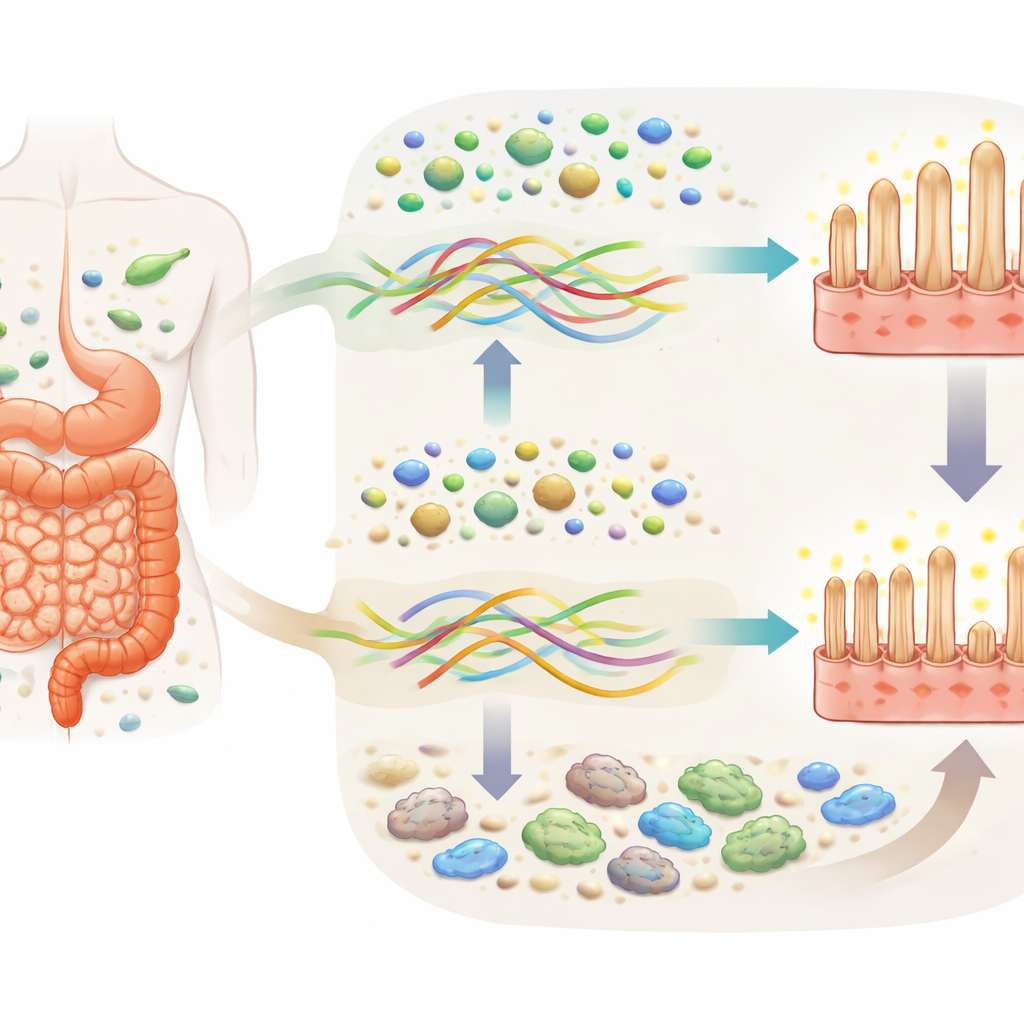
La maladie cœliaque est une affection immunitaire dans laquelle la consommation de gluten déclenche une inflammation et des lésions dans la première partie de l’intestin grêle. Cette zone, appelée duodénum, possède normalement des projections en forme de doigts (villosités) qui absorbent les nutriments. Dans la maladie cœliaque, ces villosités régressent et la muqueuse se remplit de cellules immunitaires activées. La plupart des personnes s’améliorent avec un régime strict sans gluten, mais la récupération peut être lente et incomplète. Parallèlement, de nombreux produits sans gluten sont pauvres en fibres, ce qui soulève des questions sur l’impact de cela sur les microbes intestinaux qui dépendent des fibres comme principale source d’énergie.
Un microbiome affaibli pour utiliser les fibres
Les chercheurs ont prélevé des liquides du duodénum et des échantillons de selles auprès de trois groupes : des personnes nouvellement diagnostiquées atteintes de la maladie cœliaque, des patients cœliaques en bonne santé sous régime sans gluten, et des témoins sains. Ils ont cartographié les bactéries présentes et utilisé des outils informatiques et des tests génétiques pour estimer les capacités fonctionnelles de ces microbes. Chez les patients nouvellement diagnostiqués comme chez les patients traités, la communauté du petit intestin était moins diversifiée et contenait moins de bactéries dégradant les fibres appartenant à un groupe appelé Prevotellaceae. Les gènes participant à la dégradation des amidons et des fibres de type inuline étaient également réduits. Fait important, ces déficits semblaient présents même lorsque l’apport en fibres des personnes n’était pas sensiblement différent, ce qui indique une perte intrinsèque de la capacité microbienne plutôt qu’un simple manque de fibres dans l’alimentation.
Apport en fibres, alimentation quotidienne et composés intestinaux
Pour comprendre comment le régime pouvait influencer ces changements, l’équipe a estimé l’apport en fibres à l’aide de questionnaires alimentaires et a analysé l’ADN végétal dans les selles pour voir quels types de plantes les participants consommaient réellement. Beaucoup de participants dans tous les groupes consommaient moins de fibres que ce que recommandent les autorités de santé, et les personnes atteintes de la maladie cœliaque sous traitement se tournaient souvent davantage vers le riz et moins vers les céréales contenant du gluten. Pourtant cela n’expliquait pas entièrement les différences microbiennes. Lorsque les scientifiques ont mesuré les acides gras à chaîne courte—de petites molécules produites lors de la digestion des fibres par les microbes—ils ont constaté que les personnes atteintes de forme active de la maladie cœliaque présentaient les niveaux les plus bas, tandis que les patients traités montraient une récupération partielle. Ce schéma soutient l’idée que la machinerie de traitement des fibres de l’intestin est endommagée dans la maladie cœliaque mais peut s’améliorer une fois le gluten éliminé.
Tester les fibres et des bactéries utiles chez la souris
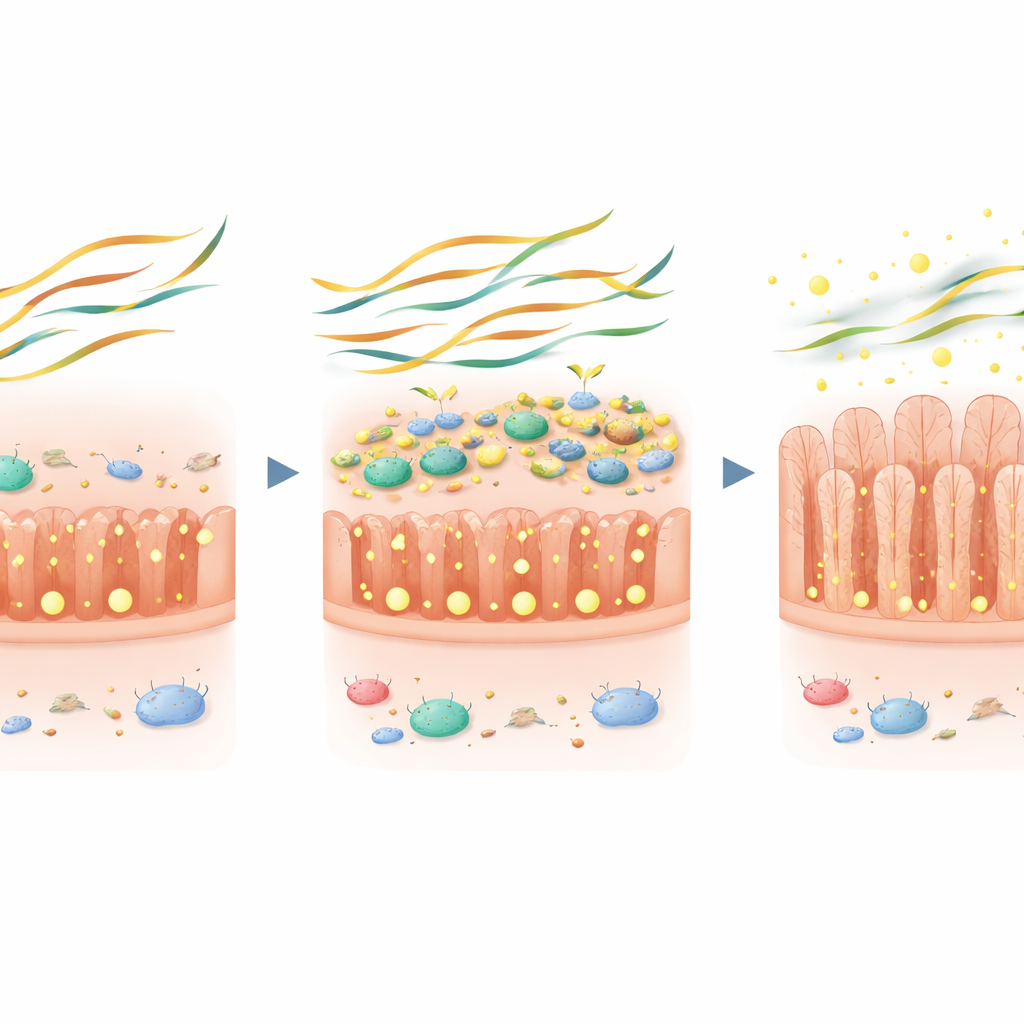
Pour explorer la causalité, l’équipe a utilisé des souris porteuses d’un gène humain de risque pour la maladie cœliaque et pouvant être sensibilisées au gluten. Après avoir induit des lésions intestinales liées au gluten, elles ont mis les souris soit sur un régime sans gluten seul, soit sur un régime sans gluten enrichi en inuline (une fibre végétale soluble) ou en un amidon résistant. Les souris recevant de l’inuline présentaient des niveaux plus élevés d’acides gras à chaîne courte dans l’intestin grêle et une guérison plus rapide de la muqueuse, avec moins de cellules inflammatoires et des villosités plus hautes. L’amidon résistant apportait des bénéfices plus modestes. Lorsque la même fibre a été donnée à des souris axéniques (sans microbes), elle a produit peu d’effets bénéfiques, montrant que les microbes sont nécessaires. Enfin, lorsque des souris axéniques ont été colonisées par un cocktail de souches de Prevotella puis nourries à l’inuline, leur intestin grêle a produit davantage de ces acides gras utiles, confirmant que des bactéries spécifiques amatrices de fibres peuvent restaurer cette fonction perdue.
Ce que cela pourrait signifier pour les personnes atteintes de la maladie cœliaque
Pris ensemble, ces résultats suggèrent que la maladie cœliaque n’est pas seulement une histoire de gluten et du système immunitaire. Elle implique aussi une perturbation de « l’économie des fibres » de l’intestin grêle, dans laquelle des bactéries clés et leurs outils de dégradation des fibres disparaissent. L’étude ouvre la voie à un futur où des fibres adaptées comme l’inuline, associées aux partenaires microbiens appropriés, pourraient être utilisées en complément d’un régime sans gluten pour accélérer la guérison de la muqueuse intestinale. Bien que des essais cliniques supplémentaires soient nécessaires avant de modifier les recommandations thérapeutiques, ce travail souligne que soutenir les microbes résidents de l’intestin grêle pourrait devenir une composante importante de la prise en charge des personnes atteintes de la maladie cœliaque.
Citation: Wulczynski, M., Constante, M., Galipeau, H.J. et al. Small intestinal microbial fiber metabolism dysfunction in celiac disease. Nat Commun 17, 2698 (2026). https://doi.org/10.1038/s41467-026-70644-4
Mots-clés: maladie cœliaque, microbiome intestinal, fibres alimentaires, acides gras à chaîne courte, Prevotella