Clear Sky Science · fr
Un actionneur myoneural avec biophysique conçue pour des systèmes biohybrides implantables
Reconstruire les muscles en tant que machines vivantes intelligentes
Imaginez que les médecins puissent transformer le muscle d’une personne en un moteur vivant qui ne se fatigue jamais, pilotable par un ordinateur et pouvant rester sans danger à côté d’organes délicats pendant des années. Cette étude décrit une méthode pour y parvenir. Les chercheurs conçoivent un « actionneur myoneural » chez le rat — un muscle dont l’innervation est délibérément réorganisée afin qu’il puisse être commandé par de l’électronique, résister à la fatigue et conserver un comportement de tissu naturel. De tels actionneurs vivants pourraient un jour restaurer le mouvement, soutenir des organes défaillants ou fournir des sensations réalistes pour des prothèses avancées.
Pourquoi les muscles vivants font de meilleurs moteurs
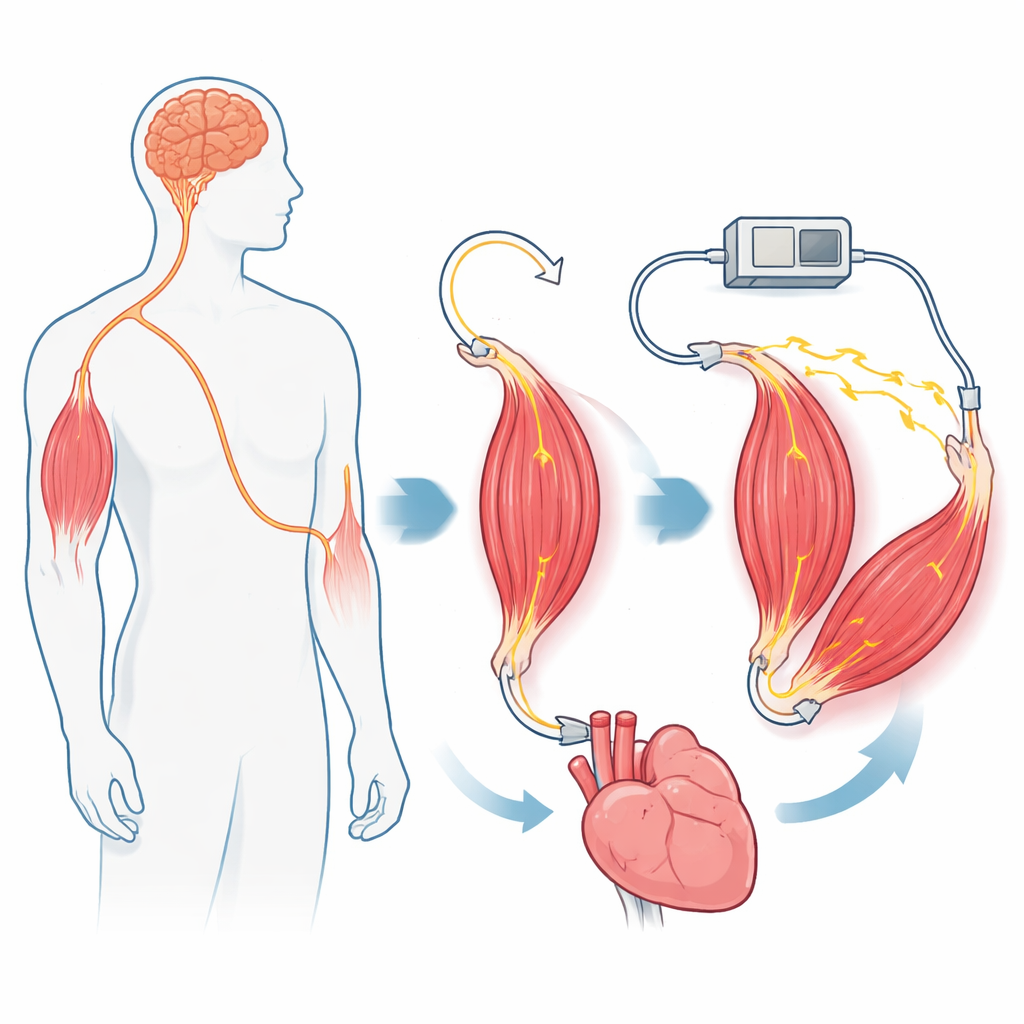
Les moteurs artificiels alimentés par l’électricité, l’air ou des fluides sont puissants, mais ils sont lourds, difficiles à miniaturiser à des tailles compatibles avec le corps et composés de matériaux qui ne s’intègrent pas bien au tissu vivant. En revanche, le muscle squelettique est léger, économe en énergie, capable d’autoréparation et déjà conçu pour fonctionner à l’intérieur du corps. Il peut croître, s’adapter et répondre à de minuscules signaux nerveux. Cependant, lorsque les muscles sont contrôlés directement par des impulsions électriques d’un dispositif implanté, ils se fatiguent rapidement. Cette fatigue survient parce que la stimulation électrique standard tend à recruter en premier les fibres les plus grosses et les plus rapides, mais aussi les moins durables. Pour exploiter le muscle comme moteur implantable fiable, l’équipe a dû modifier l’organisation et le recrutement de ses fibres nerveuses — sans compromettre la santé et la durabilité naturelles du muscle.
Échanger les voies nerveuses pour réécrire le contrôle
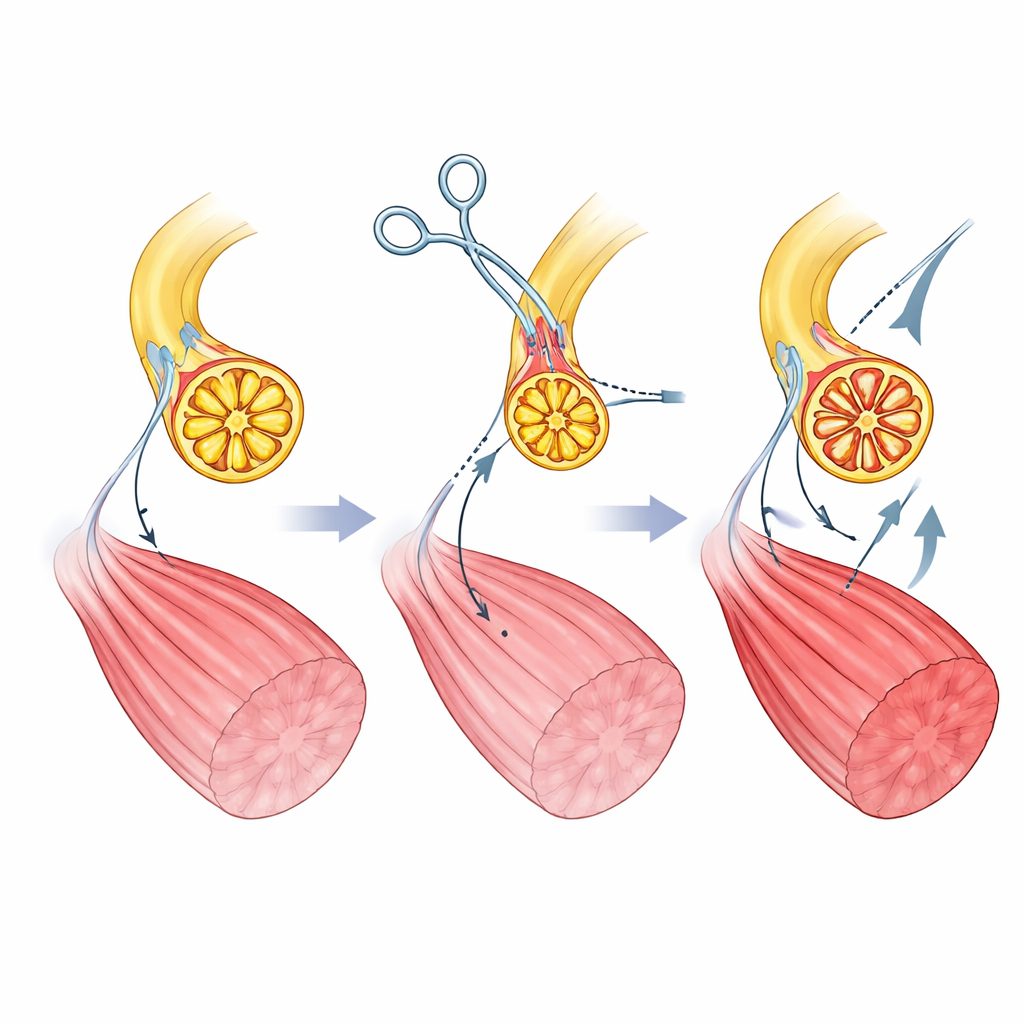
Les auteurs créent leur actionneur myoneural chez le rat en reconnectant chirurgicalement un muscle de la patte. Ils sectionnent d’abord le nerf moteur normal qui véhicule les commandes de la moelle épinière et empêchent sa repousse. Puis ils dirigent un nerf différent — celui qui transporte habituellement des signaux de toucher et d’étirement depuis la peau et les tissus — directement dans le muscle. Au fil du temps, ce nerf « sensitif » régénère à l’intérieur du muscle et forme de nouveaux points de contact avec les fibres musculaires. La microscopie montre que ces nouvelles jonctions ressemblent et se comportent comme des connexions motrices normales, et le muscle retrouve sa capacité à se contracter lorsque le nerf sensitif est stimulé électriquement. Fait important, les axones de ce nerf sensitif sont plus uniformes et de plus petit diamètre que ceux du nerf moteur d’origine, ce qui prépare un recrutement des fibres musculaires plus équilibré sous commande informatique.
Des muscles qui continuent de fonctionner sous forte sollicitation
Une fois les muscles réacheminés cicatrisés, l’équipe les soumet à des protocoles d’essais exigeants. Ils comparent les muscles natifs avec les nouveaux actionneurs lors de contractions uniques répétées et lors de longues périodes de contraction continue. Les actionneurs myoneuraux perdent de la force beaucoup plus lentement et montrent une sortie plus régulière dans le temps, avec une amélioration de 260 % de la résistance à la fatigue en travail continu. Leur comportement sur des minutes est fondamentalement différent du muscle non modifié : au lieu d’une chute rapide de la force, la diminution est plus progressive puis se stabilise. Malgré une perte de masse durant le réacheminement, les actionneurs conservent une structure fibreuse saine et produisent une force similaire par unité de masse par rapport au muscle natif, et ils maintiennent leur état pendant au moins 15 semaines même sans exercice ni stimulation supplémentaire.
Contrôle informatique sans perturber le cerveau
Parce que la nouvelle innervation déconnecte le muscle des signaux moteurs normaux du cerveau, toutes les contractions proviennent désormais d’un stimulateur externe. Les chercheurs intègrent le muscle dans une boucle de rétroaction : un capteur mesure la force, un contrôleur ajuste la stimulation nerveuse, et le système suit une force cible choisie sur de nombreux cycles. Les muscles natifs échouent rapidement dans ce dispositif, mais les actionneurs myoneuraux continuent de suivre les consignes. Pour rendre le système plus sûr et plus flexible, l’équipe introduit aussi un « bloc nerveux » réversible. En appliquant un signal électrique à haute fréquence sur le nerf plus près de la moelle épinière, ils empêchent les impulsions de stimulation d’envoyer des signaux indésirables vers le système nerveux central tout en permettant toujours la réponse côté muscle. Dans les tests, l’actionneur a continué de générer des forces contrôlées tandis que le cerveau restait effectivement isolé de la stimulation artificielle.
Des membres bioniques au soutien d’organes défaillants
Pour démontrer les usages possibles de ce moteur vivant, les auteurs construisent deux systèmes de démonstration chez le rat. Dans le premier, ils couplent l’actionneur en série avec un autre muscle jouant le rôle du muscle résiduel au niveau d’un site d’amputation. En resserrant ou relâchant cette paire, ils modifient l’étirement du muscle résiduel et, par conséquent, l’activité de ses fibres nerveuses sensorielles — ajustant en quelque sorte la sensation de position et de force du membre. Cette « interface mécanoneurale proprioceptive » pourrait fournir éventuellement un retour naturel depuis des membres robotiques ou des avatars virtuels. Dans le second système, ils enroulent l’actionneur autour d’une section d’intestin grêle remplie de liquide. Lorsqu’il est commandé par stimulation nerveuse, le muscle comprime et relâche le segment intestinal, et le suivi du mouvement montre que l’organe se déplace de concert avec l’actionneur. Cela suggère des dispositifs futurs capables de prêter une force mécanique à des organes affaiblis comme l’intestin, la vessie ou même le cœur.
Ce que cela pourrait signifier pour la médecine de demain
Globalement, ce travail montre qu’en réacheminant soigneusement les nerfs, le muscle d’une personne peut être transformé en un actionneur résistant à la fatigue, piloté par ordinateur, qui conserve un comportement de tissu natif et peut être électriquement isolé du cerveau si nécessaire. Comme l’approche repose sur des techniques chirurgicales et des électrodes proches des outils cliniques existants, elle pourrait être plus facile à traduire en application clinique que des implants entièrement synthétiques ou des tissus cultivés en laboratoire. Si des actionneurs myoneuraux similaires peuvent être construits et contrôlés en toute sécurité chez l’humain, ils pourraient constituer le cœur de nouveaux systèmes biohybrides visant à restaurer la sensation des membres, assister des organes défaillants et fournir des signaux mécaniques précis au corps sans l’encombrement et la rigidité des machines traditionnelles.
Citation: Song, H., Herrera-Arcos, G., Friedman, G.N. et al. A myoneural actuator with engineered biophysics for implantable biohybrid systems. Nat Commun 17, 2584 (2026). https://doi.org/10.1038/s41467-026-70626-6
Mots-clés: actionneur biohybride, neuroprothèses, fatigue musculaire, régénération nerveuse, soutien d’organes