Clear Sky Science · fr
StrucGAP : une plateforme modulaire, rationalisée et traçable d’exploration de données pour la glycoprotéomique structurale et site-spécifique
Comprendre les manteaux sucrés des protéines
Chaque cellule de notre corps est recouverte d’une forêt de structures sucrées attachées aux protéines. Ces « manteaux sucrés », appelés glycannes, contribuent discrètement à réguler l’adhérence cellulaire, la communication et la réponse à l’environnement. Les appareils modernes peuvent désormais inventorier ces motifs sucrés avec un niveau de détail étonnant, mais les chercheurs sont souvent submergés par le volume et la complexité des données. Cette étude présente StrucGAP, une nouvelle plateforme computationnelle conçue pour transformer ces mesures denses en récits biologiques clairs et significatifs, en prenant le vieillissement de l’utérus de souris comme cas d’étude.
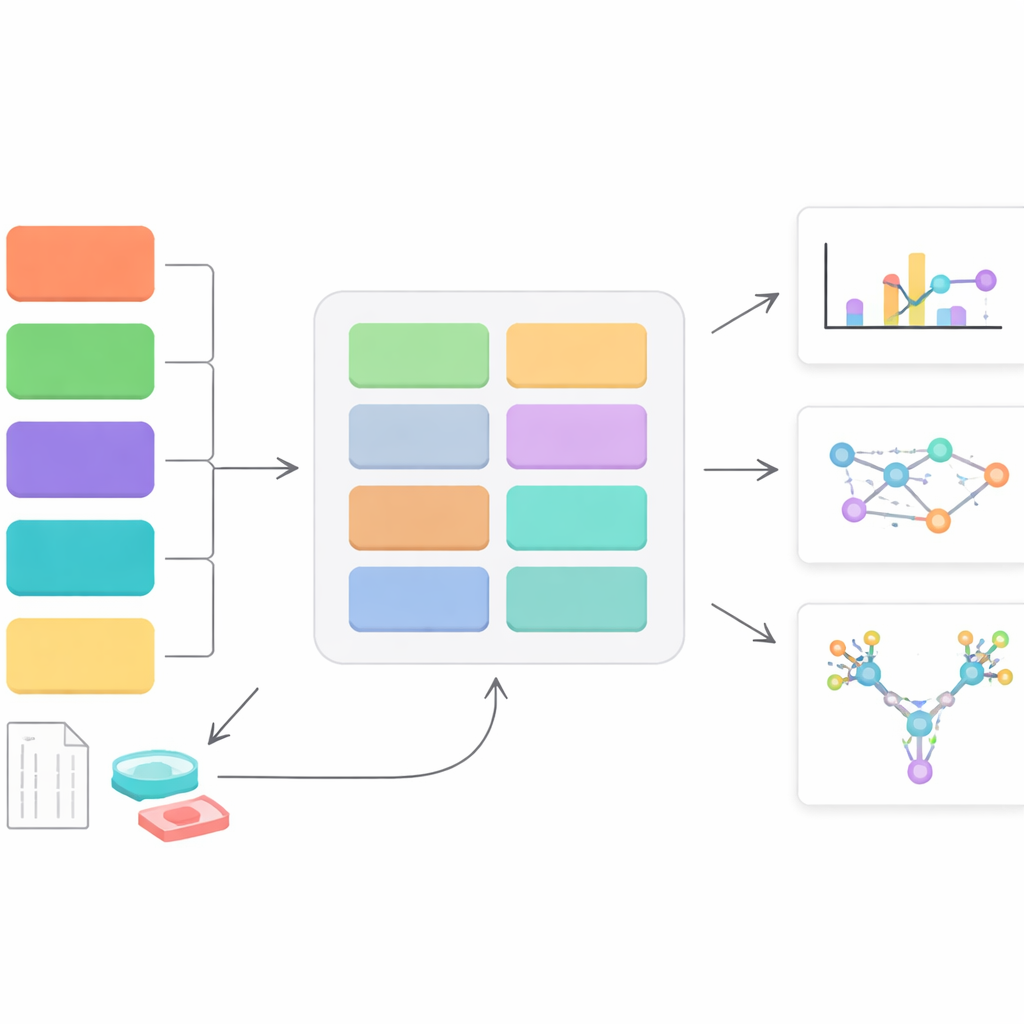
Un nouveau centre de contrôle pour les données de manteaux sucrés
StrucGAP est une plateforme logicielle développée pour analyser un type précis de décoration sucrée : les glycannes N-liés, qui se fixent à des sites particuliers sur les protéines. Plutôt que de viser un outil polyvalent, StrucGAP est conçu dès l’origine pour ce problème spécifique. Il accepte les résultats de plusieurs moteurs de recherche en spectrométrie de masse populaires qui identifient quels glycannes sont présents sur quels sites protéiques. Une fois ces identifications intégrées, StrucGAP les traite via une série de modules qui vérifient la qualité des données, résument les motifs glycanes globaux, suivent l’évolution des sites spécifiques entre conditions et relient ces changements à des fonctions et voies biologiques connues.
Décomposer les sucres complexes en éléments signifiants
La plupart des outils existants considèrent chaque glycan comme un objet unique et indivisible. StrucGAP adopte une approche différente : il décompose chaque glycan en éléments constitutifs plus petits et biologiquement pertinents, tels que des cœurs communs, des schémas de ramification et des motifs connus incluant des résidus fucose ou acides sialiques. Il examine alors non seulement quels glycannes entiers augmentent ou diminuent, mais aussi quels motifs apparaissent plus souvent, moins souvent ou en nouvelles combinaisons. Cette vue par « sous-structures » rend l’analyse plus robuste face aux assignations incertaines et aide à révéler des motifs qui pourraient rester cachés, en particulier lorsque des motifs rares mais importants s’enrichissent dans une condition donnée.
Suivre les changements de sucres pendant le vieillissement utérin
Pour démontrer les capacités de StrucGAP, les auteurs l’ont appliqué à un jeu de données détaillé provenant du tissu utérin de souris femelles jeunes et d’âge moyen. L’expérience brute a identifié plus de vingt mille glycopeptides uniques, chacun correspondant à un site protéique particulier portant un glycan spécifique. StrucGAP a d’abord nettoyé et standardisé les données, puis cartographié la distribution des glycannes sur les sites protéiques et le nombre de variations structurelles présentes à chaque position. L’utérus s’est avéré riche à la fois en glycannes simples de type high-mannose et en types complexes plus élaborés, avec de nombreuses compositions glycanes existant sous forme de multiples isomères structurels. En zoomant sur les sous-structures, la plateforme a catalogué la fréquence d’occurrence et de cooccurrence de différents cœurs, nombres de ramifications et motifs tels que les épitopes Lewis ou des formes particulières d’acide sialique.
Des motifs à la fonction : adhésion et remodelage
Le module quantitatif de StrucGAP a ensuite comparé les utérus jeunes et âgés, trouvant plus d’un millier de glycopeptides augmentés et quelques centaines diminués avec l’âge. Un thème récurrent fut la « fucosylation du cœur » : une manière spécifique dont un résidu fucose se lie au cœur du glycan ; cette modification montrait des variations dans les deux sens, suggérant une régulation finement accordée plutôt qu’un simple interrupteur marche/arrêt. D’autres motifs sont apparus à mesure que les seuils statistiques étaient resserrés : des glycannes plus ramifiés, des motifs de type Lewis spécifiques et des acides sialiques contenant du Neu5Ac se sont enrichis progressivement. En reliant ces caractéristiques structurelles à des bases de données de fonctions géniques et de voies, StrucGAP a montré que les glycannes changeants se concentraient sur des protéines impliquées dans l’adhésion cellulaire, les interactions avec la matrice environnante et le remodelage de l’architecture tissulaire. La plateforme a également mis en relation ces motifs avec les changements des enzymes qui construisent et élaguent les glycannes, ainsi qu’avec les protéines lectines, dessinant des réseaux coordonnés susceptibles de piloter le vieillissement utérin.
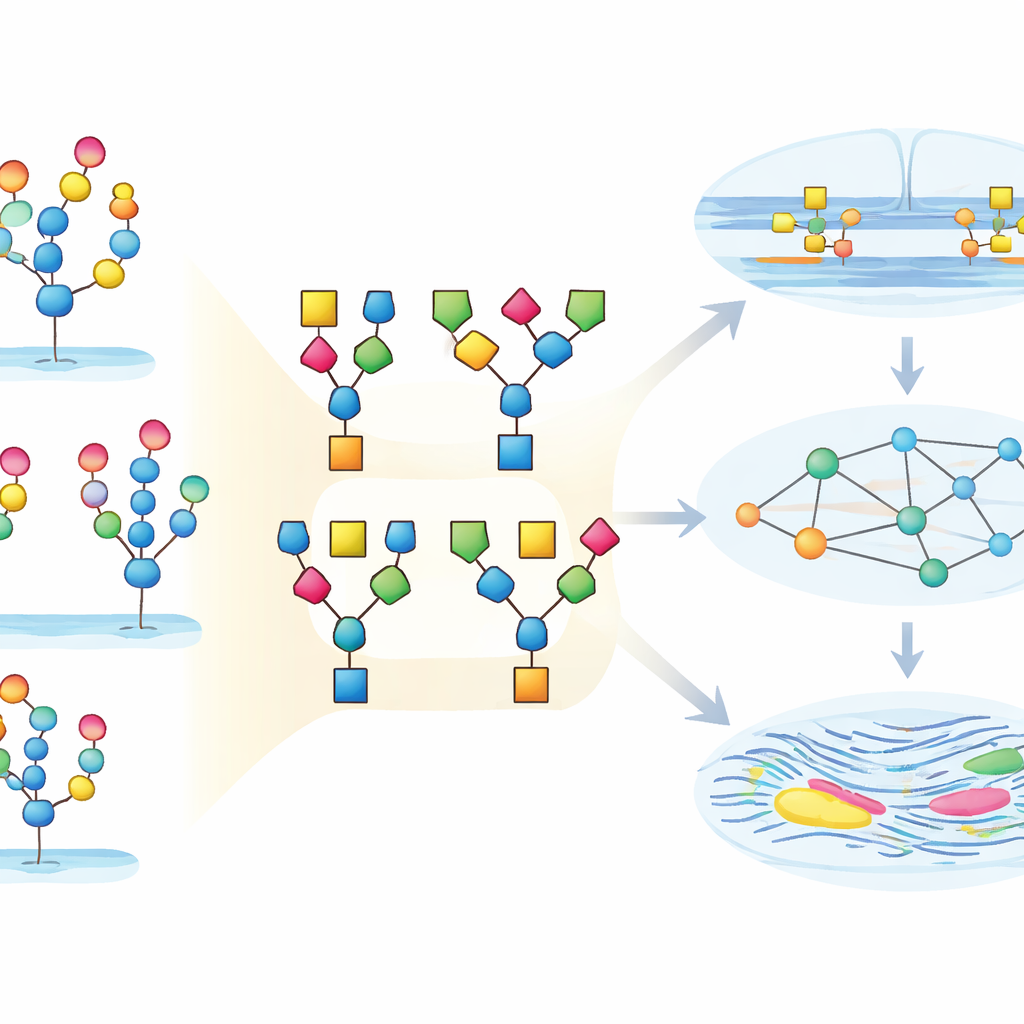
Transformer l’avalanche de données en insight biologique
Concrètement, ce travail montre comment une masse hautement technique de mesures « sucre-sur-protéine » peut être convertie en une carte lisible des changements tissulaires au fil du temps. StrucGAP fait office à la fois de gardien de la qualité et de moteur de narration : il nettoie les données, résume les motifs sucrés clés, les relie aux enzymes qui les façonnent et aux voies qu’ils influencent, et génère automatiquement des graphiques et rapports mettant en évidence les découvertes les plus importantes. Dans l’utérus de souris, cela révèle un basculement coordonné vers des glycannes plus chargés, riches en Neu5Ac et en fucose, associés à l’adhésion et au remodelage tissulaire. Plus généralement, StrucGAP offre aux chercheurs un moyen pratique de passer des données brutes de glycoprotéomique à des hypothèses testables sur la manière dont les manteaux sucrés contribuent à la santé, la maladie et le vieillissement.
Citation: Yang, M., Wu, Y., Zhang, Z. et al. StrucGAP: a modular, streamlined and traceable data mining platform for structural and site-specific glycoproteomics. Nat Commun 17, 2579 (2026). https://doi.org/10.1038/s41467-026-70560-7
Mots-clés: glycoprotéomique, N-glycosylation, plateforme bioinformatique, vieillissement utérin, glycosylation des protéines