Clear Sky Science · fr
Transitions structurelles lors de l’assemblage progressif des particules centrales du protéasome
Comment les cellules se débarrassent des déchets moléculaires
À l’intérieur de chacune de nos cellules, les protéines usées ou endommagées doivent être dégradées avant de s’accumuler comme des ordures. Une immense machine moléculaire appelée protéasome effectue une grande partie de ce nettoyage, et elle est déjà une cible pour des médicaments anticancéreux. Cette étude lève le voile sur la manière dont le cœur catalytique du protéasome se construit étape par étape dans des cellules de levure, révélant des raccourcis inattendus et des mécanismes de sécurité qui garantissent que la machine finale fonctionne avec précision et seulement lorsqu’elle est prête.
Construire un cylindre qui déchiquette les protéines
La partie active du protéasome est un noyau en forme de cylindre composé d’anneaux empilés de sous‑unités protéiques. Ce cylindre abrite des sites de découpe dissimulés qui fragmentent les autres protéines en petits morceaux. Parce qu’activer ces couteaux trop tôt serait dangereux, les cellules assemblent le cylindre au travers d’une série d’intermédiaires partiellement formés. Les auteurs se sont concentrés sur des versions précoces du noyau, appelées complexes précurseurs, qui sont généralement rares et éphémères. En ralentissant légèrement l’une des dernières étapes d’assemblage, ils ont pu capturer et purifier ces formes précoces issues de levure et les imager par cryo‑microscopie électronique à haute résolution, qui fige les molécules en action et révèle leur forme tridimensionnelle.
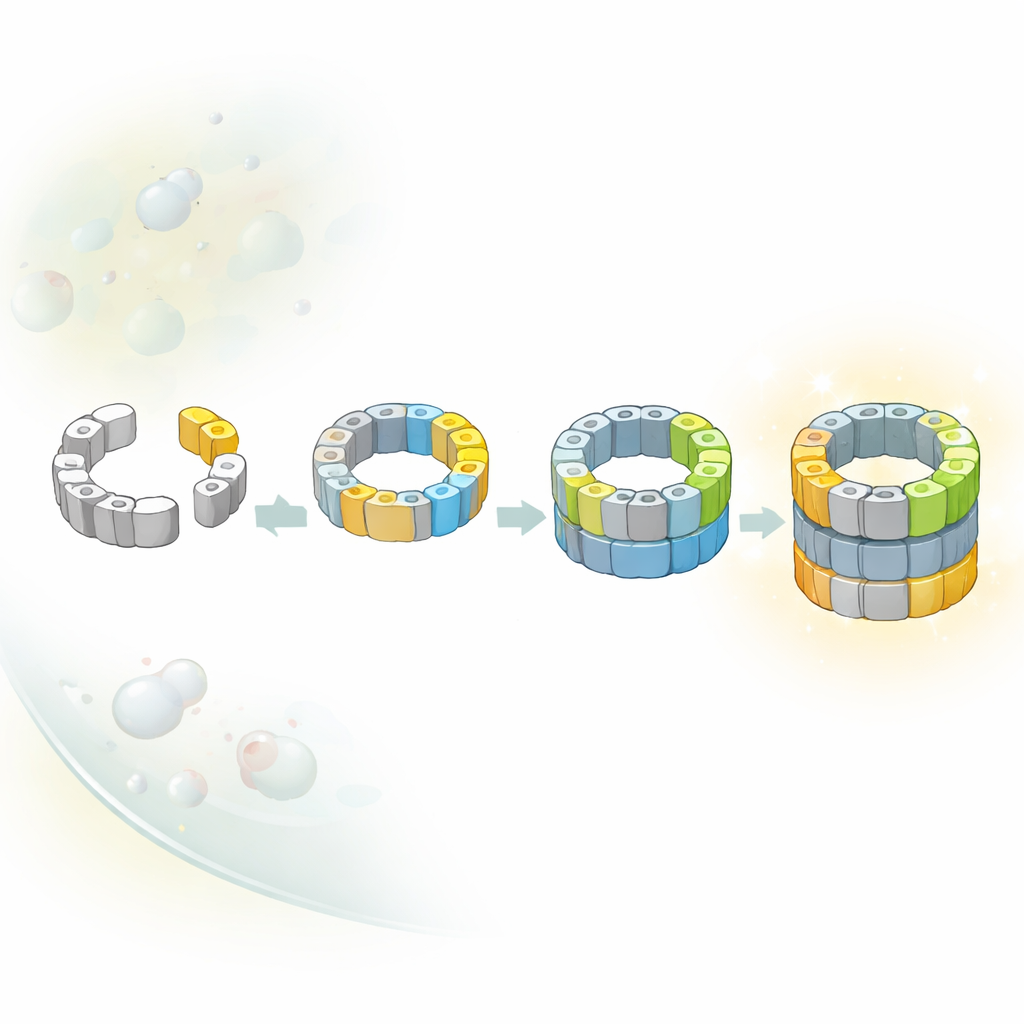
Plusieurs routes pour atteindre le même noyau
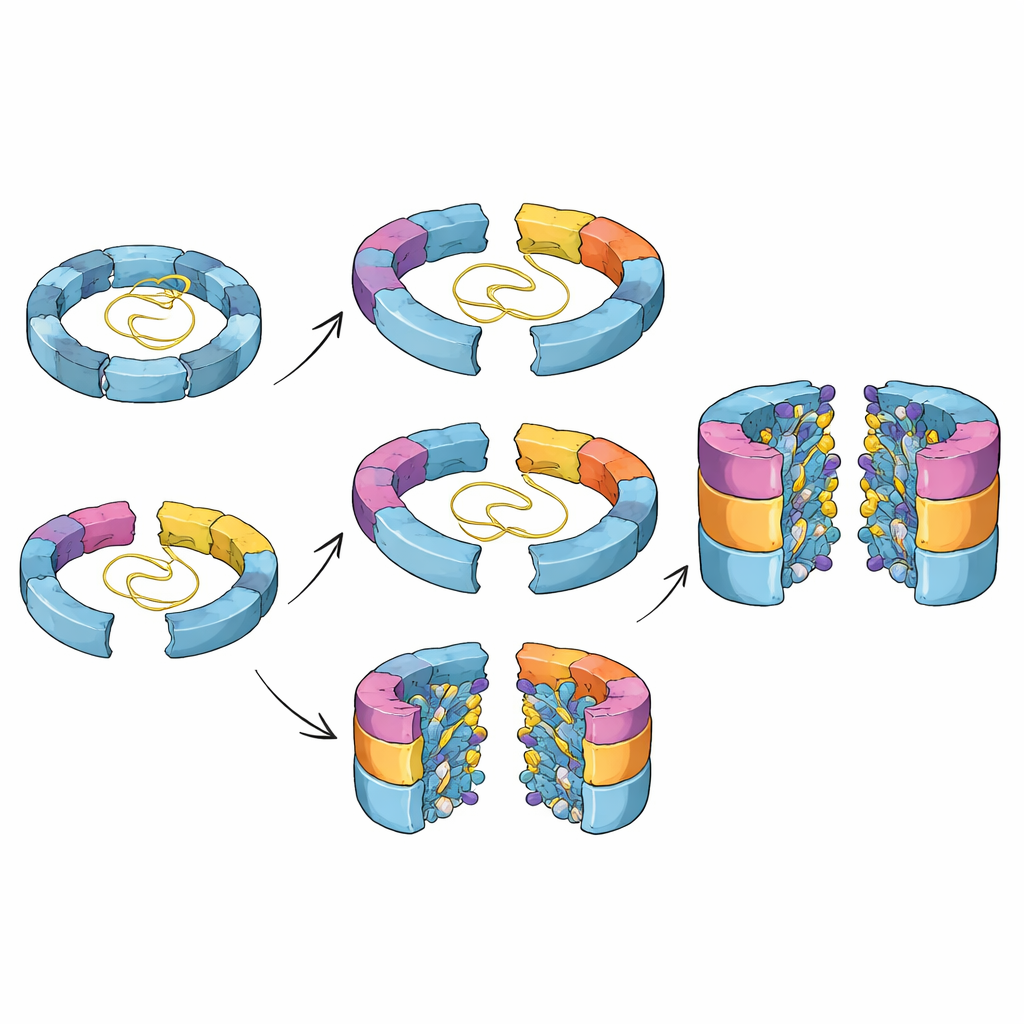
Les schémas classiques des manuels suggèrent souvent que les machines cellulaires complexes se construisent selon un itinéraire unique et fixe. Ici, les chercheurs montrent que ce n’est pas le cas pour le noyau du protéasome. Ils ont identifié plusieurs intermédiaires distincts qui diffèrent par les sous‑unités catalytiques ayant rejoint le cylindre à demi‑achevé. En combinant des instantanés structuraux et des manipulations génétiques qui activent ou désactivent des sous‑unités individuelles, ils montrent qu’au moins deux voies alternatives mènent d’un demi‑cylindre précoce à un quasi‑cylindre complet. Dans une voie, une sous‑unité particulière nommée β5 arrive en premier ; dans une autre, une sous‑unité différente, β1, peut se joindre plus tôt. L’équilibre entre ces parcours dépend probablement des blocs de construction les plus disponibles dans l’environnement cellulaire encombré.
Des pièces lâches à une chambre de découpe verrouillée
Les structures révèlent aussi comment les sites de découpe du protéasome sont soigneusement préparés au fur et à mesure de l’assemblage. Dans les intermédiaires précoces, des régions en boucle entourant les résidus de coupe enfouis sont souples et mal ordonnées, et les centres catalytiques sont encore bloqués par de courts segments « propeptide ». À mesure que des sous‑unités supplémentaires viennent se placer autour de l’anneau, ces boucles prennent progressivement des conformations plus définies qui alignent des acides aminés cruciaux nécessaires à l’auto‑activation. Ce n’est que lorsque deux demi‑cylindres se rejoignent enfin, complétant le cylindre double‑anneau, que ces boucles se verrouillent complètement en position active et déclenchent l’élimination des segments bloquants. Ce couplage entre géométrie et chimie veille à ce que l’activité de coupe puissante n’apparaisse qu’à l’intérieur d’une chambre scellée, protégeant le reste de la cellule.
Les chaperons guident puis lâchent prise
En cours de route, des protéines aides spécialisées appelées chaperons accompagnent le cylindre en formation et empêchent des combinaisons incorrectes. Un chaperon, Ump1, commence largement non structuré mais se replie progressivement à mesure que davantage de sous‑unités l’entourent, finissant piégé dans la cavité centrale puis détruit une fois que le cylindre est actif. Une autre paire de chaperons, Pba1–Pba2, saisit la surface de l’anneau externe de deux façons ingénieuses. Une boucle flexible de Pba1 s’insère entre deux sous‑unités de l’anneau externe comme un entretoise, les maintenant légèrement écartées et empêchant une fermeture prématurée. En même temps, l’extrémité terminale d’une sous‑unité de l’anneau externe (α1) aide à positionner les segments voisins de sorte qu’au stade final, les chaperons puissent être libérés et l’anneau se refermer correctement. Lorsque les chercheurs ont supprimé la queue de α1, le cylindre s’est bloqué dans un état tardif presque achevé qui retenait obstinément ses chaperons, confirmant que cette petite région agit comme une partie d’un mécanisme de libération.
Pourquoi ces étapes cachées sont importantes
Ensemble, ces résultats dressent un tableau détaillé de la manière dont les cellules orchestrent l’assemblage d’un destructeur de protéines dangereux mais essentiel. Le travail montre que le noyau du protéasome peut se construire par plus d’une voie, que ses sites actifs sont progressivement façonnés, et que les protéines aides non seulement stabilisent les intermédiaires précoces mais sont aussi intégrées à un circuit de temporisation qui assure leur départ au bon moment. Comprendre ces étapes cachées aide à expliquer comment de petits changements génétiques dans les facteurs d’assemblage peuvent contribuer à la maladie et peut faciliter la conception de médicaments qui moduleraient l’activité du protéasome dans le cancer, les troubles immunitaires ou la neurodégénérescence en ciblant sa construction plutôt que sa forme finale.
Citation: Mark, E., Ramos, P.C., Nunes, M.M. et al. Structural transitions in the stepwise assembly of proteasome core particles. Nat Commun 17, 2582 (2026). https://doi.org/10.1038/s41467-026-70525-w
Mots-clés: assemblage du protéasome, dégradation des protéines, chaperons moléculaires, cryo-microscopie électronique, contrôle qualité cellulaire