Clear Sky Science · fr
Chimérisme moléculaire transitoire pour exploiter des organites xénogènes
Panneaux solaires empruntés dans une seule cellule
Nous pensons généralement à la vie solaire en termes de plantes et d’algues, mais certains prédateurs unicellulaires prennent un raccourci : ils volent les « panneaux solaires » — les chloroplastes — de leurs proies. Cette étude examine comment un microbe de ce type, Rapaza viridis, maintient ces pièces volées en fonctionnement pendant des semaines, alors même qu’elles proviennent d’une espèce complètement différente. En révélant comment les propres protéines de l’hôte pénètrent et soutiennent ces chloroplastes étrangers, le travail éclaire la façon dont des composants cellulaires complexes comme les chloroplastes ont pu apparaître à l’origine.
Comment un microbe vole et utilise l’énergie verte
Rapaza viridis est un petit flagellé qui se nourrit d’une algue verte spécifique appelée Tetraselmis. Plutôt que de tout digérer, Rapaza conserve les chloroplastes capturés, désormais appelés « kleptoplastes », et rejette le reste de la cellule algale, y compris son noyau. Ces kleptoplastes sont découpés en morceaux et transmis aux cellules filles de Rapaza. Pendant environ deux semaines, l’hôte peut vivre presque entièrement de l’énergie et du carbone produits par ces chloroplastes empruntés, même s’ils ne reçoivent plus d’instructions ni de pièces de rechange du génome algal d’origine. Ce mode de vie inhabituel offre une fenêtre vivante sur les étapes précoces qui ont pu conduire à l’établissement permanent des chloroplastes.
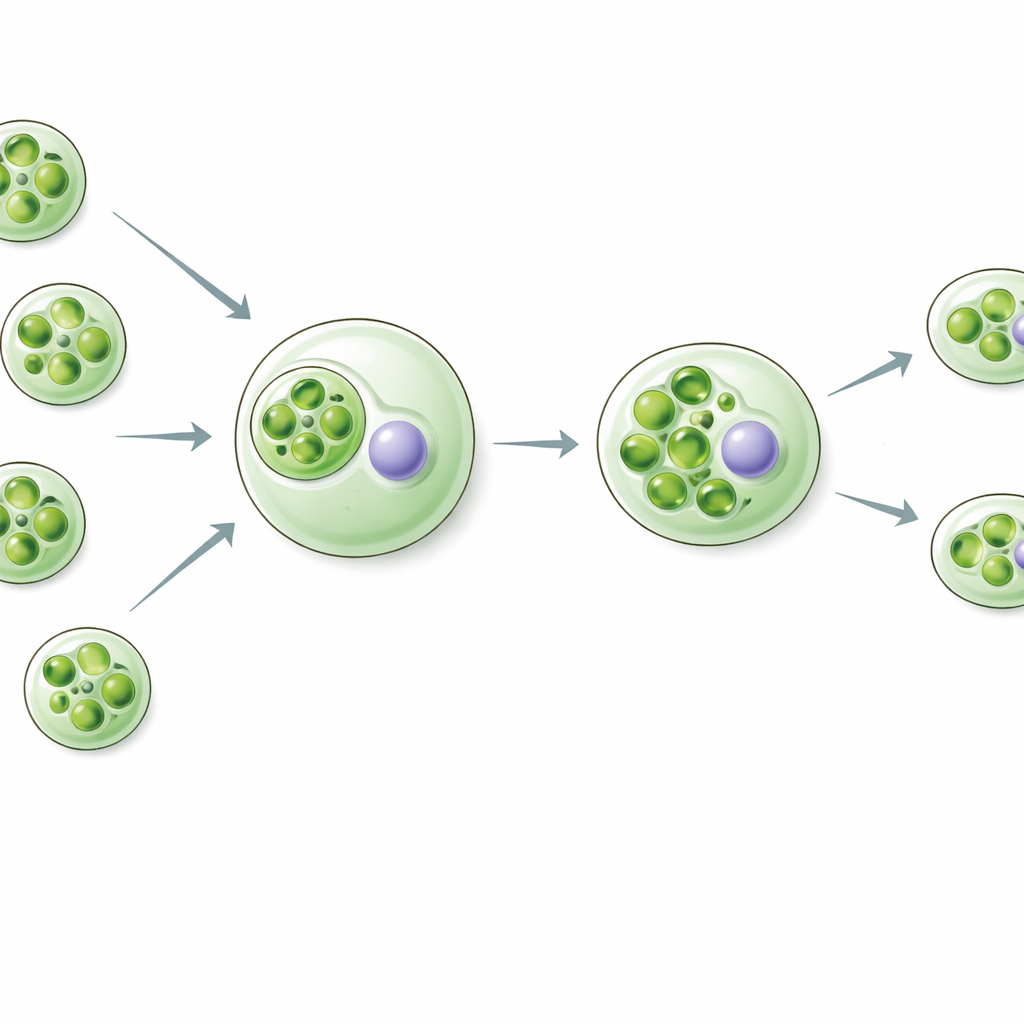
Les gènes de l’hôte entrent en jeu pour maintenir les éléments volés
Les chercheurs ont posé une question cruciale : si le noyau algal a disparu, qui fournit les protéines nécessaires pour conserver le kleptoplaste actif ? En analysant l’activité génétique dans le temps chez Rapaza, ils ont identifié 37 gènes de l’hôte dont les produits semblent fonctionner à l’intérieur des chloroplastes. Beaucoup de ces gènes ressemblent à des composants de la machinerie photosynthétique — protéines collectrices de lumière, éléments de transport d’électrons et enzymes qui fixent le carbone. Deux ont attiré l’attention : une protéine ressemblant à la petite sous-unité de RuBisCO (RvRbcS-like) et une protéine similaire à une activase de RuBisCO (RvRca-like). Les deux sont liées à des aides essentielles de la RuBisCO, l’enzyme centrale qui capture le dioxyde de carbone. Ces gènes de l’hôte s’expriment fortement après l’ingestion de la proie, précisément au moment où les kleptoplastes sont remodelés et préparés pour un usage à long terme.
Prouver que les protéines de l’hôte pénètrent dans les kleptoplastes
Trouver des séquences génétiques suggestives ne suffit pas : les protéines doivent réellement atteindre l’intérieur des kleptoplastes. À l’aide d’anticorps sur mesure et de microscopie à fluorescence, l’équipe a suivi où s’accumulent les protéines RvRbcS-like et RvRca-like. Ils ont conçu des souches de Rapaza avec de petites étiquettes détectables sur RvRbcS-like et montré que le signal chevauchait les kleptoplastes et la RuBisCO elle-même. Un marquage similaire avec un anticorps contre RvRca-like a révélé que cette protéine se concentre également à l’intérieur des kleptoplastes. Sur des gels protéiques, les deux protéines apparaissaient raccourcies, en accord avec l’élimination d’un segment frontal spécial lors de la traversée des membranes — exactement comme les signaux de ciblage qui guident les protéines vers des chloroplastes ordinaires.
Pourquoi ces aides empruntées comptent
Pour tester si ces protéines de l’hôte sont réellement importantes, les auteurs ont utilisé l’édition génomique basée sur CRISPR pour supprimer chaque gène. Les cellules dépourvues de RvRbcS-like ont montré une croissance médiocre, une capacité photosynthétique réduite, une production nettement moindre de grains de stockage riches en énergie et une mortalité beaucoup plus précoce que la normale. Les niveaux de la grande sous-unité de RuBisCO d’origine algale ont également diminué, suggérant que sans la sous-unité petite de remplacement fournie par l’hôte, le complexe enzymatique se désassemble. La suppression de RvRca-like a eu un effet plus modéré mais néanmoins net : la croissance précoce était proche de la normale, mais la photosynthèse et le stockage du carbone déclinaient plus tard, révélant une perte d’efficacité progressive. Ensemble, ces résultats montrent que Rapaza ne se contente pas de parquer des chloroplastes volés ; il les entretient et les remodèle activement avec son propre ensemble protéique.
Étiquettes de livraison sur mesure et structures internes reconstruites
La plupart des protéines putativement ciblées vers les kleptoplastes chez Rapaza présentent de longues « têtes » peu structurées à leur extrémité avant, souvent avec des segments prédits pour traverser une membrane. En fusionnant l’une de ces têtes à une protéine rapporteur luciférase, les auteurs ont montré que ce segment seul suffit à acheminer une protéine cargo dans les kleptoplastes. Une analyse de séquence détaillée a révélé plusieurs classes de ces régions de ciblage, qui ressemblent étroitement à celles utilisées par un groupe d’algues apparentées pour importer des protéines dans leurs chloroplastes permanents à triple membrane. Une protéine hôte particulièrement remarquable, RvRbcS-like, porte quatre domaines apparentés à RuBisCO et une queue souple riche en motifs répétitifs censés favoriser la séparation de phase des protéines. Les auteurs proposent que cette queue aide à réorganiser le pyrénoïde — le noyau dense de fixation du carbone à l’intérieur du kleptoplaste — en multiples gouttelettes qui peuvent être héritées par les cellules filles.
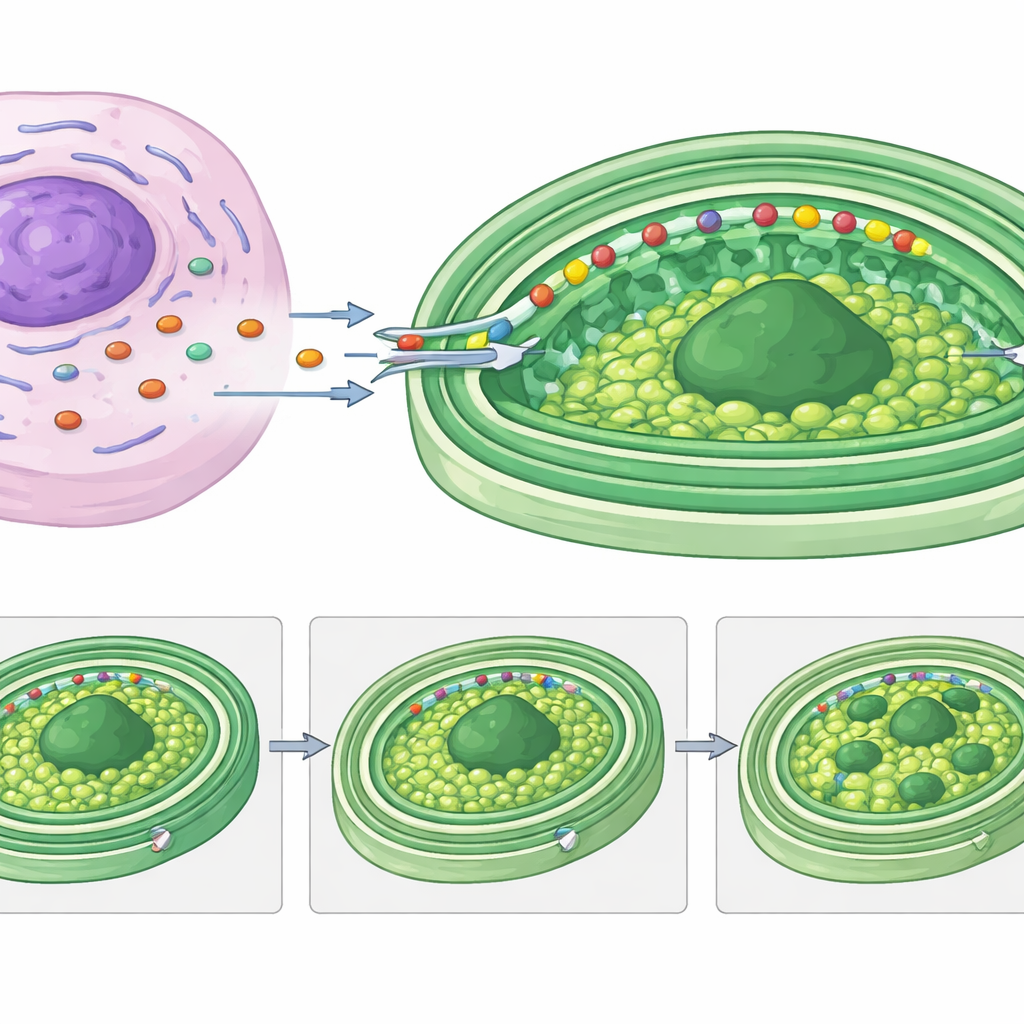
Ce que cela signifie pour l’histoire des cellules complexes
Pour le non-spécialiste, le message clé est que Rapaza viridis montre une version vivante et réversible de ce qui a pu se produire lorsque des cellules anciennes ont d’abord transformé des bactéries libres en éléments permanents comme les chloroplastes. Ici, l’hôte construit rapidement un partenariat moléculaire temporaire : ses propres gènes fournissent des pièces de rechange cruciales et réagencent même la structure interne des chloroplastes volés, le tout guidé par des étiquettes de livraison spécialisées. Ce « chimérisme moléculaire transitoire » démontre que même des intégrations de courte durée entre espèces peuvent être sophistiquées et finement réglées. L’étude de ce système donne aux scientifiques un modèle puissant pour comprendre comment les cellules complexes ont appris à contrôler, nourrir et utiliser en sécurité des usines d’énergie étrangères — et comment de nouveaux organites peuvent encore émerger au cours de l’évolution.
Citation: Kashiyama, Y., Maruyama, M., Nakazawa, M. et al. Transient molecular chimerism for exploiting xenogeneic organelles. Nat Commun 17, 2371 (2026). https://doi.org/10.1038/s41467-026-70516-x
Mots-clés: kleptoplastie, évolution des chloroplastes, Rapaza viridis, <keyword>biogenèse des organites