Clear Sky Science · fr
Caractérisation sans marqueur de la masse et de la taille de biomolécules de quelques kDa par microscopie de diffusion nanofluidique augmentée par transformeur de vision hiérarchique
Voir les plus petites molécules
Beaucoup des messagers les plus importants de l’organisme — comme les hormones et les signaux du système immunitaire — sont si petits qu’ils sont quasiment invisibles aux microscopes puissants à moins d’être marqués par des fluorophores. Ces marqueurs peuvent modifier le comportement des molécules, un inconvénient sérieux pour le développement de médicaments et la biologie fondamentale. Cette étude présente une méthode pour déterminer la masse et la taille d’individus moléculaires aussi petits que l’insuline sans aucun marqueur, en combinant des puces nanofluidiques et une intelligence artificielle avancée. Elle ouvre la voie à l’observation, une par une, de biomolécules clés dans leur état naturel.
Des canaux microscopiques comme éprouvettes
Au cœur de la méthode se trouve la microscopie de diffusion nanofluidique, qui utilise une puce de la taille d’un ongle gravée de canaux extrêmement étroits. Ces canaux ne font que quelques dizaines de nanomètres de largeur — des milliers de fois plus fins qu’un cheveu humain. Les molécules dissoutes dans un tampon dérivent librement à travers ces canaux au lieu d’être adsorbées sur une surface. Lorsqu’on éclaire la puce avec de la lumière visible, à la fois les parois du canal et toute molécule en transit diffusent la lumière. Comme le canal est beaucoup plus grand que la molécule, leurs diffusions interfèrent de manière à amplifier fortement la signature optique de la molécule. En soustrayant des images d’un canal vide des images prises lorsqu’une molécule est présente, les chercheurs obtiennent un enregistrement de type film (un kymographe) de son passage dans le canal, contenant des informations à la fois sur sa masse et sur sa diffusion.
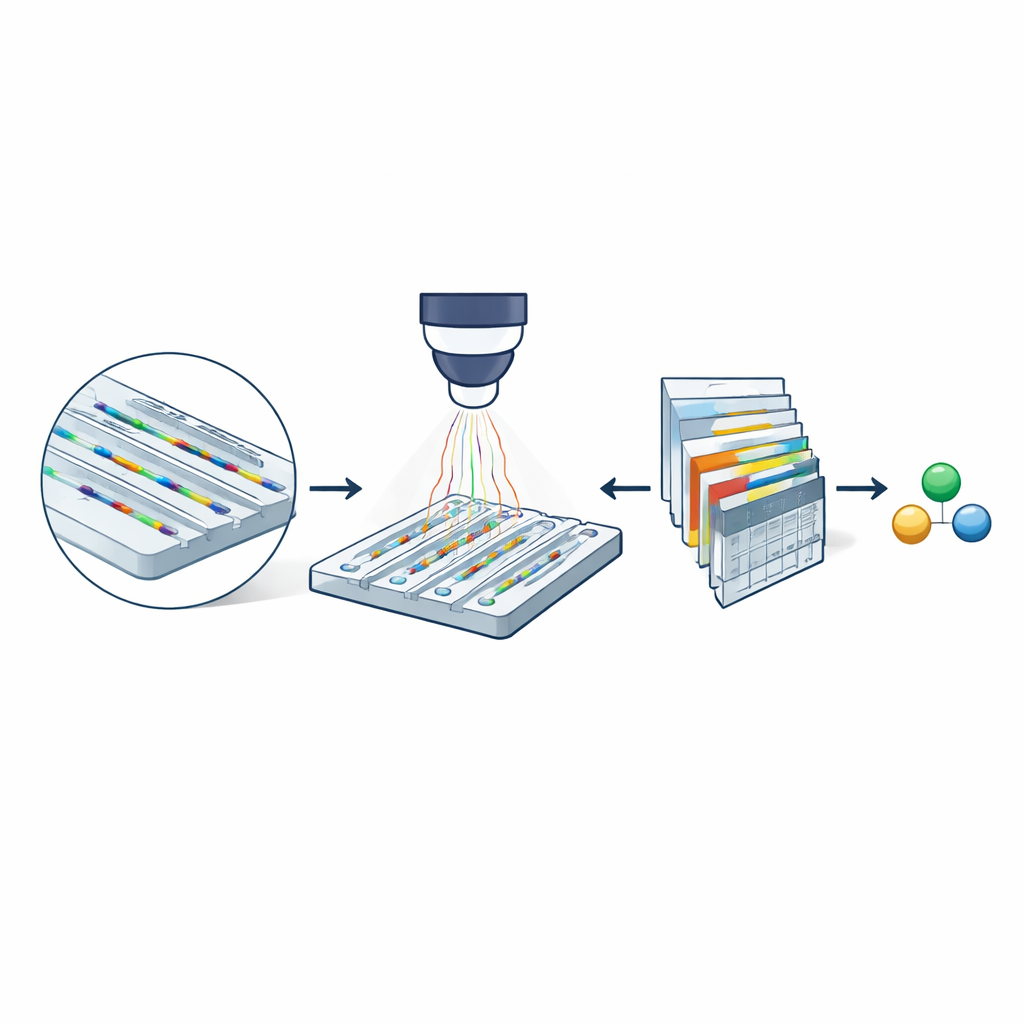
Pourquoi des canaux plus petits comptent
Même avec ce renforcement optique, les versions antérieures de la technique ne permettaient de caractériser que des molécules de plus d’environ 60 kilodaltons — des protéines de grande taille typiques — parce que les signaux des espèces plus petites se perdaient dans le bruit. L’équipe montre que réduire la section transversale des nanocanaux améliore drastiquement la sensibilité : le contraste optique d’une molécule augmente à mesure que l’aire du canal diminue. Des expériences comparant deux tailles de canaux avec la protéine albumine sérique bovine montrent que sa trajectoire est clairement visible dans le canal plus étroit mais presque effacée dans le canal plus large. Ce simple changement géométrique suggère qu’en principe des biomolécules beaucoup plus petites pourraient être détectables si leurs signaux faibles peuvent être extraits de manière fiable de séquences d’images bruitées.
Laisser une IA lire des films bruités
Pour atteindre ce régime, les chercheurs ont développé un modèle d’apprentissage profond spécialisé appelé transformeur de vision hiérarchique. Plutôt que d’essayer de reconstruire piste par piste chaque molécule pixel par pixel, le modèle parcourt le kymographe à plusieurs échelles et produit deux sorties : une carte de probabilité qui indique où une molécule est susceptible d’être à chaque position spatio-temporelle, et une carte de propriétés qui encode des estimations de masse moléculaire et de taille hydrodynamique. En pondérant les estimations de propriétés par la carte de probabilité, le modèle peut ignorer les régions principalement bruitées. L’entraînement s’appuie entièrement sur des trajectoires simulées superposées au bruit de fond mesuré expérimentalement, permettant au système d’apprendre à quoi ressemblent de vrais signaux même lorsqu’ils sont à peine visibles à l’œil.
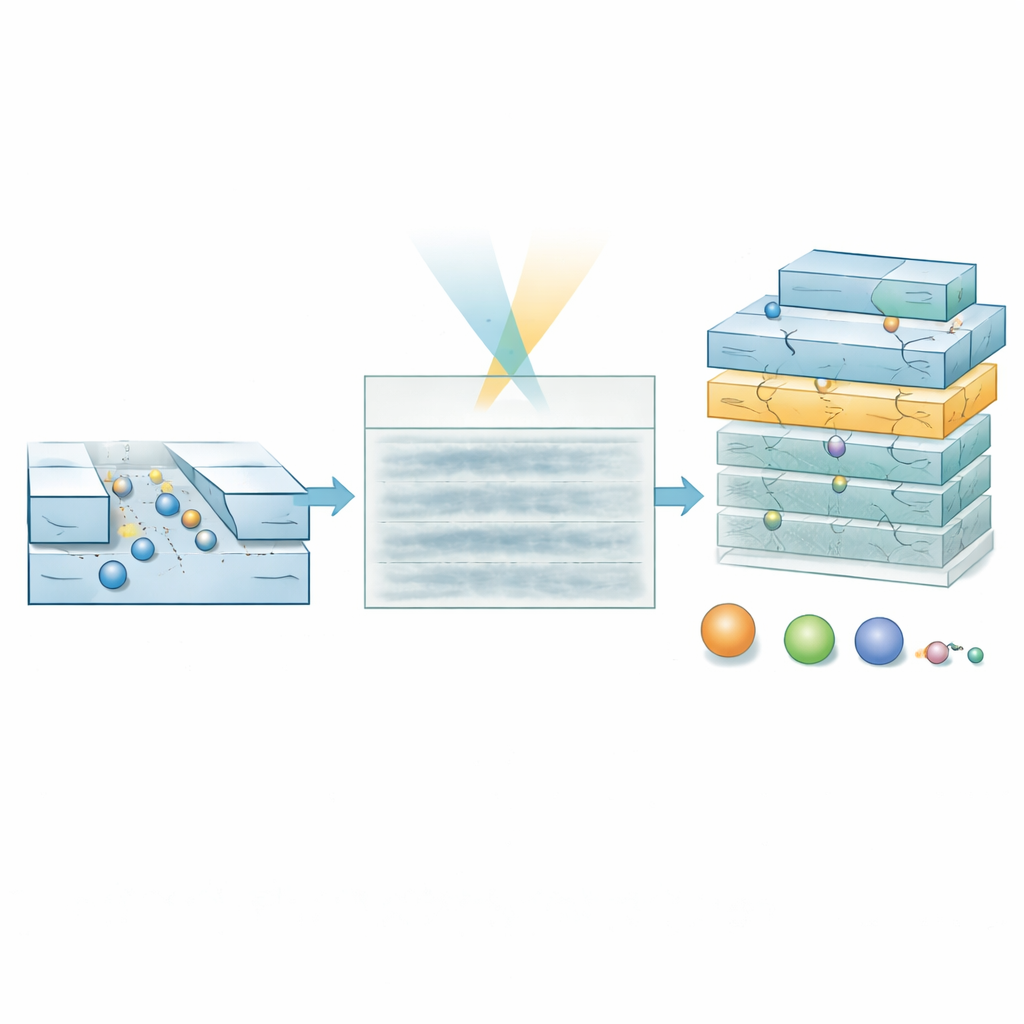
Test sur l’ADN et des hormones
Les auteurs ont d’abord validé l’approche en utilisant une « échelle » d’ADN standard, un mélange de fragments double-brin de longueurs et masses connues, dans des canaux relativement larges où tous les fragments sont délibérément en dessous de la limite de détection habituelle. Dans les films bruts, on ne distingue aucune trace d’ADN claire. Pourtant le modèle d’IA produit des cartes de probabilité qui mettent correctement en évidence les passages moléculaires et prédit des masses correspondant aux valeurs attendues une fois les données à faible confiance filtrées. La méthode rend aussi compte correctement de tailles effectives plus petites pour les fragments d’ADN rigides et en forme de tige que leur longueur physique totale, reflétant l’effet de leur conformation sur la diffusion. Le test le plus exigeant a utilisé des canaux ultras-étroits pour étudier l’hormone peptidique insuline, qui ne pèse qu’environ 5,8 kilodaltons et mesure environ 1,5 nanomètre de diamètre. Là encore, les kymographes semblent dénués de caractéristiques, mais le modèle extrait un groupe serré de valeurs de masse et de taille en excellent accord avec les données de la littérature, nettement séparé des contrôles constitués uniquement de tampon.
Repousser les limites
Pour comprendre jusqu’où cette stratégie peut aller, l’équipe a comparé la précision du modèle à la borne inférieure de Cramér–Rao, une limite statistique qui définit la meilleure précision possible pour tout estimateur non biaisé donné le niveau de bruit des données. En utilisant de grands ensembles de simulations, ils montrent que dès que le nombre d’images contribuant à la trajectoire d’une molécule dépasse environ dix mille, les estimations de masse et de taille du modèle se rapprochent de cet optimum théorique, même pour une particule de six kilodaltons. Des expériences sur l’insuline à différentes concentrations reproduisent la même tendance : des trajectoires effectives plus longues donnent des mesures plus précises, limitées principalement par le temps pendant lequel de très petites molécules à diffusion rapide restent dans le champ. Les auteurs proposent des stratégies futures — comme piéger doucement les molécules dans les canaux ou réutiliser les données via le bootstrap — pour augmenter encore le temps d’observation utile.
Ce que cela signifie pour la biologie et la médecine
Concrètement, ce travail montre qu’il est désormais possible de peser et de mesurer quelques-unes des plus petites et importantes molécules de l’organisme individuellement, sans les marquer par fluorescence ni les fixer sur une surface. En mariant des canaux nanofabriqués à une IA conçue pour lire des films bruités de diffusion de la lumière, la méthode abaisse d’environ un facteur dix la limite de détection en masse de cette approche de microscopie sans marqueur. Cela ouvre la porte à l’étude, au niveau monocellulaire, de familles de petites protéines de signalisation et d’hormones peptidiques — comme les cytokines, les chimiokines et l’insuline — et à la caractérisation de nanoparticules biologiques et de vecteurs médicamenteux avec une sensibilité sans précédent. À mesure que la technologie mûrit, elle pourrait devenir un outil puissant pour la découverte de médicaments, le diagnostic et les études fondamentales sur la manière dont les interactions moléculaires façonnent la vie aux plus petites échelles.
Citation: K. Moberg, H., Yeroshenko, B., Fritzsche, J. et al. Label-free mass and size characterization of few-kDa biomolecules by hierarchical vision transformer augmented nanofluidic scattering microscopy. Nat Commun 17, 2533 (2026). https://doi.org/10.1038/s41467-026-70514-z
Mots-clés: microscopie monocellulaire sans marqueur, diffusion nanofluidique, transformeur de vision, petites biomolécules, détection de l’insuline