Clear Sky Science · fr
Une mutation pathogène de Tau entraîne une dysfonction autophagie‑lysosome qui limite la dégradation de Tau dans un modèle de démence frontotemporale
Quand les équipes de nettoyage du cerveau sont dépassées
Pourquoi certaines personnes développent-elles des troubles sévères de la mémoire et du comportement des décennies avant la vieillesse ? Cette étude s’attaque à la question en se focalisant sur une seule protéine cérébrale, Tau, et sur les minuscules « centres de recyclage » cellulaires qui la contrôlent normalement. En observant des neurones humains vivants au microscope ultra‑précis, les chercheurs montrent comment une mutation pathogène de Tau encrasse le système d’élimination cellulaire et comment l’activation de ce système avec une petite molécule peut aider à dégager l’encombrement. Leurs résultats pourraient ouvrir des pistes pour de nouvelles stratégies thérapeutiques contre certaines formes de démence.
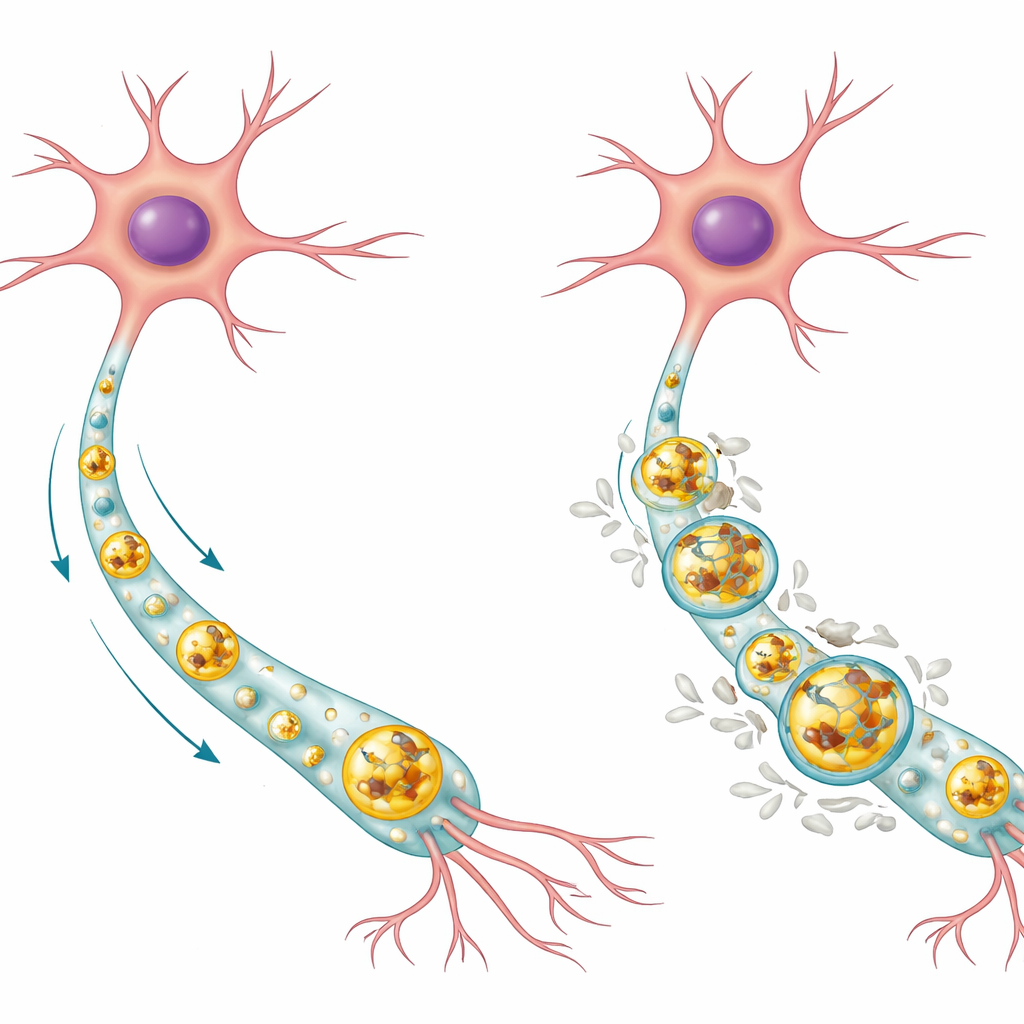
Comment les cellules cérébrales font habituellement le ménage
Les neurones sont des cellules longévives qui ne se divisent pas pour diluer les éléments endommagés ; ils dépendent donc fortement de systèmes internes de nettoyage. Une voie clé est la voie autophagie‑lysosome. Dans ce processus, les protéines indésirables et les éléments usés sont entourés de sacs membranaires appelés autophagosomes, qui fusionnent ensuite avec des compartiments remplis d’enzymes, les lysosomes, où le contenu est dégradé et recyclé. Chez des neurones humains sains, les auteurs ont constaté que la protéine Tau normale tend à s’accumuler à l’intérieur du centre acide des lysosomes, où elle peut être dégradée, tandis que la forme phosphorylée de Tau (modification chimique associée à la maladie) se situe davantage sur la membrane externe du lysosome. La plupart des lysosomes dans les cellules saines étaient totalement dépourvus de Tau, ce qui suggère que ce système maintient habituellement les niveaux de Tau bas et bien contrôlés.
Ce qui déraille dans une forme génétique de démence
L’équipe s’est concentrée sur une mutation du gène MAPT, nommée p.R406W, qui provoque une forme héréditaire de démence frontotemporale et peut mimer des pertes de mémoire de type Alzheimer. En utilisant la technologie des cellules souches, ils ont reprogrammés des cellules cutanées de patients en cellules souches pluripotentes induites, puis en un grand nombre de neurones humains porteuses soit de la mutation soit corrigées par édition génétique. Dans les neurones mutants, les taux de Tau total et de Tau phosphorylé étaient nettement plus élevés, non pas parce que les cellules produisaient plus de Tau, mais parce qu’elles l’éliminaient moins efficacement. L’imagerie super‑résolution a révélé que presque tous les lysosomes des cellules mutantes étaient remplis de Tau et que la forme phosphorylée recouvrait particulièrement la membrane lysosomale. Cette accumulation indiquait que la principale voie d’élimination des protéines des cellules était engorgée.
Centres de recyclage bouchés et trafic ralenti
En examinant de plus près la machinerie de recyclage, les chercheurs ont observé que les lysosomes des neurones mutants étaient plus nombreux, de plus grande taille et avaient tendance à se situer plus loin du corps cellulaire. L’imagerie en direct avec des colorants fluorescents montra que ces lysosomes se déplaçaient plus lentement et parcouraient des distances plus courtes le long des fibres nerveuses, bien que les rails sous‑jacents (les microtubules) semblaient normaux. Les neurones mutants contenaient aussi davantage d’autophagosomes, plus de la protéine adaptatrice de cargaison p62, et un surplus de gouttelettes lipidiques — signes que le matériel était étiqueté pour élimination mais pas complètement dégradé. À l’aide d’un rapporteur sensible au pH, ils ont constaté que les autophagosomes des cellules mutantes échouaient souvent à fusionner correctement avec les lysosomes, entraînant un entassement de vésicules de recyclage « à moitié finies » et des défauts généralisés du nettoyage cellulaire, pas seulement pour Tau mais aussi pour d’autres cargaisons.
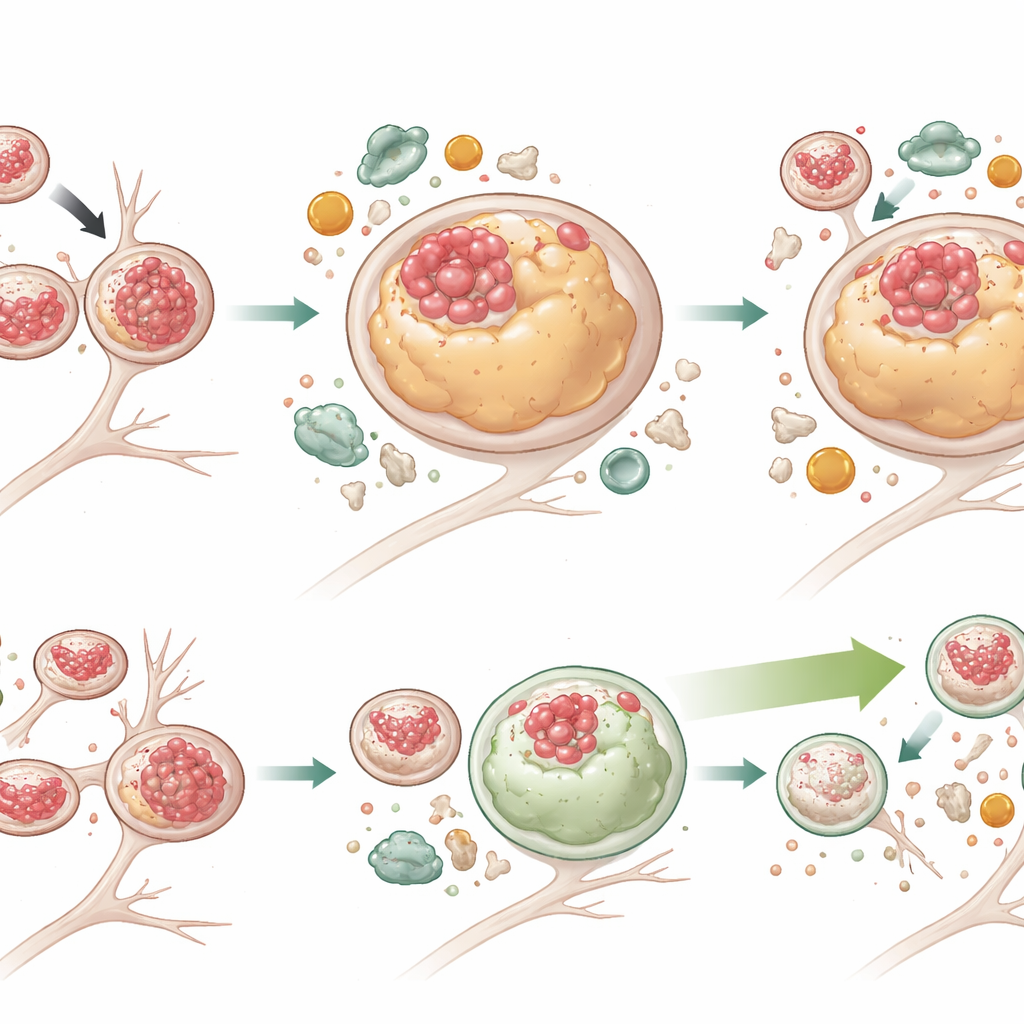
Renforcer le nettoyage cellulaire sans dénouer complètement l’embouteillage
Pour tester si l’amélioration de l’autophagie pouvait pallier ces problèmes, l’équipe a traité les neurones avec G2‑567, une petite molécule montrée antérieurement pour stimuler le système autophagie‑lysosome. Après deux semaines de traitement, les neurones mutants présentaient des niveaux substantiellement plus faibles de Tau total et de Tau phosphorylé, et beaucoup plus de lysosomes étaient à nouveau dépourvus de Tau. Les lysosomes ont aussi retrouvé une taille plus proche de la normale. Les marqueurs d’autophagie active ont augmenté, tandis que p62 — indicateur d’un blocage de la dégradation — a diminué dans les cellules mutants, démontrant une dégradation plus efficace des cargaisons. Fait notable, G2‑567 n’a pas corrigé tous les défauts : les lysosomes des neurones mutants restaient souvent plus éloignés du corps cellulaire et se déplaçaient lentement, et une protéine adaptatrice (JIP3) liée au transport lysosomal restait élevée. Cela suggère que les fonctions de mouvement et de dégradation des lysosomes peuvent être partiellement découplées, et que l’amélioration du seul processus de dégradation peut suffire à réduire l’accumulation toxique de Tau.
Ce que cela signifie pour les futurs traitements de la démence
Pour le non‑spécialiste, l’essentiel est que dans ce modèle génétique de démence frontotemporale, le problème n’est pas simplement que Tau devient anormal ; c’est que le système de recyclage du neurone ne suit plus. La mutation p.R406W de Tau perturbe directement plusieurs étapes de la voie autophagie‑lysosome, provoquant l’accumulation de Tau — en particulier de sa forme phosphorylée — sur et à l’intérieur des lysosomes, avec d’autres matériaux non dégradés. En stimulant pharmacologiquement la machinerie de nettoyage de la cellule, les chercheurs ont réussi à abaisser les niveaux de Tau et à normaliser la taille des lysosomes, même si les défauts de transport persistaient. Ces résultats renforcent l’idée que des médicaments conçus pour stimuler en toute sécurité l’autophagie et la fonction lysosomale pourraient aider à rétablir l’équilibre protéique dans les démences liées à Tau et peut‑être dans des affections plus courantes comme la maladie d’Alzheimer.
Citation: Mirfakhar, F.S., Marsh, J.A., Sato, C. et al. A pathogenic Tau mutation drives autophagy-lysosome dysfunction that limits Tau degradation in a model of frontotemporal dementia. Nat Commun 17, 2699 (2026). https://doi.org/10.1038/s41467-026-70473-5
Mots-clés: protéine tau, autophagie, dysfonctionnement lysosomal, démence frontotemporale, neurodégénérescence