Clear Sky Science · fr
L’hydrophobicité de surface et la rigidité déterminent la corona protéique des nanoparticules administrées par voie orale traitant la colite
Transformer les comprimés en traitements plus intelligents
Les personnes atteintes de maladies inflammatoires de l’intestin, comme la colite, prennent souvent des anti-inflammatoires puissants, mais une grande partie de la dose est perdue ou provoque des effets secondaires ailleurs dans le corps. Cette étude explore une nouvelle façon de rendre les médicaments oraux plus semblables à des missiles guidés : en concevant de minuscules particules porteuses de médicament qui recrutent les protéines intestinales du patient comme système de ciblage naturel, aidant ainsi les médicaments à atteindre les cellules immunitaires qui alimentent l’inflammation intestinale.
Comment l’intestin habille les nanoparticules
Lorsqu’une nanoparticule pénètre dans l’organisme, elle est rapidement recouverte d’une fine couche de protéines, formant ce que les scientifiques appellent une « corona protéique ». Dans l’intestin malade, cette corona diffère beaucoup de celle observée dans les tissus sains parce que la composition protéique locale est modifiée. Les auteurs ont montré précédemment que la colite engendre une corona intestinale particulière qui oriente modérément les particules vers des cellules immunitaires appelées macrophages, qui à la fois entretiennent et résolvent l’inflammation. Ici, ils cherchent à façonner délibérément cette corona en ajustant deux caractéristiques fondamentales des particules porteuses de médicament — leur caractère hydrophobe et leur rigidité — pour transformer un effet modeste induit par la maladie en une stratégie de ciblage puissante.
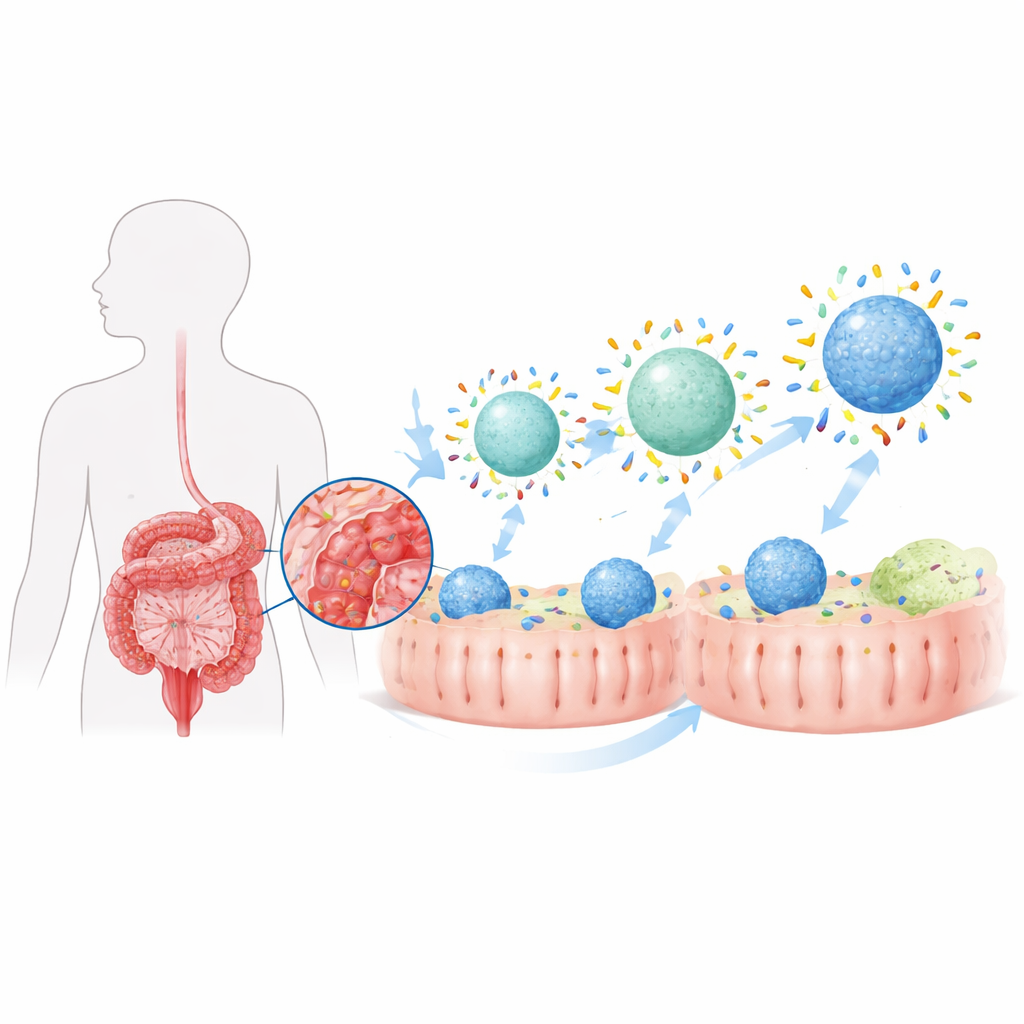
Rendre les particules plus attractives pour les protéines
L’équipe a fabriqué des nanoparticules à base de lipides semblables à de petites bulles de graisse et a modulé le caractère hydrophile ou hydrophobe de leurs surfaces en ajoutant différentes quantités d’un polymère de revêtement courant. Les particules aux surfaces plus hydrophobes lièrent beaucoup plus de protéines intestinales lorsqu’elles furent exposées aux liquides de colite, à la fois chez l’animal et en éprouvette. Lorsque ces particules « phobes » furent chargées du stéroïde budésonide et administrées par voie orale à des rats colitiques, elles délivrèrent beaucoup plus de médicament aux macrophages du côlon que des versions plus hydrophiles. En conséquence, les animaux traités retrouvèrent davantage de masse corporelle, présentèrent moins de raccourcissement du côlon et de dommages tissulaires, et eurent des niveaux plus faibles de molécules inflammatoires dans l’intestin. Cependant, bien que l’inflammation se soit améliorée, elle ne revint pas entièrement à l’état sain, ce qui suggère que l’augmentation seule de la quantité totale de protéines de la corona ne suffisait pas.
Durcir les particules pour choisir de meilleurs partenaires
Pour aller plus loin, les chercheurs maintinrent des surfaces hydrophobes mais modifièrent la structure interne pour rendre les particules molles, intermédiaires ou rigides en remplissant leurs cœurs de sphères plastiques de tailles différentes. Les trois types captèrent des quantités totales de protéines intestinales similaires, mais la composition des protéines changea. Les particules les plus rigides formèrent des coronas particulièrement riches en protéines capables de se lier à des récepteurs sur les macrophages ou de transporter de petits nutriments que ces cellules internalisent. Une de ces protéines, S100A8, est abondante dans les intestins enflammés et peut engager des récepteurs spécifiques des macrophages. Le blocage de S100A8 sur la corona réduisit fortement la captation des particules rigides par les macrophages, révélant ainsi qu’elle est un composant clé du ciblage sélectionné par la rigidité de la particule.
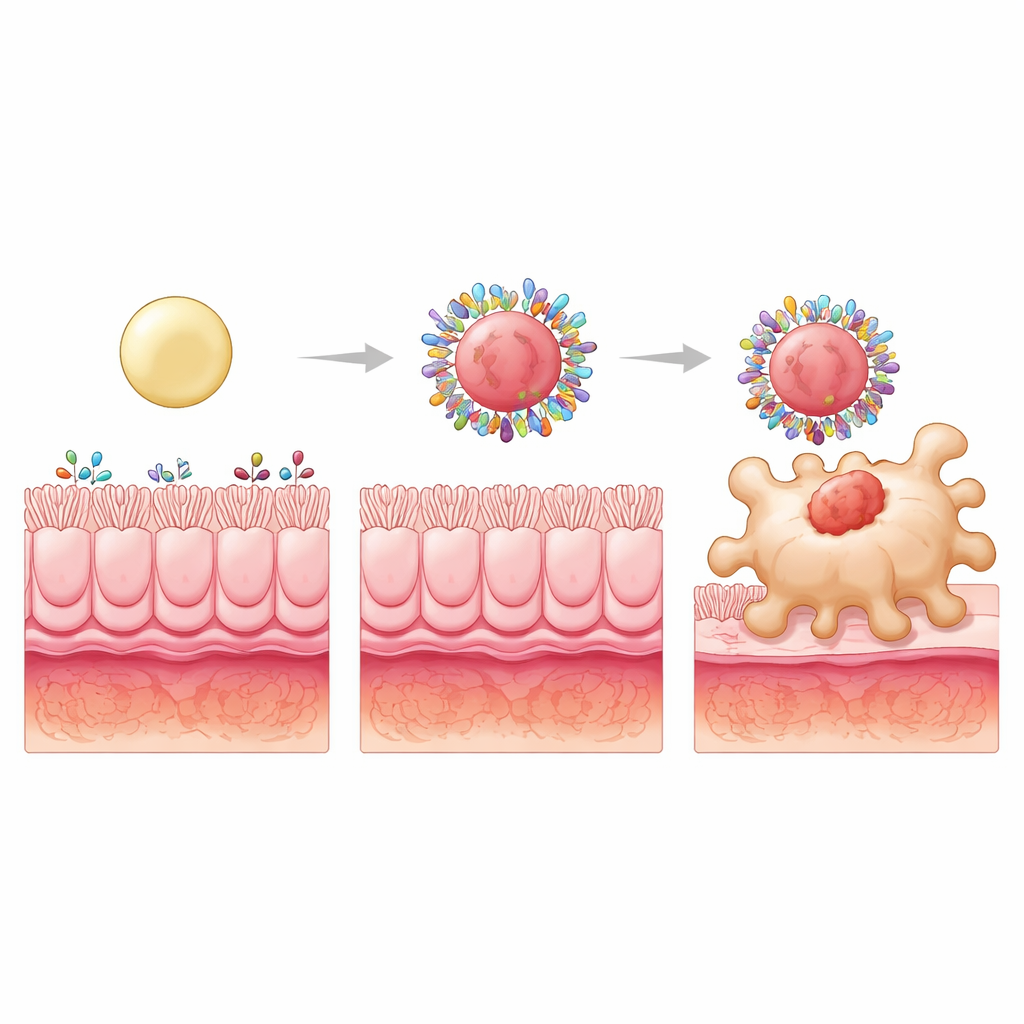
Du meilleur ciblage à une meilleure guérison
Lorsque la budésonide fut encapsulée dans ces particules à forte hydrophobicité et haute rigidité et administrée par voie orale à des rats atteints de colite, les bénéfices furent spectaculaires. La formulation rigide réduisit non seulement les lésions intestinales et le stress oxydatif, mais normalisa également plusieurs signaux inflammatoires à des niveaux observés chez des animaux sains. Elle rétablit un équilibre plus sain entre les types de macrophages « d’attaque » et « calmes » et renforça les cellules T régulatrices, qui contribuent à contenir les réponses immunitaires. Il est important de noter que ces effets dépendaient de l’environnement protéique altéré par la maladie dans la colite ; la même conception ne montra pas de ciblage particulier chez des rats sains, soulignant que la corona est un allié dynamique et spécifique à la maladie.
Pourquoi cela compte pour les médicaments du futur
Ce travail montre que l’on peut orienter les protéines endogènes du corps pour qu’elles agissent comme des « étiquettes » intelligentes et renouvelables sur des vecteurs de médicaments oraux simplement en ajustant les propriétés de surface et mécaniques des vecteurs. En augmentant d’abord la capture protéique grâce à des surfaces hydrophobes, puis en utilisant la rigidité pour favoriser les protéines homing vers les macrophages comme S100A8, les chercheurs ont créé des nanoparticules qui cherchent naturellement les cellules immunitaires responsables de la colite et délivrent la thérapie là où elle est le plus nécessaire. La même logique de conception — manipuler la perception et le comportement des particules à la surface intestinale — pourrait être adaptée à de nombreuses nanomédecines et pathologies, offrant une voie nouvelle et plus subtile vers le ciblage thérapeutique sans ajouter d’agents de ciblage artificiels.
Citation: Wu, J., Ni, M., Xing, L. et al. Surface hydrophobicity and rigidity determines protein corona on orally delivered nanoparticles treating colitis. Nat Commun 17, 2497 (2026). https://doi.org/10.1038/s41467-026-70453-9
Mots-clés: libération de médicaments par nanoparticules, maladie inflammatoire de l’intestin, corona protéique, nanomédecine orale, ciblage des macrophages