Clear Sky Science · fr
Informations operando sur des sites actifs Cu2+ stables pour une conversion électrochimique efficace du CO2 en C2H4
Transformer un problème climatique en matière première utile
Le dioxyde de carbone est le principal gaz à effet de serre responsable du changement climatique, mais c’est aussi une source de carbone bon marché et abondante. Chimistes et ingénieurs s’efforcent de trouver des moyens de convertir le CO2 en produits courants en utilisant de l’électricité propre plutôt que des combustibles fossiles. Cette étude présente un nouveau matériau à base de cuivre qui convertit le CO2 en éthylène — un ingrédient clé pour les plastiques et de nombreux produits chimiques — avec une grande efficacité et une stabilité à long terme, rapprochant l’idée de recycler le CO2 en biens de valeur d’une application pratique.
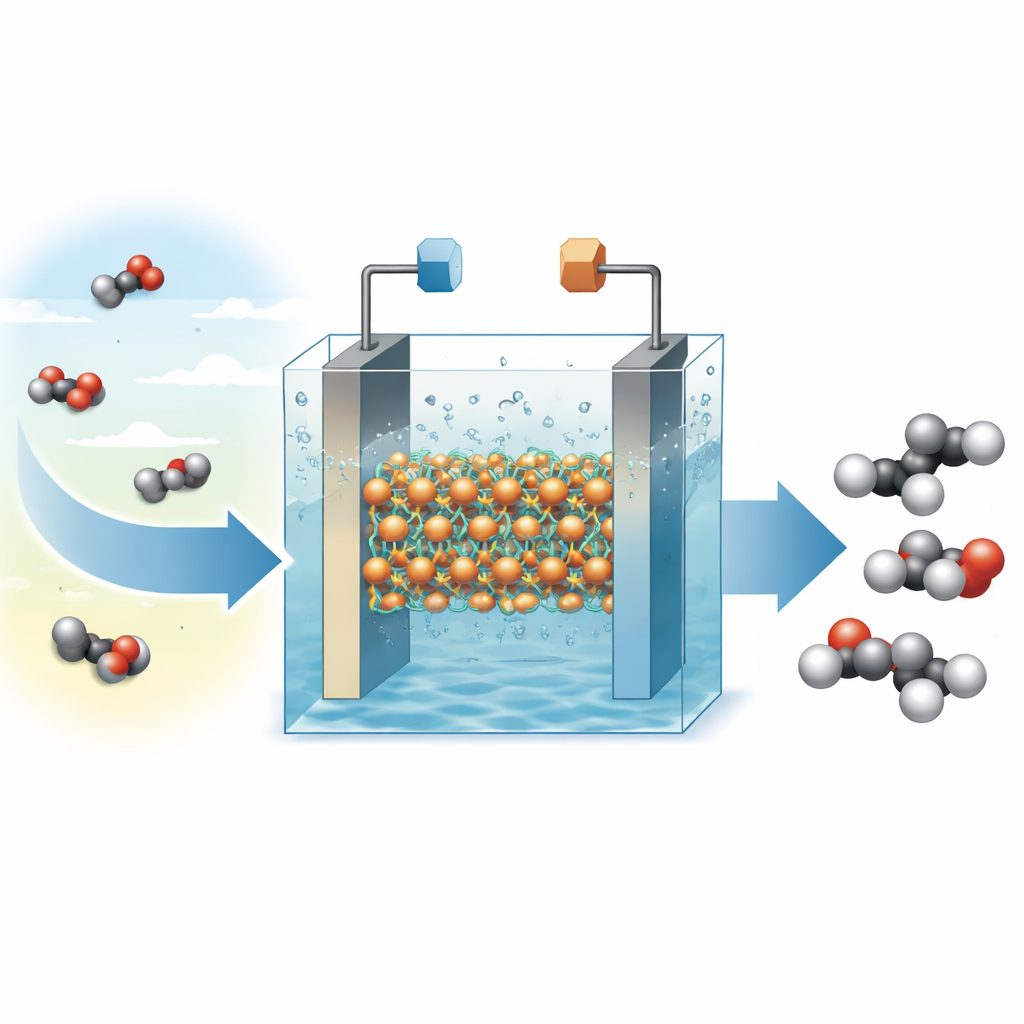
Pourquoi l’éthylène est important
L’éthylène est l’un des produits chimiques les plus produits au monde, utilisé pour fabriquer des plastiques, des solvants et une myriade de produits de consommation. Aujourd’hui, il est presque entièrement issu du pétrole et du gaz naturel, ce qui libère d’importantes quantités de CO2. Si l’on pouvait fabriquer l’éthylène directement à partir du CO2 en utilisant de l’électricité renouvelable, on pourrait à la fois réduire les émissions et créer une boucle carbone fermée. Le cuivre est l’un des rares éléments capables d’orienter le CO2 vers des molécules à plusieurs atomes de carbone comme l’éthylène, mais les surfaces de cuivre conventionnelles ont tendance à se remodeler et à changer d’état chimique en fonctionnement, ce qui réduit leur sélectivité et raccourcit leur durée de vie.
Concevoir un habitat calme pour le cuivre actif
Les auteurs abordent ce problème en construisant un polymère métal–organique — appelé CuBBTA — dans lequel les ions cuivre sont verrouillés dans un échafaudage répétitif formé avec une molécule organique nommée benzobistriazole. Dans cette structure, les atomes de cuivre restent dans un état de charge élevé (Cu2+) et se situent à des distances bien définies les uns des autres, reliés par des atomes d’azote et des groupes hydroxyles pontants. Des études structurales détaillées par diffraction des rayons X, microscopie électronique et spectroscopie avancée confirment que les atomes de cuivre sont isolés mais périodiquement arrangés, formant un réseau quasi bidimensionnel avec de nombreux sites de cuivre précisément espacés exposés au CO2 réagissant.
Performances solides dans un dispositif pratique
Testé dans une cellule liquide à flux et dans un électrolyseur à membrane — des configurations plus proches des dispositifs industriels — CuBBTA affiche des performances impressionnantes. En milieu alcalin, il convertit le CO2 en éthylène avec une efficacité faradique d’environ 62 %, ce qui signifie que près des deux tiers du courant électrique sont consacrés à la production d’éthylène plutôt qu’à des produits secondaires. Le matériau atteint également une forte efficacité de conversion énergétique pour la production d’éthylène et soutient des courants proches d’un ampère pendant plus de 50 heures tout en maintenant une sélectivité pour l’éthylène supérieure à 55–60 %. L’imagerie et la spectroscopie après réaction révèlent que la structure globale et la distribution des sites de cuivre restent essentiellement inchangées, contrairement à de nombreux catalyseurs à base de cuivre qui se dégradent ou s’agglomèrent en particules plus grosses.
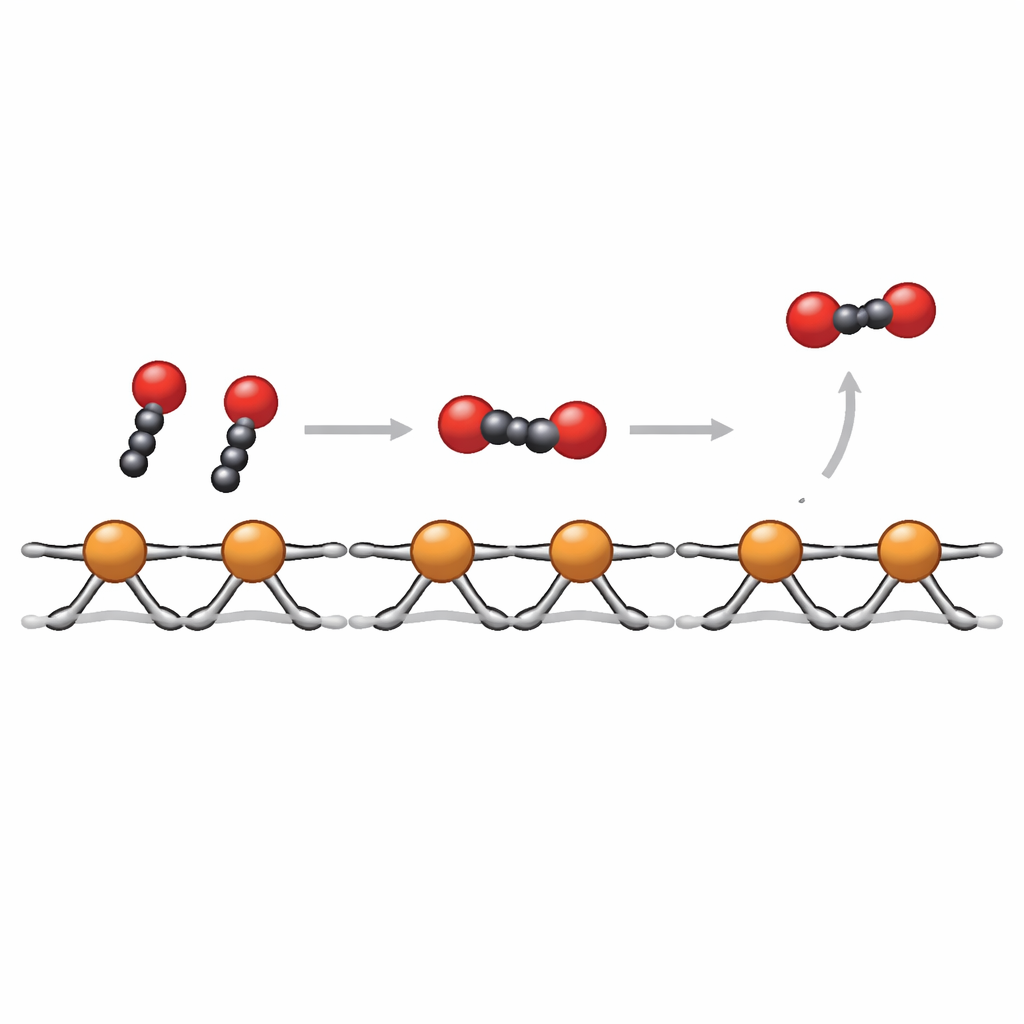
Observer les atomes à l’œuvre en temps réel
Pour comprendre pourquoi CuBBTA est si stable et sélectif, l’équipe a utilisé plusieurs techniques operando qui sondent le matériau pendant qu’il convertit réellement le CO2. Les mesures d’absorption des rayons X montrent que les ions cuivre restent à l’état Cu2+ sur une large plage de tensions appliquées, sans signe de formation d’amas de cuivre métallique. Les mesures Raman et infrarouges confirment que le réseau organique et les liaisons cuivre–ligand restent intacts. La spectroscopie infrarouge des molécules adsorbées en surface, combinée à la spectrométrie de masse en ligne, révèle que les sites de cuivre voisins dans le polymère favorisent la formation d’un intermédiaire apparié clé, souvent noté *COCHO, créé lorsque deux fragments plus petits dérivés du CO2 se couplent sur des sites adjacents. Les calculs quantiques mécaniques soutiennent ce tableau, indiquant que l’espacement fixe et la forte coordination autour du Cu2+ abaissent la barrière énergétique pour cette étape de formation de liaison C–C par rapport à une surface de cuivre métallique conventionnelle.
Comment cela fait avancer le recyclage du CO2
En termes simples, CuBBTA fonctionne comme une chaîne de montage bien organisée : les molécules de CO2 arrivent, sont partiellement réduites sur des postes en cuivre individuels, puis deux fragments se rencontrent sur des postes voisins pour former l’épine dorsale à deux carbones de l’éthylène. Parce que les ions cuivre sont maintenus fermement en place et protégés contre des conditions locales trop agressives, la chaîne continue de fonctionner sans que la machinerie ne se détériore. L’étude montre que des structures cuivre–organiques soigneusement conçues peuvent à la fois stabiliser la forme de cuivre la plus efficace et arranger les sites actifs à des distances optimales pour favoriser le couplage carbone–carbone. Cette stratégie ouvre une voie vers des dispositifs plus durables et efficaces qui transforment le CO2 de déchet en produits chimiques de valeur en utilisant de l’électricité renouvelable.
Citation: Zhang, Z., Xu, Q., Han, J. et al. Operando insights on stable Cu2+ active sites for efficient electrochemical CO2-to-C2H4 conversion. Nat Commun 17, 2654 (2026). https://doi.org/10.1038/s41467-026-70442-y
Mots-clés: réduction électrochimique du CO2, catalyseurs au cuivre, production d'éthylène, polymères métal–organiques, utilisation du carbone