Clear Sky Science · fr
Une atlas d’interactions à l’échelle du genre chez les orthologues de NS4B identifie un rôle conservé de l’UFMylation dans la réplication des orthoflavivirus
Pourquoi cette étude sur les virus est importante
Des virus comme le dengue, le Zika et le West Nile gagnent de nouvelles régions et peuvent provoquer tout, de la fièvre à des infections cérébrales et des malformations congénitales. Pourtant, nous manquons encore de traitements larges et fiables. Cette étude explore comment un partenariat méconnu entre ces virus et un système cellulaire d’étiquetage, l’UFMylation, aide les agents pathogènes à se multiplier. En cartographiant cette relation à travers de nombreux virus apparentés, les auteurs mettent au jour une faiblesse partagée qui pourrait être exploitée pour développer de futurs antiviraux.
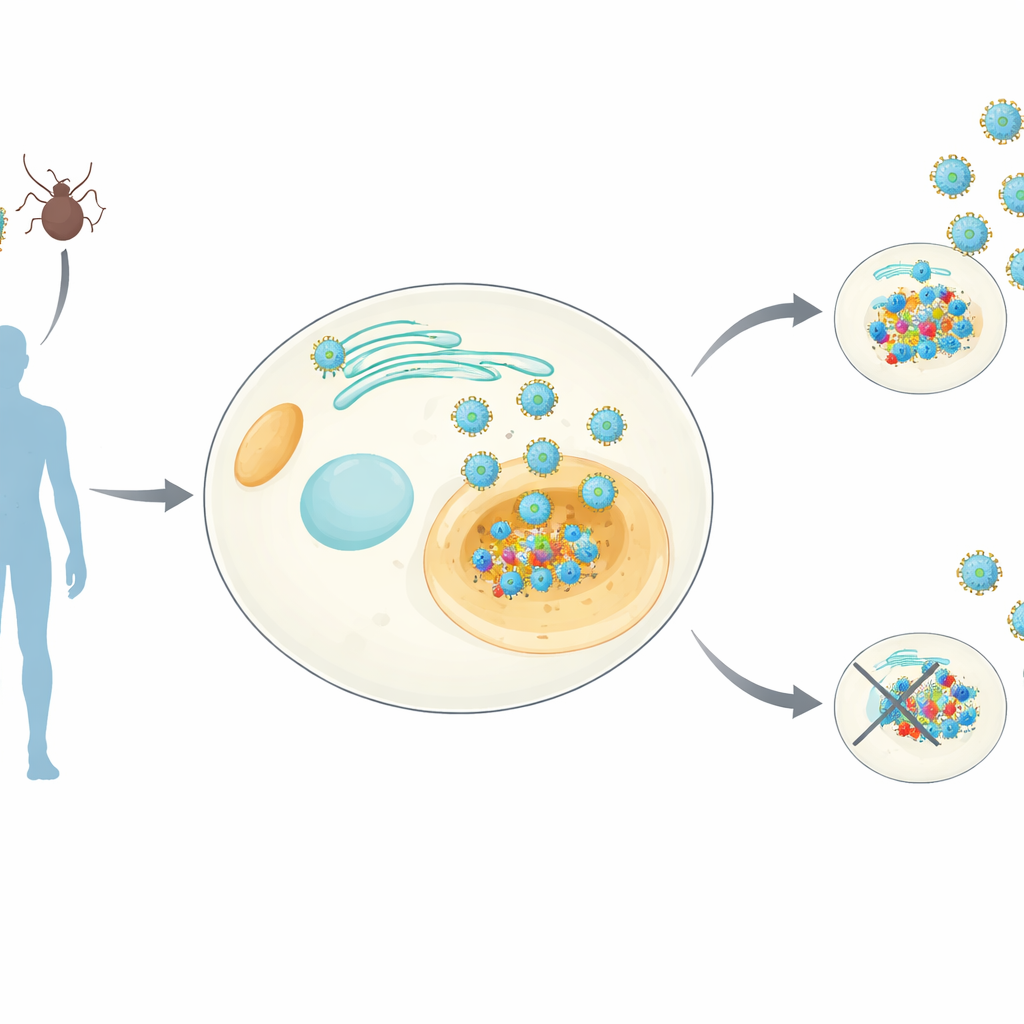
À la suite d’un acteur viral clé
Les orthoflavivirus – le groupe qui comprend le dengue, le Zika, la fièvre jaune et d’autres – portent tous une petite protéine appelée NS4B qui s’insère dans les membranes à l’intérieur de nos cellules. On sait que NS4B est essentielle pour la réplication virale, mais ses fonctions exactes demeuraient floues. Les chercheurs ont créé des lignées cellulaires humaines produisant de manière stable NS4B de huit orthoflavivirus différents. Ils ont ensuite utilisé des techniques sensibles de spectrométrie de masse pour extraire NS4B avec les protéines humaines qui s’y lient, et parallèlement mesuré comment l’expression de NS4B modifie l’ensemble des protéines de la cellule. Cela a produit un « atlas d’interactions » au niveau du genre – qu’ils appellent le NS4Bome – montrant à la fois des cibles hôtes communes et spécifiques à chaque virus.
Astuces partagées et adaptations particulières
L’atlas a révélé 538 protéines humaines qui interagissent avec NS4B et plus de 500 dont l’abondance change en présence de NS4B. Nombre d’entre elles sont concentrées dans des voies gérant la production d’énergie mitochondriale, le remodelage des membranes internes et le transport des protéines et lipides nouvellement synthétisés. Certaines interactions étaient partagées par la plupart des virus, suggérant des ruses conservées au cours de l’évolution que tous les orthoflavivirus utilisent. D’autres étaient présentes seulement chez certaines espèces ou souches, ce qui pourrait expliquer pourquoi certains virus préfèrent les moustiques aux tiques, ou provoquent des atteintes cérébrales plutôt que des fièvres hémorragiques. Cette vue systématique transforme un ensemble d’études antérieures fragmentaires en une carte cohérente de la façon dont ces virus réorganisent la cellule.
Un allié surprenant : le système d’UFMylation
Parmi les nombreux partenaires auxquels NS4B s’est lié, un a émergé : UBA5, l’enzyme initiale de la voie d’UFMylation. L’UFMylation est un système cellulaire qui attache une petite protéine marqueur, UFM1, à des cibles sélectionnées, influençant des processus comme le contrôle de la qualité des protéines et les réponses au stress. Grâce à l’interférence ARN et à des inactivations géniques par CRISPR, l’équipe a montré que des cellules dépourvues de UBA5 ou incapables d’effectuer l’UFMylation présentaient une réplication fortement réduite du Zika et de plusieurs virus apparentés. La réintroduction d’UBA5 normal a restauré la croissance virale, alors que des formes mutantes incapables d’assurer l’UFMylation ne l’ont pas fait, prouvant que l’activité d’étiquetage elle‑même est cruciale pour l’infection.
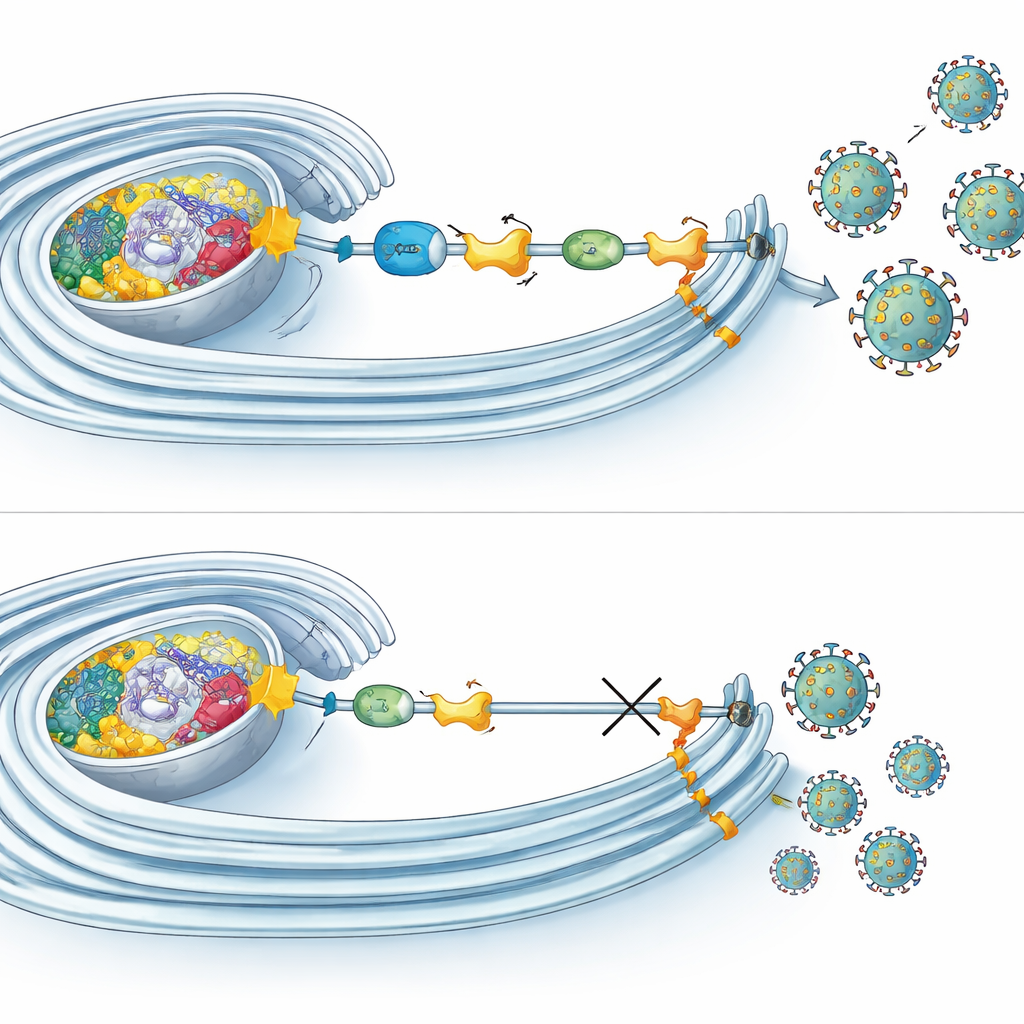
Comment l’étiquetage soutient les usines virales
Des expériences de microscopie et biochimiques ont révélé que plusieurs composants de l’UFMylation se rassemblent précisément là où l’ARN viral est copié à l’intérieur de membranes remodelées. Là, ils s’associent non seulement à NS4B mais aussi à d’autres protéines virales qui constituent la machinerie de réplication. Fait intéressant, bloquer l’UFMylation n’empêchait pas l’entrée virale, la synthèse d’ARN ou la traduction protéique. En revanche, cela handicapait surtout les étapes tardives du cycle, telles que l’assemblage ou la libération de particules infectieuses. Parallèlement, l’UFMylation influençait la respiration mitochondriale : lorsque la voie était désactivée, les cellules présentaient une consommation d’oxygène réduite et des mitochondries de morphologie altérée. À l’inverse, tôt lors de l’infection par le Zika, la respiration mitochondriale augmentait, suggérant que les virus pourraient exploiter l’UFMylation pour stimuler la production d’énergie cellulaire au moment où ils en ont le plus besoin.
Test d’un médicament dans des cellules et de petits poissons
Les auteurs se sont ensuite intéressés à un composé de faible masse moléculaire, DKM 2‑93, qui bloque le site actif de UBA5. Dans des cellules humaines en culture, cet inhibiteur a réduit la production du virus Zika d’environ dix fois à des doses laissant les cellules majoritairement saines, et a montré une activité dans plusieurs types cellulaires. Pour savoir si cette stratégie pouvait fonctionner dans un organisme vivant, ils ont utilisé un modèle de Zika chez le poisson zèbre, qui reproduit des caractéristiques clés de la maladie dans le cerveau en développement. Le traitement des embryons infectés par DKM 2‑93 durant le développement cérébral précoce a significativement diminué les niveaux d’ARN viral et réduit la proportion de poissons présentant des malformations sévères, indiquant un bénéfice antiviral réel in vivo.
Ce que cela signifie pour les traitements futurs
En construisant une carte complète des interactions de NS4B provenant de nombreux orthoflavivirus avec les protéines humaines, cette étude met en lumière l’UFMylation comme une voie d’aide conservée dont ces virus dépendent pour produire des particules infectieuses. Parce que ce même système hôte semble soutenir le dengue, le Zika, le West Nile et d’autres, des médicaments qui moduleraient sélectivement l’UFMylation pourraient agir comme antiviraux à large spectre, plutôt que de cibler un virus à la fois. Bien qu’il faille encore travailler pour identifier précisément quelles protéines sont étiquetées et garantir la sécurité, les résultats identifient une cible hôte prometteuse qui pourrait un jour aider à freiner les flambées de multiples maladies transmises par les moustiques et les tiques avec une approche thérapeutique unique.
Citation: Rajasekharan, S., Barragan Torres, V.A., Pinheiro Gomes, Y.C. et al. A genus-wide interaction atlas across NS4B orthologues identifies a conserved role for UFMylation in orthoflavivirus replication. Nat Commun 17, 2489 (2026). https://doi.org/10.1038/s41467-026-70437-9
Mots-clés: virus Zika, dengue, interactions hôte–virus, UFMylation, antiviraux à large spectre