Clear Sky Science · fr
Cages photochromiques assemblées dynamiquement opérant en eau avec de la lumière visible
Façonner de minuscules conteneurs réactifs à la lumière
Imaginez que des médicaments, des capteurs ou des catalyseurs puissent être activés et désactivés dans le corps simplement en exposant à une lumière colorée sûre. Cette étude décrit de minuscules molécules creuses — des « cages » — qui s’assemblent et se réarrangent lorsqu’on les éclaire, même en eau et en utilisant de la lumière rouge capable de traverser les tissus humains. Ces conteneurs intelligents se comportent un peu comme de simples machines : ils changent de forme, migrent entre des environnements lipophiles et aqueux, et interagissent avec des ions métalliques ou d’autres partenaires, le tout sous contrôle externe.
Pourquoi les cages contrôlées par la lumière sont importantes
Les cellules vivantes reposent sur d’innombrables structures moléculaires qui s’adaptent rapidement aux changements de conditions. Les chimistes cherchent depuis longtemps des nanostructures artificielles capables d’agir de façon analogue : répondre à des signaux comme le pH, la température ou des réactifs, et modifier ce qu’elles lient ou comment elles se comportent. La lumière est un signal particulièrement attractif car il peut être appliqué avec une grande précision spatiale et temporelle et ne laisse pas de résidus. Cependant, la plupart des cages moléculaires réactives à la lumière ne fonctionnent que dans des solvants organiques et nécessitent souvent une lumière ultraviolette agressive, peu adaptée à la biologie. Ce travail s’attaque aux deux problèmes en concevant des cages qui répondent à la lumière visible et rouge et peuvent opérer en eau, ouvrant la voie à des usages biomédicaux et technologiques futurs.
Construire des cages qui se reconfigurent sous la lumière
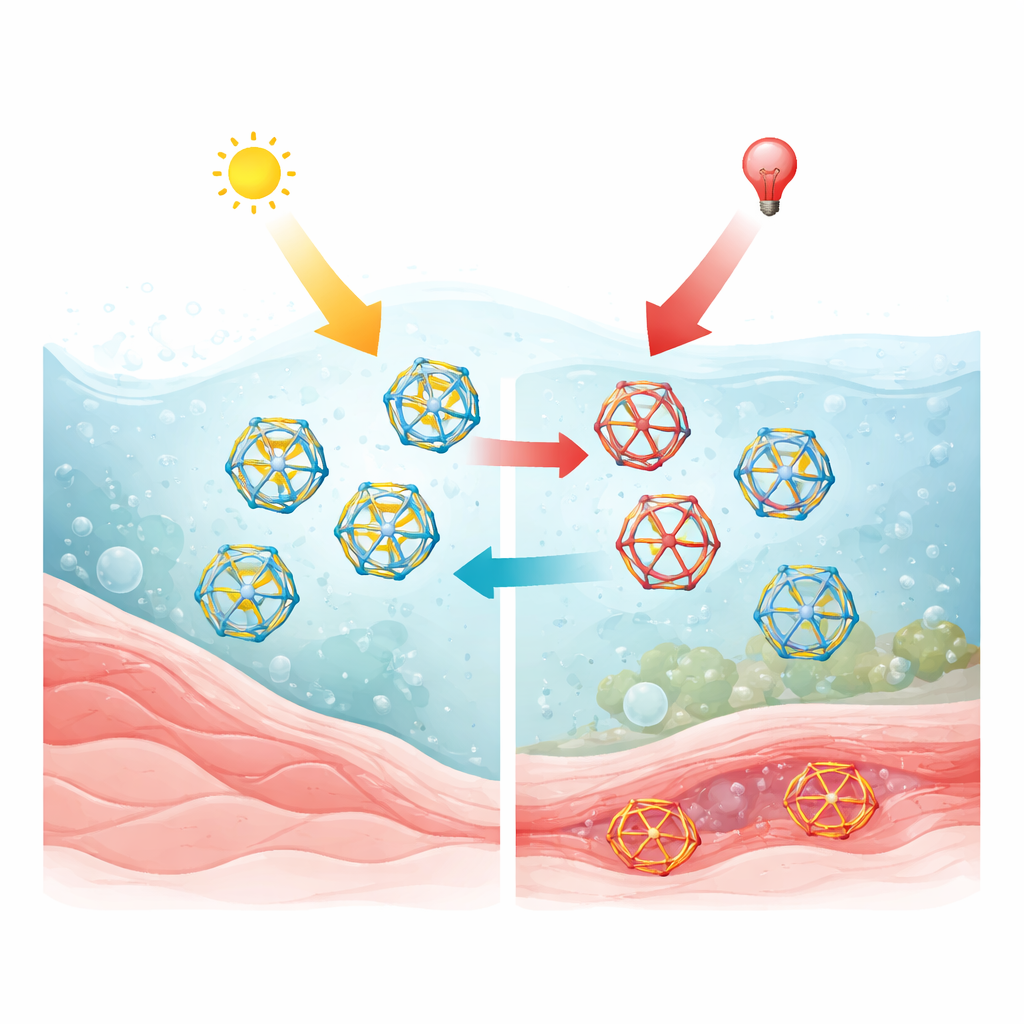
Les chercheurs partent d’un « photoswitch » spécial basé sur l’azobenzène, une molécule qui peut basculer entre deux formes selon la couleur de la lumière. Ils y ajoutent des groupes aldéhyde pour créer des éléments de construction pouvant se lier à une amine à trois bras par des liaisons chimiques réversibles, permettant aux pièces de s’auto-assembler en cages creuses bien définies. Dans leur premier système, trois piliers d’azobenzène fluorés et deux nœuds amine forment spontanément une cage dynamique en solution. La lumière rouge (environ 660 nm) replie les trois piliers en une forme coudée, mettant la cage sous légère contrainte, tandis que la lumière violette ou verte les ramène vers la forme originale, plus relâchée. Parce que le cadre de la cage maintient les interrupteurs dans un agencement particulier, il oriente l’efficacité et l’ampleur des changements induits par la lumière, produisant une photo‑réponse marquée et prévisible.
Verrouiller la forme et la faire fonctionner en eau
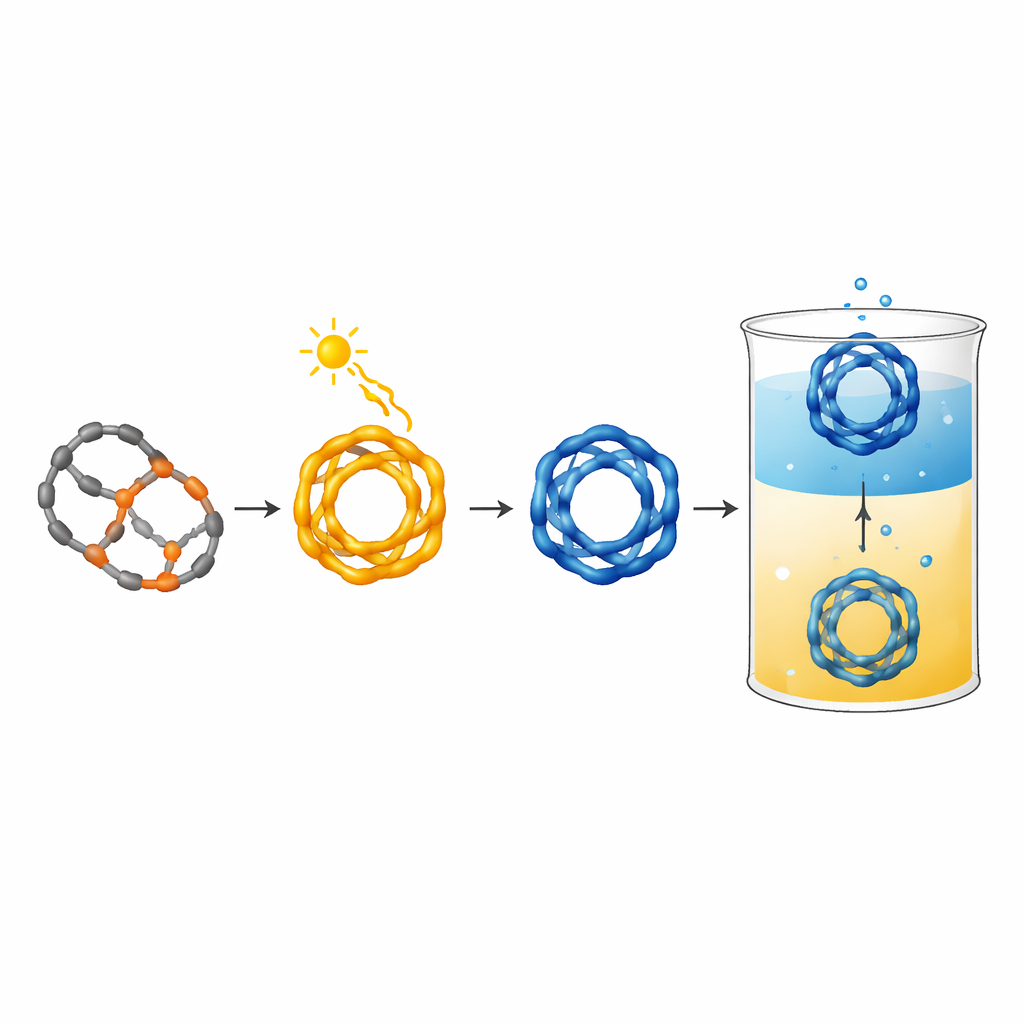
Pour passer d’un réseau fragile en perpétuelle réorganisation à un dispositif robuste, les auteurs « figent » chimiquement les liaisons dynamiques, les transformant en connexions permanentes et obtenant ainsi une cage covalente stable. Cette cage verrouillée peut toujours commuter entre des formes contrôlées par la lumière, mais sans se désassembler. Une astuce clé est la protonation : lorsque la cage est chargée positivement par un acide, elle devient soluble en eau et peut être transférée de manière réversible entre une phase organique et une phase aqueuse en faisant traverser du dioxyde de carbone puis en le laissant s’échapper. En eau, la cage reste photoswitchable avec de la lumière visible et peut même former des complexes d’inclusion avec des hôtes tels que les cucurbituriles, ce qui indique qu’elle peut transporter ou interagir avec des invités à l’intérieur de son intérieur creux. Des tests de toxicité en culture cellulaire humaine montrent qu’à faibles concentrations submicromolaires, la cage protonée est compatible avec les cellules, suggérant une utilisation possible en expériences biologiques à des doses soigneusement choisies.
Atteindre le proche infrarouge et dialoguer avec les métaux
Pour étendre le contrôle plus profondément dans la « fenêtre thérapeutique » utile en biologie, l’équipe conçoit un deuxième élément d’azobenzène portant des atomes de chlore. Cette variante peut être commutée dans les deux sens en n’utilisant que de la lumière rouge et proche infrarouge, sans recourir à des couleurs plus énergétiques. Elle forme également sa propre famille de cages, bien que les atomes de chlore plus volumineux rendent ces cages plus encombrées et susceptibles de s’ouvrir partiellement ou de se réarranger. En mélangeant des éléments fluorés et chlorés, les scientifiques créent des cages hybrides qui réarrangent leur composition en réponse à la lumière et à la chaleur. Ils montrent aussi que des cadres de cage similaires, construits à partir d’une unité bipyridine non basculante, agissent comme ligands multivalents pour des ions métalliques tels que le fer, formant des complexes colorés qui passent nettement en milieu aqueux. Lorsque ces unités de liaison aux métaux sont introduites dans une cage photoactive, les ions métalliques deviennent un moyen supplémentaire de diriger l’emplacement et le comportement des assemblages.
De petites cages à des machines d’allure vivante
Ensemble, ces expériences définissent des règles de conception pour construire des cages moléculaires qui s’assemblent seules, répondent de façon prévisible à la lumière visible et rouge, et fonctionnent en eau, y compris dans des milieux imitant des conditions biologiques. En combinant l’auto-assemblage réversible avec des étapes de « verrouillage » permanentes, et en intégrant plusieurs déclencheurs tels que la couleur de la lumière, l’acidité, le dioxyde de carbone et les ions métalliques, les auteurs se rapprochent de machines moléculaires capables d’une adaptation de type vivant. À long terme, de telles cages pourraient servir de transporteurs contrôlables pour des médicaments, de nanoréacteurs modulables pour des réactions chimiques ou de capteurs réactifs à l’intérieur de systèmes vivants, le tout piloté de l’extérieur par des couleurs de lumière choisies avec soin.
Citation: Schäfer, V., Seliwjorstow, A., Fuhr, O. et al. Dynamically assembled photochromic cages operational in water with visible light. Nat Commun 17, 2488 (2026). https://doi.org/10.1038/s41467-026-70406-2
Mots-clés: cages moléculaires photochromiques, nanotechnologie réactive à la lumière, commutation par lumière visible et rouge, auto-assemblage en eau, photoswitchs à l’azobenzène