Clear Sky Science · fr
Un modèle pentaculture 3D révèle une polarisation des macrophages pilotée par les cellules malignes dans le cancer ovarien séreux de haut grade
Pourquoi cette recherche est importante
Le cancer de l’ovaire est souvent détecté tardivement et peut résister tenacement aux traitements. Une des raisons tient au fait que les cellules tumorales vivent au sein d’un voisinage protecteur composé de cellules immunitaires et de tissu conjonctif qui les aident à échapper aux médicaments et aux défenses de l’organisme. Cette étude met au point un modèle de laboratoire sophistiqué — utilisant cinq types de cellules humaines en 3D — pour reproduire ce micro‑environnement et observer, en temps réel, comment les cellules cancéreuses poussent les cellules immunitaires voisines, appelées macrophages, à favoriser la tumeur plutôt qu’à la combattre.
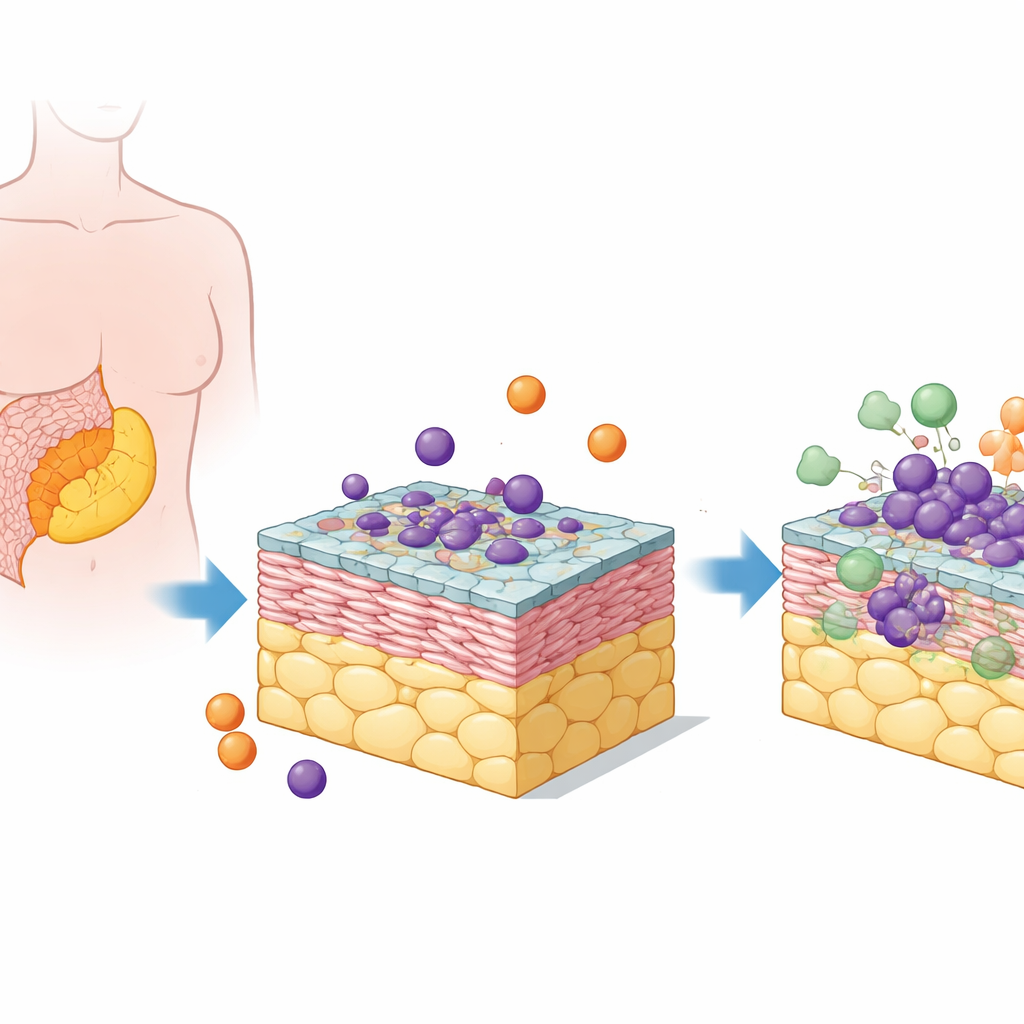
Construire un petit voisinage tumoral
Les chercheurs se sont concentrés sur le cancer ovarien séreux de haut grade, la forme la plus fréquente et la plus mortelle de la maladie. Ses métastases se développent souvent dans un tissu adipeux de l’abdomen appelé omentum. Pour recréer ce contexte, l’équipe a combiné des adipocytes humains, des cellules du tissu conjonctif (fibroblastes), un épithélium de cellules mésothéliales, des cellules de cancer ovarien et des cellules immunitaires circulantes appelées monocytes. Ces cinq types cellulaires ont été assemblés en « pentacultures » empilées en 3D qui ressemblent davantage à de véritables foyers tumoraux qu’à des couches cellulaires planes en culture.
Transformer des défenseurs immunitaires en spectateurs
Au sein de ce mini‑environnement tumoral, les monocytes ont naturellement mûri en macrophages — sans les signaux de croissance artificiels habituellement ajoutés en laboratoire. Grâce à des profils d’activité génique et à des comparaisons avec des données unicellulaires provenant d’échantillons tumoraux de patients, l’équipe a montré que les macrophages dans le modèle correspondent étroitement à ceux trouvés dans de vraies métastases ovariennes. Différentes lignées de cellules cancéreuses ont généré des mélanges distincts de types de macrophages et des architectures globales différentes des mini‑tumeurs, indiquant que les différences génétiques et moléculaires entre cellules cancéreuses façonnent fortement le paysage immunitaire environnant.
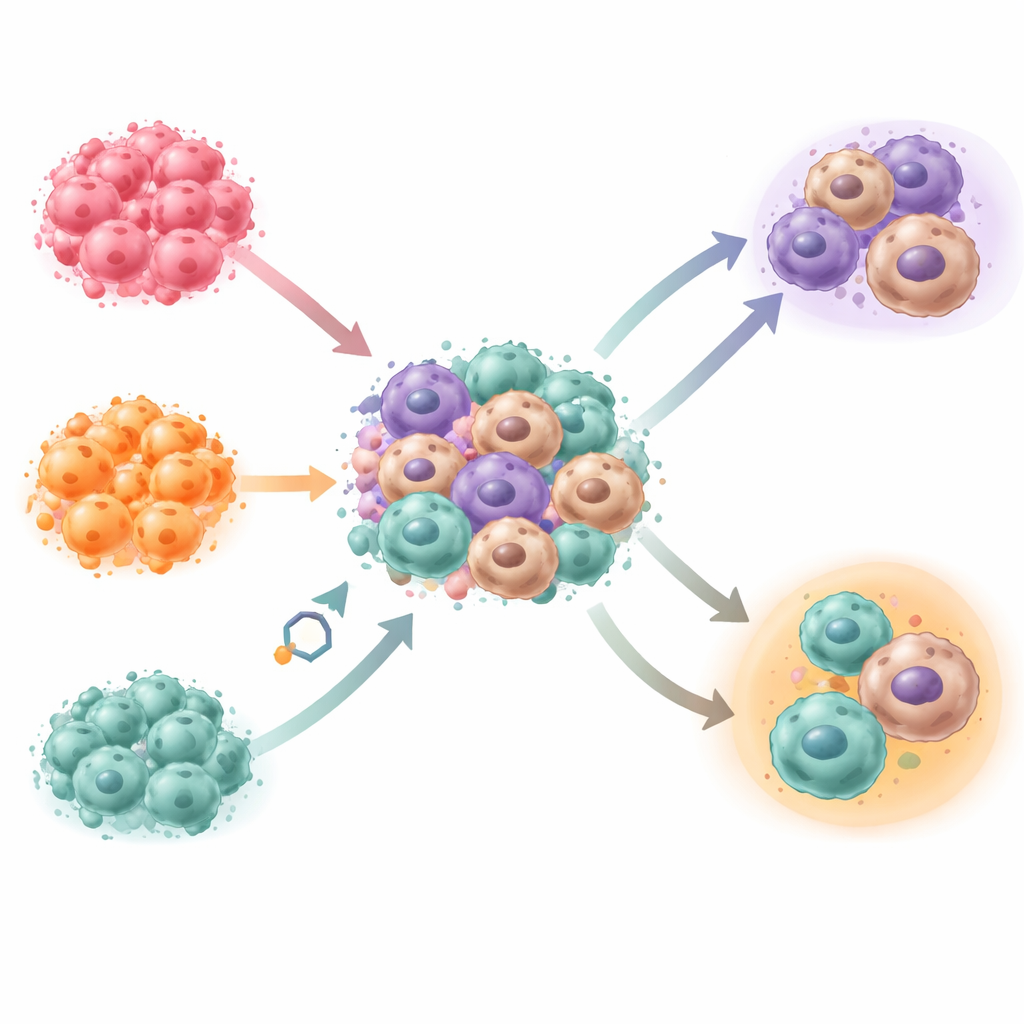
Comment les cellules cancéreuses échappent à l’ingestion
Les macrophages peuvent engloutir et détruire des cellules cancéreuses, mais les tumeurs émettent souvent des signaux de « ne pas manger » à leur surface. L’équipe a examiné deux de ces signaux, CD47 et CD24, sur trois lignées de cellules ovariennes cultivées dans le modèle 3D. Les cellules cancéreuses présentant des niveaux plus élevés de ces signaux avaient moins de chances d’être phagocytées par les macrophages. Dans les pentacultures, une lignée était facilement ingérée, une autre s’en échappait largement et une troisième affichait un comportement mixte. L’imagerie en direct a révélé que les macrophages se déplaçaient différemment et se positionnaient plus près ou plus loin des amas tumoraux selon la lignée cancéreuse, reflétant des schémas observés dans les tissus de patients.
Tester des moyens de réactiver l’attaque immunitaire
Parce que ces signaux de surface peuvent être bloqués par des anticorps thérapeutiques, les chercheurs ont traité les modèles avec des anticorps expérimentaux ciblant CD47 ou CD24. Dans des pentacultures construites avec une lignée cancéreuse particulière, le blocage de l’un ou l’autre signal a augmenté le contact entre macrophages et cellules cancéreuses, renforcé l’ingestion et réduit le nombre de cellules tumorales, tout en laissant les autres cellules du modèle largement indemnes. Dans une autre lignée très résistante, le blocage de ces signaux a eu peu d’effet, mais l’inhibition d’une voie de communication distincte (la voie TGFβ) a réduit les cellules cancéreuses d’une manière qui dépendait toujours de la présence des macrophages — suggérant des mécanismes alternatifs de destruction non basés sur l’ingestion, tels que la libération de cytokines toxiques.
Ce que cela signifie pour les patients
Pour un lecteur non spécialisé, le message clé est que tous les cancers de l’ovaire ne manipulent pas les cellules immunitaires de la même manière, même lorsqu’ils se ressemblent au microscope. En construisant un modèle 3D réaliste à cinq cellules à partir de tissus humains, ce travail montre comment les cellules tumorales peuvent programmer les macrophages pour qu’ils les ignorent ou qu’ils les attaquent, et comment le blocage de signaux spécifiques de « ne pas manger » peut parfois inverser cette situation. Le modèle reproduit fidèlement les tumeurs de patients, ce qui en fait une plate‑forme intermédiaire prometteuse pour déterminer quels médicaments ciblant l’immunité sont susceptibles de fonctionner selon les profils tumoraux. À long terme, de tels systèmes personnalisés en laboratoire pourraient aider à associer chaque patient aux thérapies qui réveilleront le mieux ses propres cellules immunitaires contre le cancer de l’ovaire.
Citation: Malacrida, B., Elorbany, S., Laforêts, F. et al. 3D pentaculture model unveils malignant cell-driven macrophage polarization in high-grade serous ovarian cancer. Nat Commun 17, 2451 (2026). https://doi.org/10.1038/s41467-026-70398-z
Mots-clés: cancer de l’ovaire, microenvironnement tumoral, macrophages, immunothérapie, culture cellulaire 3D