Clear Sky Science · fr
Les modifications ribosomiques sont associées à la sélection d’un destin mésenchymateux dans la lignée des crêtes neurales
Comment de minuscules usines cellulaires façonnent visages et tumeurs
Nos visages et certaines parties du système nerveux se construisent à partir d’un groupe itinérant de cellules embryonnaires appelées crête neurale. Ces cellules peuvent se différencier en os, cartilage, nerfs, et plus encore. Cette étude montre que leurs choix sont influencés non seulement par les gènes, mais aussi par des ajustements chimiques subtils apportés aux machines de production protéique de la cellule — les ribosomes. Les mêmes caractéristiques moléculaires qui contribuent à bâtir un visage normal peuvent, lorsqu’elles sont mal régulées, marquer des formes plus agressives de cancers infantiles.
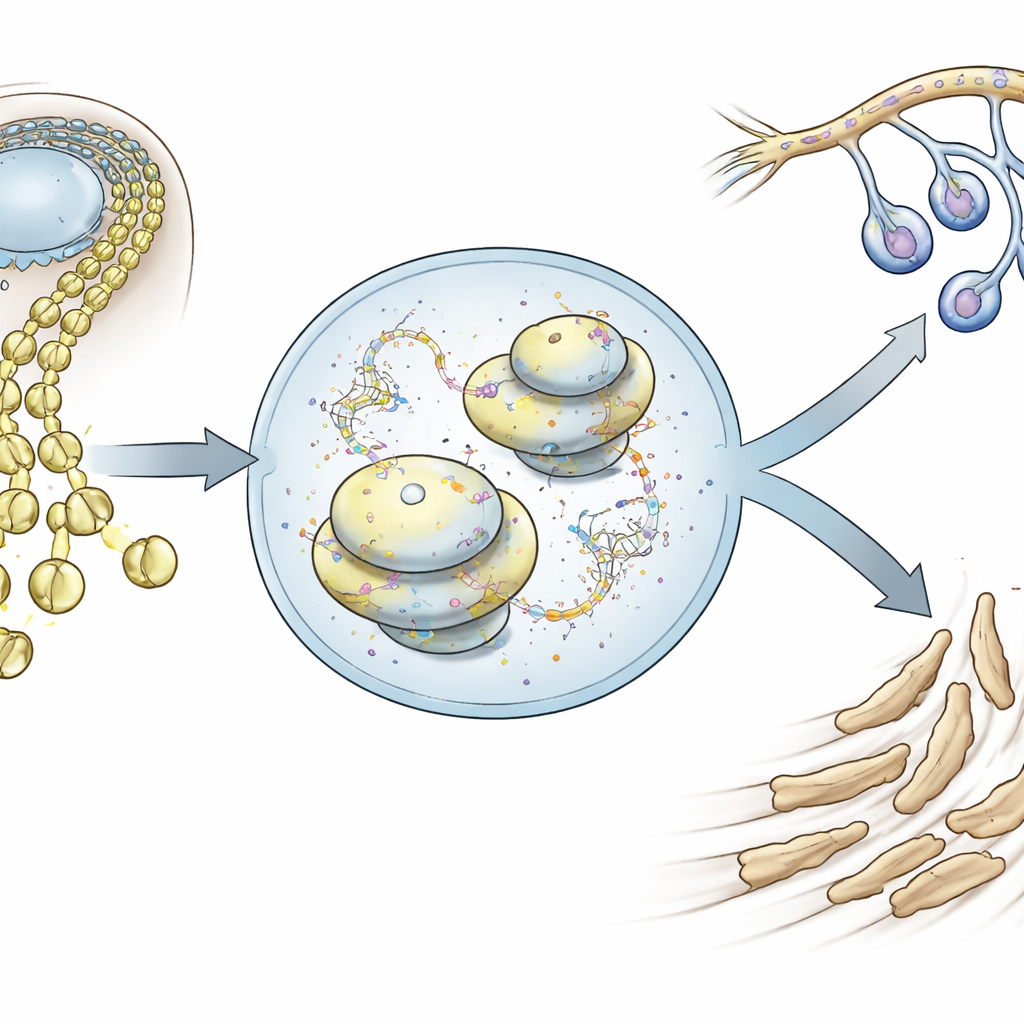
Cellules métamorphes qui construisent le visage
Les cellules de la crête neurale apparaissent le long du cerveau et de la moelle épinière en formation, puis migrent vers l’extérieur pour former une grande partie du crâne, des mâchoires et des nerfs périphériques. Grâce au séquençage ARN monocellulaire dans des embryons de souris, les auteurs ont suivi des milliers de cellules crâniennes de la crête neurale individuellement alors qu’elles quittaient le tube neural et se dirigeaient vers le visage. Ils ont constaté que, très tôt, ces cellules montrent déjà une légère inclinaison vers l’un de deux futurs principaux : une voie mésenchymateuse qui donnera les os et le cartilage faciaux, ou une voie neuro-gliale qui formera les neurones et les cellules gliales de soutien. Ces deux programmes d’activité génique coexistent initialement dans les mêmes cellules, mais deviennent mutuellement exclusifs au fur et à mesure du développement, imposant une décision de destin.
Les usines à protéines comme arbitres de destin
Lorsque l’équipe a examiné les gènes associés à l’inclinaison précoce vers le mésenchyme facial, elle a mis au jour deux groupes principaux. L’un comprenait des acteurs familiers qui poussent les cellules à se relâcher, migrer et changer d’identité, un processus connu sous le nom de transition épithélio-mésenchymateuse. L’autre groupe, plus surprenant, se concentra sur l’assemblage des ribosomes et la modification chimique de l’ARN ribosomique, le cœur de la machinerie de synthèse protéique. Plutôt que de simplement produire plus de ribosomes, les cellules de la crête neurale crânienne activaient des facteurs qui ajustent finement la manière dont les ribosomes sont construits et marqués chimiquement. Perturber la production d’ARN ribosomique chez l’embryon de souris au moment du choix de destin épargna en grande partie le développement des nerfs mais entraîna un fort retard des structures squelettiques faciales, montrant que la voie mésenchymateuse dépend particulièrement de ce contrôle ribosomique.
Une marque spécifique sur l’ARN ribosomique
En approfondissant, les chercheurs se sont concentrés sur un seul nucléotide au sein de l’ARN ribosomique 18S, à un emplacement crucial pour la synthèse protéique précise. Dans les cellules de la crête neurale crânienne inclinées vers des destins mésenchymateux, le séquençage interprétait de façon répétée mal cette position, un signe distinctif d’une modification chimique intense plutôt que d’une véritable mutation. Des travaux antérieurs avaient montré qu’un trio d’enzymes ajoute une modification complexe à cet endroit via plusieurs étapes. En combinant des données génomiques et d’ARN humaines avec la spectrométrie de masse sur des tissus embryonnaires de souris, l’étude a confirmé que ce site est normal dans l’ADN mais chimiquement altéré à des degrés divers dans l’ARN, et que la proportion de cette forme modifiée diffère entre le cerveau et les tissus faciaux. La surexpression ou l’invalidation des enzymes responsables de cette modification, en cultures cellulaires et chez l’embryon de souris, perturba le développement de la crête neurale et produisit des défauts craniofaciaux marqués, soulignant que des niveaux précis de cette marque d’ARN aident à orienter les cellules vers la voie skeletogénique.
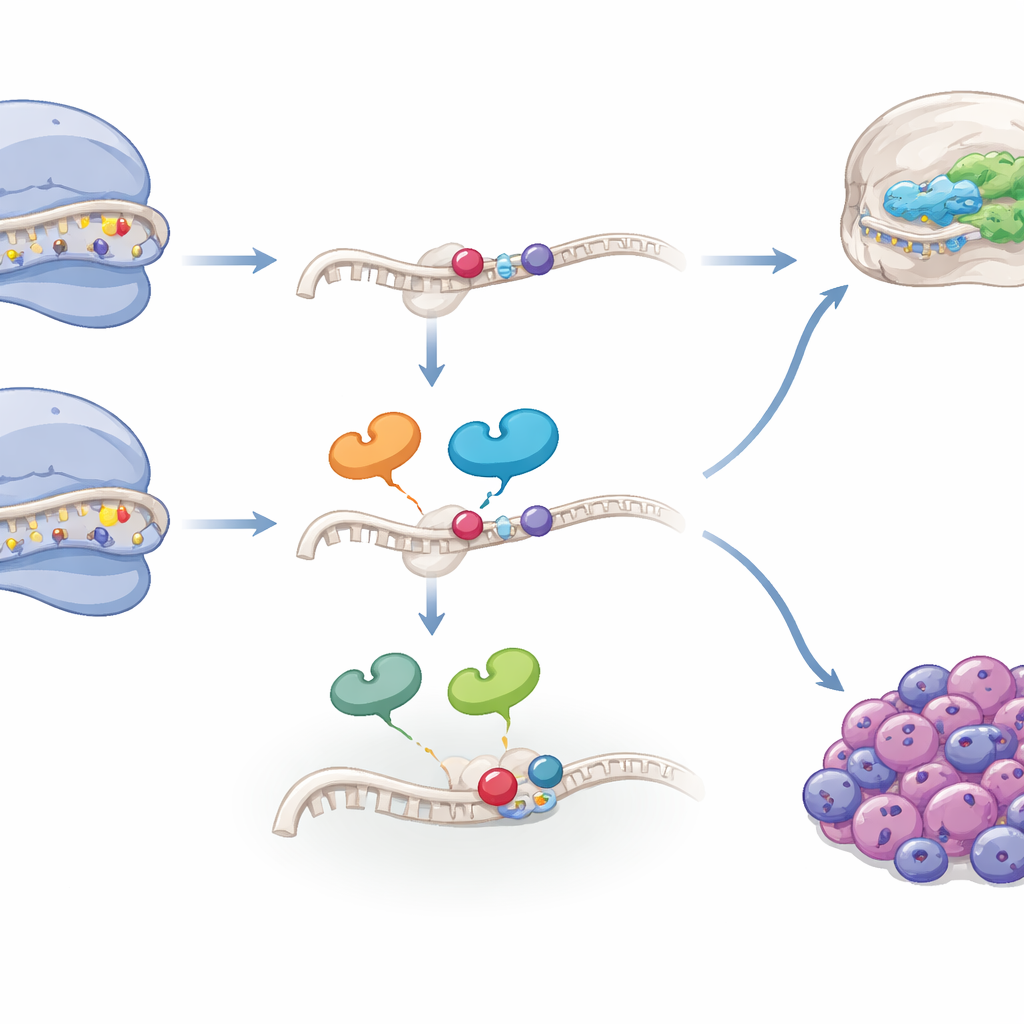
Du développement au risque de cancer
Parce que les cellules de la crête neurale peuvent aussi donner naissance à des tumeurs telles que le neuroblastome, les auteurs ont cherché si les mêmes caractéristiques ribosomiques apparaissent en cancérologie. En analysant des données ARN monocellulaires et en masse de plusieurs cohortes de neuroblastomes et de tumeurs cérébrales, ils ont observé qu’un signature génique liée au « contrôle ribosomique et à la modification de l’ARN » est enrichie dans des sous-populations tumorales présentant des traits plus proches du mésenchyme — des états souvent associés à la résistance aux thérapies et à un mauvais pronostic. Dans plusieurs cohortes de patients, des niveaux élevés de cette signature prédisaient fortement une survie plus mauvaise, en particulier dans les cas de neuroblastome sans amplification du gène de risque bien connu MYCN. Des composantes spécifiques, comme le facteur d’assemblage WDR74 et l’enzyme de modification TSR3, étaient élevées dans des lignées cellulaires agressives et rendaient ces cellules plus vulnérables à des médicaments qui provoquent un stress ribosomique. Fait intriguant, les tumeurs présentant des niveaux très faibles ou très élevés de la modification clé de l’ARN au site mis en évidence évoluaient plus mal que celles avec des niveaux intermédiaires, suggérant que tant la déficience que l’excès de ce pool ribosomique spécialisé peuvent être délétères.
Ce que cela signifie pour les visages et les cancers infantiles
Ensemble, ces résultats suggèrent que les ribosomes ne sont pas de simples usines passives de protéines mais des dispositifs réglés dont la composition chimique aide à décider comment les cellules embryonnaires construisent le visage et comment certains tumeurs se comportent. Chez les cellules de la crête neurale, une marque chimique particulière sur l’ARN ribosomique semble favoriser la production de protéines nécessaires à la formation des os et du cartilage faciaux, tandis que sa dérégulation en cancérologie est liée à des cellules tumorales plus dangereuses et métamorphes. Comprendre et potentiellement cibler ce « petit détail » ribosomique pourrait ouvrir de nouvelles voies pour prévenir les malformations craniofaciales et pour identifier ou traiter les neuroblastomes à haut risque.
Citation: Poverennaya, I., Murtazina, A., Li, L. et al. Ribosomal modifications are associated with mesenchymal fate selection in the neural crest lineage. Nat Commun 17, 2326 (2026). https://doi.org/10.1038/s41467-026-70375-6
Mots-clés: développement de la crête neurale, modifications du ribosome, formation cranio-faciale, neuroblastome, ribosomes spécialisés