Clear Sky Science · fr
L’activation synchrone des interneurones cholinergiques striataux induit la libération locale de sérotonine
Pourquoi cette découverte en neurochimie compte
Les habitudes, la motivation et les comportements compulsifs dépendent d’une petite mais cruciale région du cerveau appelée le striatum. Deux neuromodulateurs bien connus, la dopamine et la sérotonine, règlent cette région, et de nombreux médicaments psychiatriques visent à ajuster leur équilibre. Cette étude révèle une voie de communication jusque-là cachée : une classe particulière de cellules nerveuses libérant de l’acétylcholine peut directement activer des fibres sérotoninergiques et les amener à libérer davantage de sérotonine, mais seulement dans une partie précise du striatum. Ce lien nouvellement mis au jour pourrait aider à expliquer pourquoi des troubles tels que le trouble obsessionnel–compulsif (TOC) et la maladie de Parkinson impliquent souvent des altérations simultanées et entremêlées de plusieurs messagers chimiques.
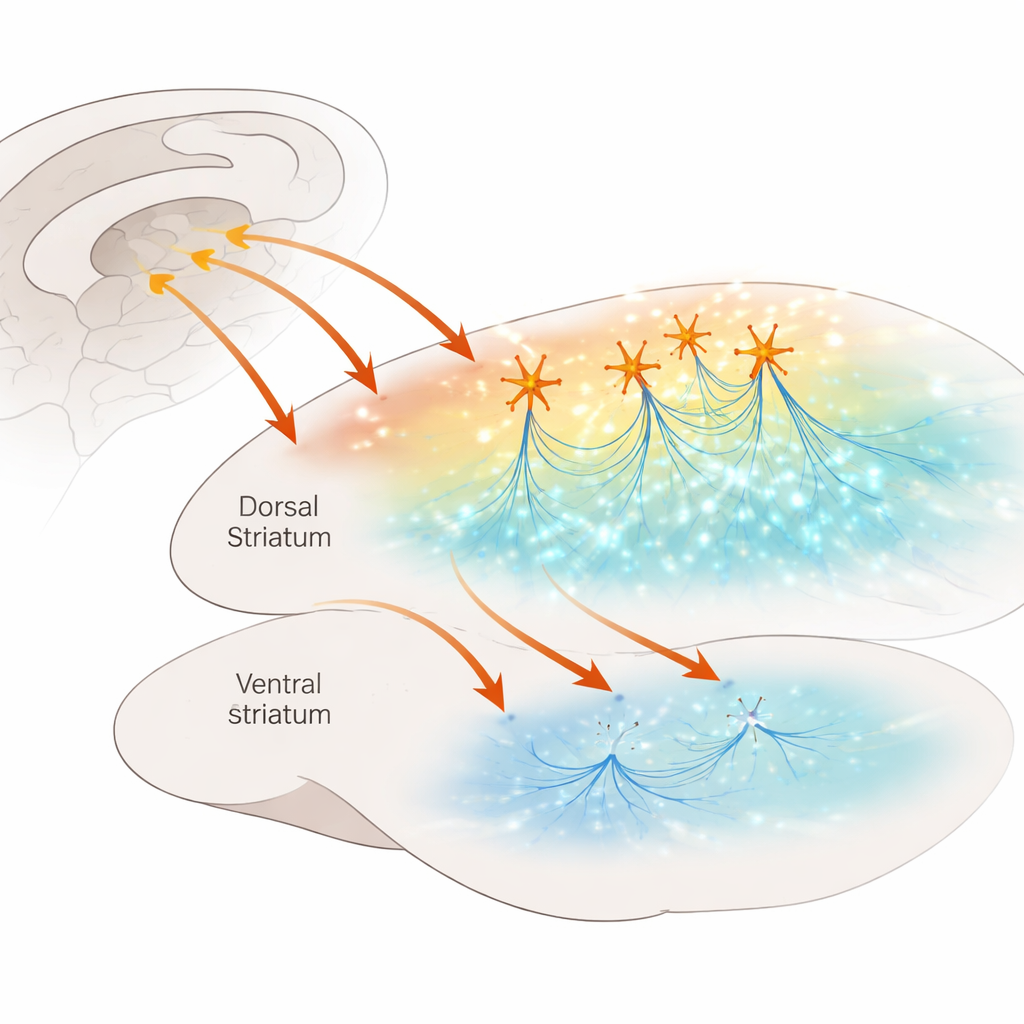
Un carrefour très fréquenté du cerveau
Le striatum dorsal fait office de centre décisionnel, nous aidant à basculer entre actions orientées vers un but et habitudes automatiques. Il reçoit des apports denses du cortex et baigne dans des neuromodulateurs tels que la dopamine et la sérotonine, qui affinent le traitement des signaux. Dans ce carrefour réside une population peu nombreuse mais puissante d’interneurones cholinergiques — des cellules qui libèrent de l’acétylcholine et tirent de façon régulière comme de petits métronomes. Des travaux antérieurs ont montré que lorsque ces cellules tirent de façon synchronisée, elles peuvent fortement augmenter la libération de dopamine en agissant sur des récepteurs nicotiniques de l’acétylcholine situés sur les fibres dopaminergiques. On ignorait si un raccourci similaire existait pour la sérotonine, alors même que celle-ci est centrale pour l’humeur, l’apprentissage et l’action des médicaments utilisés pour traiter le TOC et la dépression.
Observer la sérotonine s’allumer en temps réel
Pour aborder cette question, les chercheurs ont utilisé des souris exprimant un capteur fluorescent qui s’éclaire davantage en présence de sérotonine. Ils ont injecté un virus portant ce capteur dans le striatum, préparé de fines coupes cérébrales, puis utilisé la microscopie biphotonique pour surveiller les signaux de sérotonine pendant qu’ils stimulaient le tissu. Une stimulation électrique à l’intérieur du striatum dorsal provoquait des éclairs nets d’activité du capteur de sérotonine à décroissance lente. Lorsque l’équipe administra un médicament bloquant les récepteurs nicotiniques de l’acétylcholine, ces éclairs diminuèrent et se confinèrent spatialement, indiquant que l’acétylcholine agissant via ces récepteurs contribue à la fois à augmenter la libération de sérotonine et à en étendre la diffusion. Fait frappant, répéter la même expérience dans le striatum ventral — une région voisine dotée d’un maillage sérotoninergique encore plus dense — ne montra pas cette contribution nicotinique, révélant que cette interaction croisée est spécifique à une région.
Déclencher la sérotonine par lumière ciblée
Pour savoir si l’acétylcholine issue seulement des interneurones cholinergiques peut provoquer la libération de sérotonine, les auteurs ont eu recours à l’optogénétique. Ils ont rendu ces interneurones sensibles à de brefs éclairs de lumière bleue ou jaune et les ont activés de façon synchrone tout en continuant à surveiller le capteur de sérotonine. Une seule milliseconde de lumière suffisait à provoquer un signal de sérotonine robuste dans le striatum dorsal, avec une chronologie semblable à la composante sensible aux nicotiniques de la réponse évoquée électriquement. Le blocage des récepteurs nicotiniques abolissait presque complètement ce signal, même lorsque d’autres entrées chimiques et récepteurs dans la coupe étaient pharmacologiquement silencés. Cette combinaison de stimulation précise et de blocage récepteur montre que l’acétylcholine agit directement sur des récepteurs nicotiniques le long des fibres sérotoninergiques pour déclencher une libération locale de sérotonine, plutôt que de dépendre de voies indirectes via d’autres types cellulaires ou des axones dopaminergiques.
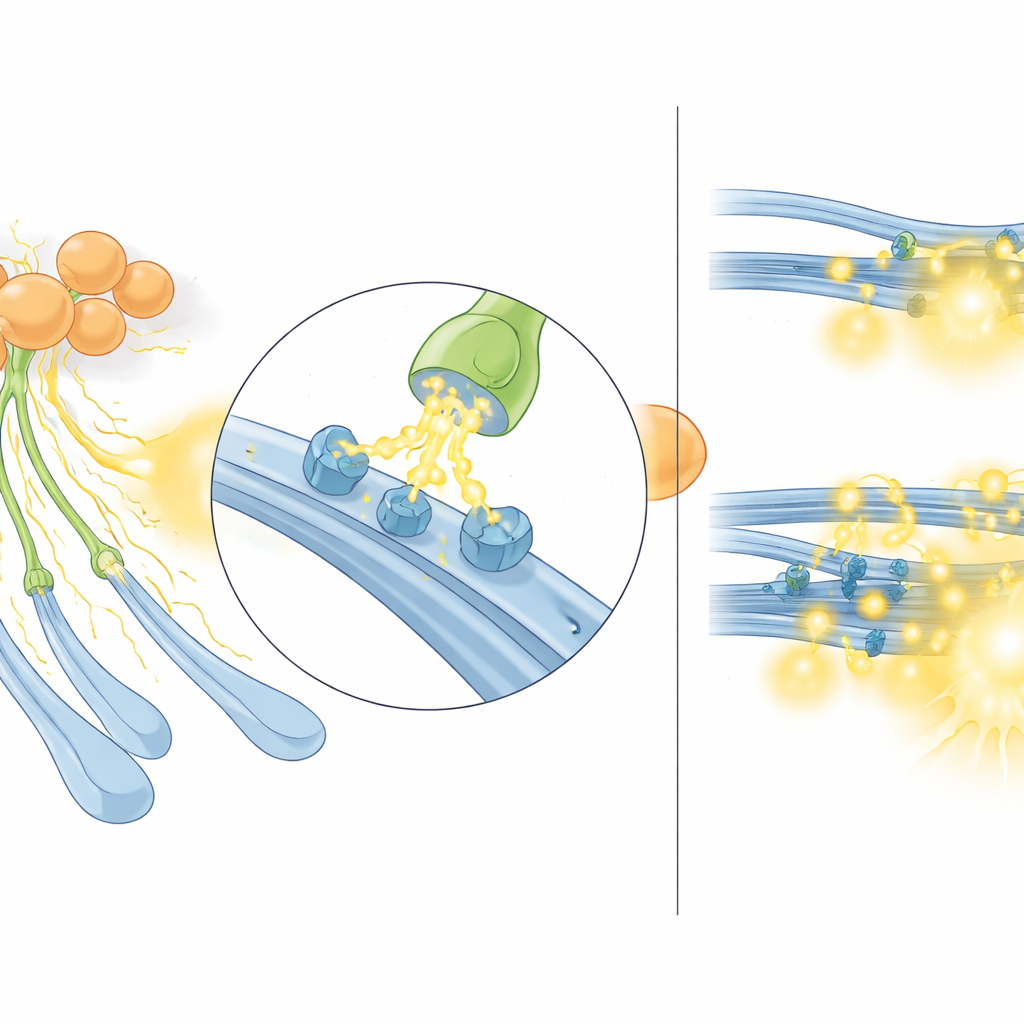
Quand le système s’emballe
L’équipe s’est ensuite demandé ce qui se passe dans un état pertinent pour la maladie où la signalisation cholinergique est anormalement forte. Ils ont utilisé des souris Sapap3 knock-out, un modèle bien établi qui présente un toilettage excessif et d’autres comportements ressemblant au TOC, et chez lequel on avait déjà montré une activité accrue des interneurones cholinergiques et une libération d’acétylcholine plus élevée. Chez ces souris, la stimulation électrique du striatum dorsal produisait des signaux du capteur de sérotonine plus importants que chez des animaux normaux. De façon importante, cette différence disparaissait lorsque les récepteurs nicotiniques étaient bloqués, ce qui signifie que seule la portion dépendante de l’acétylcholine de la libération de sérotonine était amplifiée. Un schéma similaire s’appliquait à la dopamine. Autrement dit, dans cet état hypercholinergique, les interneurones cholinergiques amplifient de manière disproportionnée la composante nicotinique de la libération de monoamines, laissant en pratique l’acétylcholine « détourner » les fibres sérotoninergiques comme voie principale de sortie de la sérotonine.
Implications plus larges pour les troubles cérébraux
Ces résultats révèlent une interaction finement réglée et confinée régionalement entre l’acétylcholine et la sérotonine dans le striatum dorsal. Dans des cerveaux sains, des rafales synchrones d’activité des interneurones cholinergiques — par exemple celles déclenchées par des événements soudains et importants sur le plan comportemental — peuvent temporairement agrandir et renforcer les signaux de sérotonine, influençant la façon dont les actions sont apprises ou supprimées. Dans des états pathologiques où l’acétylcholine est de façon persistante élevée, comme chez les souris Sapap3 knock-out et possiblement dans des affections telles que le TOC ou la maladie de Parkinson, ce même mécanisme peut devenir exagéré, contribuant à des schémas anormaux de signalisation de la sérotonine et de la dopamine. Comprendre ce lien caché offre une nouvelle perspective sur la manière dont plusieurs neuromodulateurs interagissent dans le comportement normal et la maladie, et pourrait éventuellement orienter des traitements visant plus précisément leur dynamique conjointe plutôt que de traiter chaque messager chimique isolément.
Citation: Matityahu, L., Hobel, Z.B., Berkowitz, N. et al. Synchronous activation of striatal cholinergic interneurons induces local serotonin release. Nat Commun 17, 2278 (2026). https://doi.org/10.1038/s41467-026-70359-6
Mots-clés: sérotonine striatale, interneurones cholinergiques, récepteurs nicotiniques de l’acétylcholine, trouble obsessionnel compulsif, ganglions de la base