Clear Sky Science · fr
Contrôle de la fonction lysosomale par la protéine activatrice de GTPase TBC1D9B et son partenaire de liaison TMEM55B
Comment les centres de recyclage cellulaires maintiennent l’équilibre
À l’intérieur de chacune de nos cellules se trouvent de petites poches appelées lysosomes qui font office de centres de recyclage et de centres de contrôle pour la croissance. Lorsqu’ils fonctionnent correctement, les éléments usés sont dégradés et leurs composants réutilisés ; lorsqu’ils défaillent, les déchets s’accumulent et des maladies, notamment des troubles neurodégénératifs et des cancers, peuvent apparaître. Cette étude révèle comment deux protéines peu connues contribuent à basculer les lysosomes entre un état nomade favorisant la croissance et un mode regroupé axé sur le nettoyage des déchets, faisant la lumière sur la façon dont les cellules s’adaptent à l’abondance ou à la privation.
Déplacer les centres de recyclage dans la cellule
Les lysosomes ne sont pas fixes. Ils voyagent le long de pistes internes, tirés vers l’extérieur par un ensemble de moteurs moléculaires et ramenés vers l’intérieur par un autre. Leur position dans la cellule est importante : lorsque les nutriments sont abondants, les lysosomes se dispersent vers la périphérie cellulaire et contribuent à soutenir les signaux de croissance ; lorsque la nourriture se fait rare, ils se replient vers le centre, deviennent plus acides et renforcent la dégradation de la matière cellulaire. Une petite protéine de type commutateur appelée ARL8 est connue pour pousser les lysosomes vers l’extérieur, mais jusqu’à présent personne n’avait identifié un système de freinage dédié pour la maîtriser. Les auteurs ont supposé qu’un tel frein serait crucial pour permettre aux cellules de passer rapidement en mode conservation lors d’une privation.
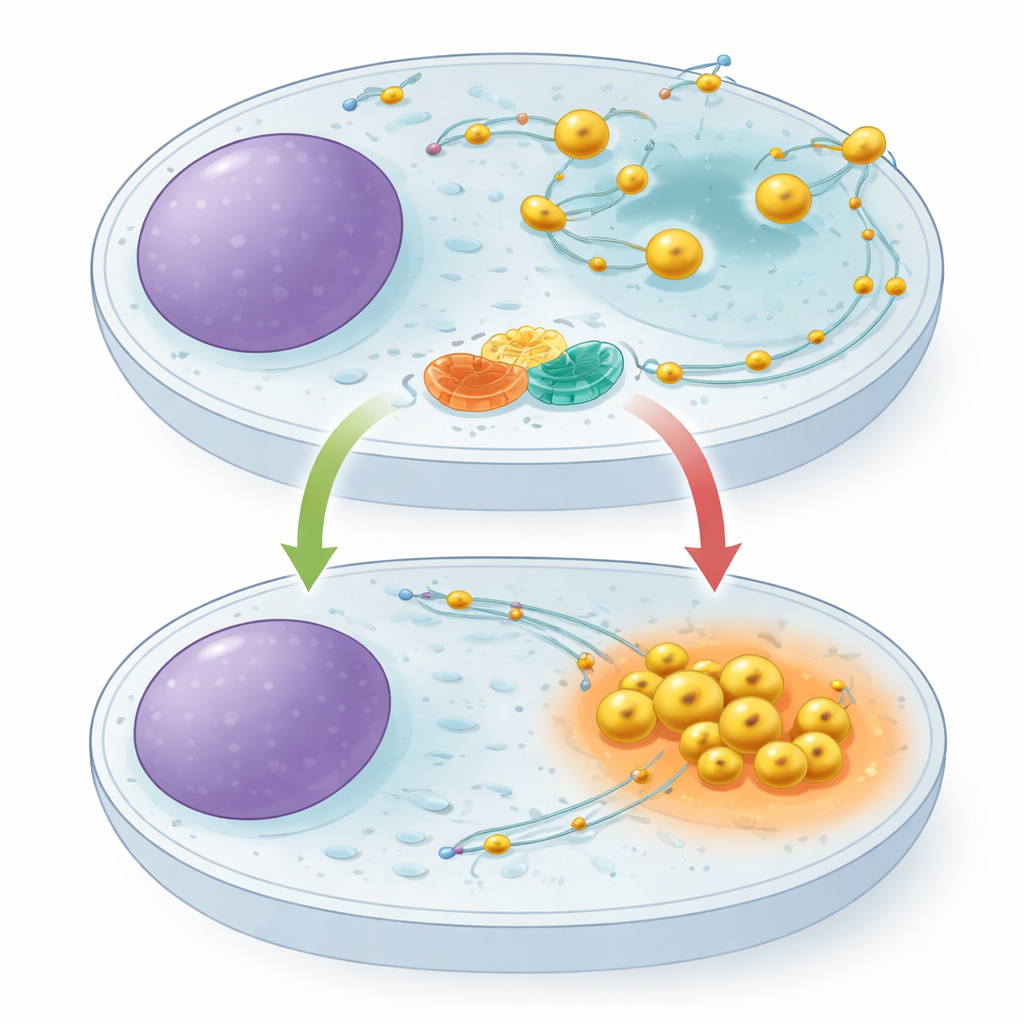
Un partenariat moléculaire à la surface du lysosome
En utilisant des techniques de pêche protéique et la spectrométrie de masse, les chercheurs ont découvert qu’une protéine nommée TBC1D9B s’attache à une protéine membranaire lysosomale appelée TMEM55B. TMEM55B traverse l’enveloppe externe du lysosome, tandis que TBC1D9B est en grande partie soluble et peut s’ancrer sur la membrane. L’équipe a montré que ces deux protéines forment un complexe direct : la TBC1D9B purifiée se lie à la partie exposée de TMEM55B en éprouvette, et des versions marquées des protéines s’enrichissent mutuellement à partir d’extraits cellulaires. Une cartographie minutieuse des segments protéiques a révélé que plusieurs régions de TBC1D9B contactent TMEM55B, positionnant TBC1D9B à la surface du lysosome sans bloquer la partie de la protéine responsable de son activité catalytique.
Quand le frein lâche, les lysosomes partent à la dérive
Pour déterminer ce que fait ce partenariat, les auteurs ont utilisé l’édition CRISPR pour supprimer soit TMEM55B soit TBC1D9B dans des cellules humaines. Dans les deux cas, les lysosomes ne se regroupaient plus près du noyau mais se dispersaient vers le bord cellulaire et se déplaçaient plus rapidement le long de leurs pistes, reproduisant l’état de cellules constamment nourries. La réintroduction de TBC1D9B normal a rétabli le positionnement correct, mais une version dépourvue d’activité catalytique ne l’a pas fait, indiquant que son activité enzymatique est essentielle. Lorsque les cellules ont été privées de nutriments, les cellules contrôle ont ramené leurs lysosomes vers l’intérieur et augmenté leur pouvoir digestif, comme le montre l’activité accrue d’enzymes clés et l’amplification de la dégradation d’un cargo test. Les cellules dépourvues de TMEM55B ou de TBC1D9B n’ont pas pu faire cela : leurs lysosomes sont restés périphériques et leur réponse dégradative à la privation a été atténuée. L’autophagie, le processus par lequel les cellules digèrent elles‑mêmes les composants endommagés, a également été compromise, avec un traitement moins efficace d’un rapporteur d’autophagie et l’accumulation de la protéine adaptatrice p62.
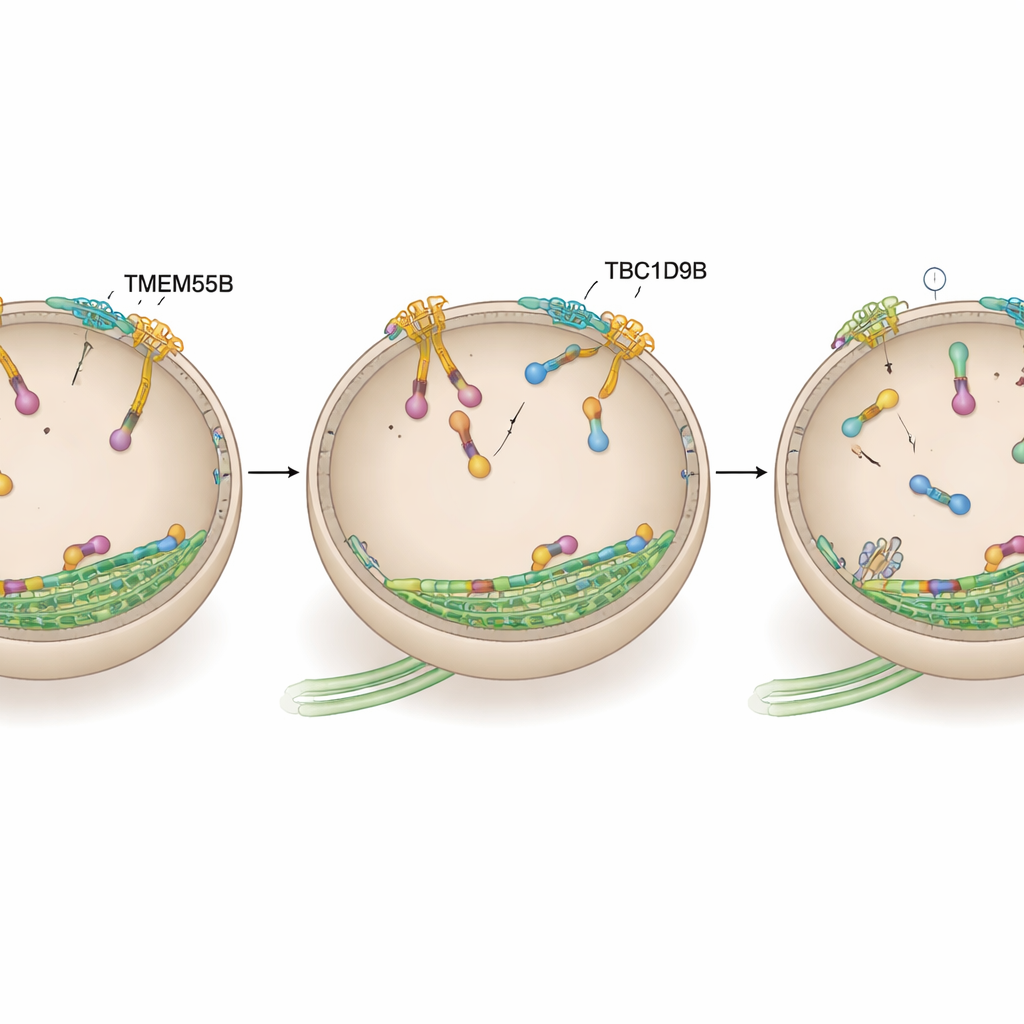
Désactiver le moteur lysosomal
L’équipe a ensuite cherché à savoir si TBC1D9B exerce ses effets en agissant directement sur ARL8, le commutateur moteur qui pousse vers l’extérieur. En utilisant le marquage de proximité dans des neurones humains et des tests d’interaction dans des lignées cellulaires et avec des protéines purifiées, ils ont montré que TBC1D9B se lie sélectivement à la forme active liée au GTP de la variante ARL8B, mais pas à sa forme inactive ni à l’ARL8A étroitement apparentée. La modélisation structurelle a prédit que des résidus clés de TBC1D9B contactent la poche à GTP d’ARL8B. Dans des essais biochimiques, TBC1D9B a accéléré l’hydrolyse du GTP lié à ARL8B, convertissant effectivement la protéine de son état « marche » à son état « arrêt » ; une version mutante de TBC1D9B dépourvue de ces résidus ne pouvait plus le faire. Conformément à cela, les cellules dépourvues de TMEM55B ou de TBC1D9B présentaient une augmentation d’ARL8B sur les lysosomes, tandis que la surexpression de TBC1D9B ramenait les lysosomes vers le centre, similaire à une réduction de l’activité d’ARL8B.
Un nouveau bouton de réglage pour l’entretien cellulaire
Enfin, les auteurs ont testé si ce frein sur ARL8B expliquait les changements cellulaires observés lorsque TBC1D9B manque. Lorsque ARL8B a été éliminé, les lysosomes sont restés regroupés près du noyau quel que soit le statut de TMEM55B ou TBC1D9B, et les défauts d’autophagie causés par la perte de TBC1D9B ont été en grande partie annulés. Ensemble, les données soutiennent un modèle dans lequel TMEM55B recrute TBC1D9B aux lysosomes, où celui‑ci inactive ARL8B et permet aux lysosomes de passer d’un état dispersé, favorable à la croissance, à un état centralisé, axé sur la digestion. Pour les non‑spécialistes, cela signifie que l’étude a mis au jour un bouton de réglage important que les cellules utilisent pour décider quand recycler plus agressivement, un processus ayant des implications pour les troubles d’accumulation de déchets dans le cerveau, le métabolisme et le cancer.
Citation: Duhay, V., Tian, M., Kosieradzka, K. et al. Control of lysosome function by the GTPase-activating protein TBC1D9B and its binding partner TMEM55B. Nat Commun 17, 2487 (2026). https://doi.org/10.1038/s41467-026-70345-y
Mots-clés: lysosomes, autophagie, signalisation cellulaire, transport d’organites, neurodégénérescence