Clear Sky Science · fr
Des fragments de SLIT3 orchestrent l’expansion neurovasculaire et la thermogenèse dans le tissu adipeux brun
Comment notre « bon gras » nous aide à rester au chaud
Quand nous entrons dans le froid, notre organisme se mobilise rapidement pour nous maintenir à température. Un acteur clé de cette réponse est la graisse brune, un type de tissu adipeux qui brûle des calories pour produire de la chaleur. Cette étude révèle comment la graisse brune organise ses petits vaisseaux sanguins et ses fibres nerveuses pour augmenter la production de chaleur, mettant au jour un système de communication caché qui pourrait un jour être exploité pour améliorer le métabolisme et traiter les maladies liées à l’obésité.
Une fournaise cachée à l’intérieur du corps
Le tissu adipeux brun, ou graisse brune, fonctionne comme une fournaise interne. À la différence du tissu adipeux blanc qui stocke l’énergie, la graisse brune consomme du carburant pour générer de la chaleur lorsqu’on est exposé au froid. Pour ce faire efficacement, les cellules de graisse brune ont besoin d’un apport sanguin abondant pour fournir oxygène et nutriments, et d’un réseau dense de nerfs sympathiques qui signalent quand augmenter la production de chaleur. Face au froid, ces vaisseaux et ces nerfs se développent de manière remarquable. Jusqu’ici, on ne comprenait pas clairement comment ces différentes composantes du tissu coordonnaient leur croissance aussi précisément.
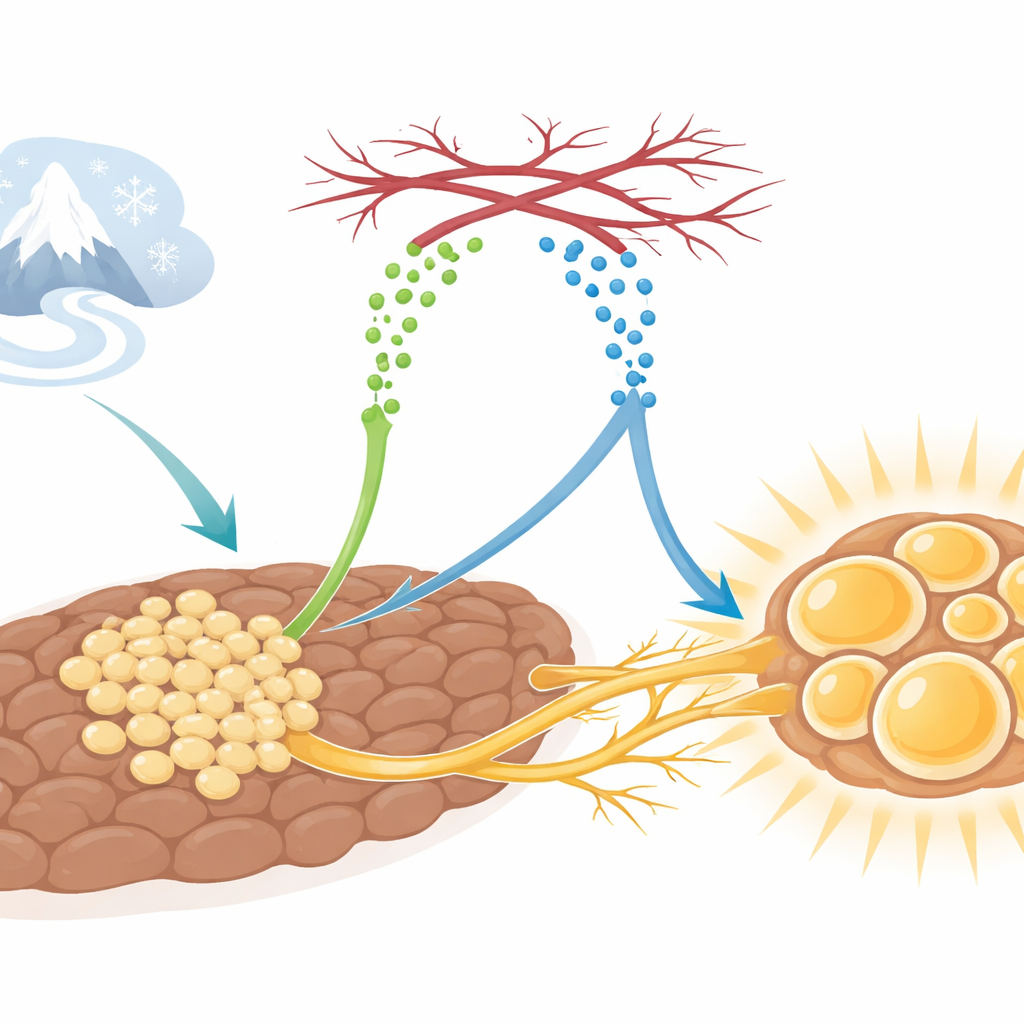
La molécule messagère qui déclenche tout
Les chercheurs ont identifié une protéine appelée SLIT3, produite par des cellules adipeuses immatures connues sous le nom de progéniteurs adipeux, comme élément central de cette coordination. Chez les souris exposées au froid, les niveaux de SLIT3 dans la graisse brune augmentent. Lorsque l’équipe a bloqué SLIT3 spécifiquement dans la graisse brune ou dans ces cellules progénitrices, les animaux ont eu du mal à maintenir leur température corporelle au froid. Leur tissu adipeux brun est devenu plus « blanchi », avec des gouttelettes lipidiques plus grosses, une expression plus faible de gènes thermogéniques comme Ucp1, et une dépense énergétique réduite, alors même que la prise alimentaire et l’activité étaient inchangées. Ces observations désignent SLIT3 comme un organisateur clé de la réponse de la graisse brune au froid, non pas en modifiant la machinerie interne de chaque cellule, mais en façonnant l’environnement tissulaire autour d’elles.
Construire vaisseaux sanguins et câbles nerveux de concert
En observant de plus près, les scientifiques ont constaté que la graisse brune dépourvue de SLIT3 présentait moins de capillaires et moins de fibres nerveuses sympathiques parcourant le tissu. L’imagerie tridimensionnelle a confirmé que le réseau nerveux était nettement plus clairsemé. Fait important, lorsque le signal nerveux habituel était contourné grâce à un médicament qui active directement la graisse brune, les cellules répondaient normalement. Cela démontre que SLIT3 n’est pas nécessaire pour que les cellules adipeuses brûlent du carburant, mais pour construire le « câblage » neurovasculaire permettant au cerveau de les contrôler. L’équipe a identifié les progéniteurs adipeux comme la principale source locale de SLIT3 et montré que la suppression de SLIT3 uniquement dans ces cellules suffisait à atténuer la croissance des vaisseaux, la croissance nerveuse et la production de chaleur lors de l’exposition au froid.
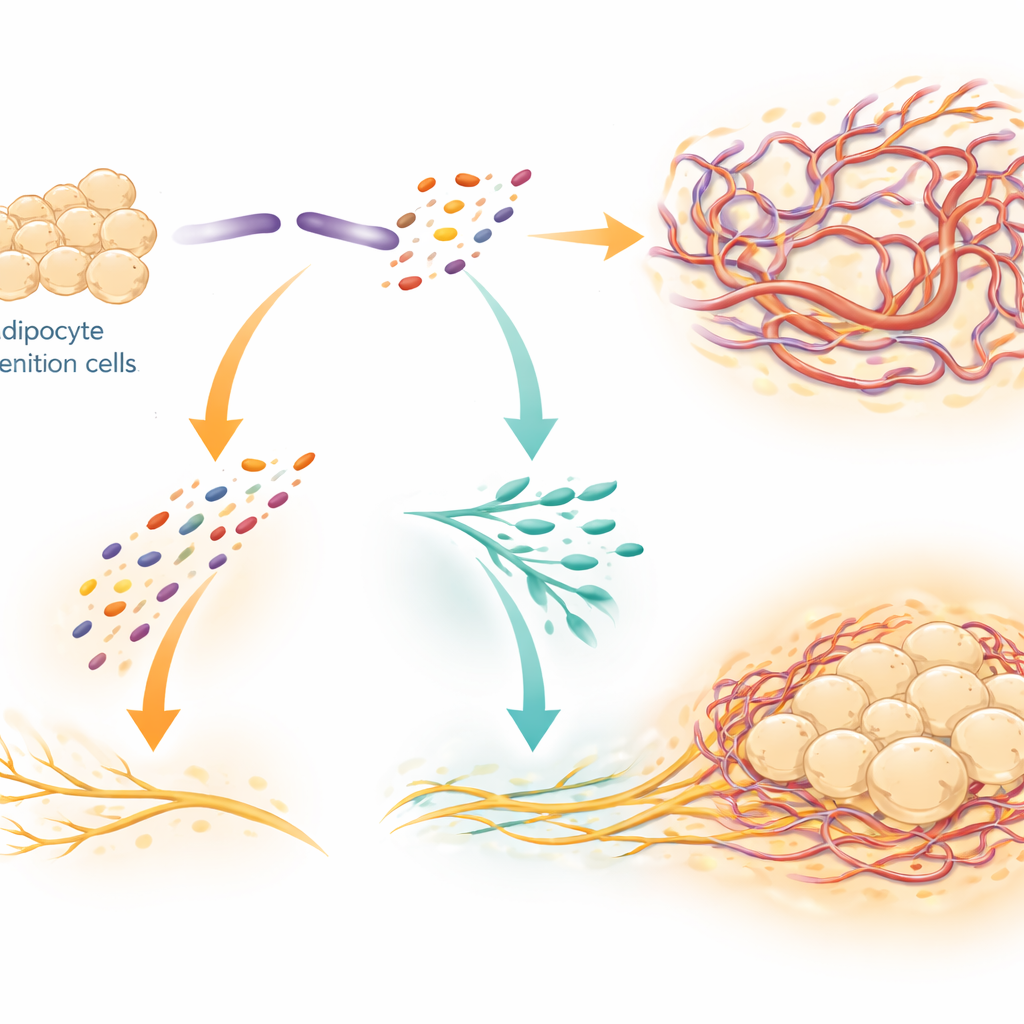
Une protéine, deux fragments, deux fonctions
SLIT3 n’agit pas comme un signal unique et statique. Les chercheurs ont montré qu’une enzyme appelée BMP1 coupe SLIT3 en deux fragments distincts ayant des rôles différents. Le fragment N-terminal (SLIT3-N) stimule principalement la croissance des capillaires, en agissant via des récepteurs sur les cellules endothéliales qui tapissent les vaisseaux sanguins. Le fragment C-terminal (SLIT3-C) favorise surtout l’expansion des nerfs sympathiques. Ils ont identifié un récepteur nommé PLXNA1 sur les fibres nerveuses comme un partenaire d’accostage direct pour SLIT3-C, soutenu par des tests biochimiques d’interaction et des modèles structurels informatiques. Quand PLXNA1 était réduit, la capacité de SLIT3 ou de SLIT3-C à renforcer la croissance nerveuse et à élever la température de la graisse brune disparaissait, et la densité nerveuse globale ainsi que les niveaux de noradrénaline dans le tissu chutaient fortement.
Liens avec le métabolisme et la santé humaine
Pour vérifier si ce système a une importance chez l’homme, les auteurs ont analysé des échantillons de graisse issus de larges cohortes d’obésité humaine. Une expression plus élevée de SLIT3 dans le tissu adipeux était associée à des profils plus sains : davantage d’adiponectine, moins de cellules immunitaires inflammatoires dans la graisse viscérale, un meilleur contrôle de la glycémie et des niveaux plus élevés de l’adipokine bénéfique omentine. Des études génétiques antérieures ont également relié des variantes près de SLIT3 et de son récepteur PLXNA1 à l’obésité et à la résistance à l’insuline. Ensemble, ces éléments suggèrent que la voie SLIT3 pourrait contribuer au maintien d’un tissu adipeux sain et d’un équilibre métabolique chez l’humain.
Ce que cela signifie pour rester au chaud et en bonne santé
Dans l’ensemble, l’étude montre que les cellules adipeuses immatures de la graisse brune font plus que se transformer en cellules matures : elles sculptent activement le réseau de soutien du tissu. En libérant SLIT3 et en permettant sa découpe en deux fragments, elles stimulent de manière indépendante mais synchronisée la croissance des vaisseaux sanguins et des nerfs nécessaires à une thermogenèse efficace. Ce système de signalisation finement réglé « deux en un » garantit que la graisse brune peut se préparer rapidement quand l’environnement exige plus de chaleur. À long terme, comprendre et exploiter en toute sécurité cette voie pourrait ouvrir de nouvelles pistes pour augmenter la dépense énergétique, améliorer la santé du tissu adipeux et lutter contre les maladies métaboliques.
Citation: Serdan, T.D.A., Cervantes, H., Frank, B. et al. SLIT3 fragments orchestrate neurovascular expansion and thermogenesis in brown adipose tissue. Nat Commun 17, 2445 (2026). https://doi.org/10.1038/s41467-026-70310-9
Mots-clés: tissu adipeux brun, thermogenèse, remodelage neurovasculaire, signalisation SLIT3, santé métabolique